Le test immunochimique fécal, ou FIT, est un test simple et non invasif destiné aux patients qui présentent à leur médecin des symptômes liés au cancer de l’intestin. Il s’agit d’un test de selles qui permet de détecter de manière fiable d’infimes quantités de sang humain dans les selles qui ne sont pas toujours visibles à l’œil nu. La plupart des cancers de l’intestin saignent à des degrés divers dans le côlon et se mélangent aux selles. Le FIT a été largement utilisé dans les programmes de dépistage du cancer de l’intestin, mais étonnamment, ce n’est qu’avec la restriction de l’accès aux soins de santé que le COVID a suscité l’intérêt d’étendre son utilisation clinique aux patients présentant des symptômes de cancer de l’intestin. Nous avons émis l’hypothèse que le test FIT pourrait mesurer la quantité de sang dans les selles des patients présentant des symptômes préoccupants et les classer en différents groupes à risque de cancer colorectal pour aider les médecins à déterminer la nécessité et l’urgence de recommander des investigations plus approfondies. envahissant le côlon. |
L’incidence et la mortalité dues au cancer colorectal augmentent dans certains pays. Les programmes de dépistage intestinal de la population ont accru la demande sur des ressources limitées en endoscopie.
Les patients présentant des symptômes colorectaux qui soulèvent la possibilité d’un diagnostic de cancer colorectal sont également en concurrence pour la capacité d’endoscopie, ce qui peut entraîner des retards dans le diagnostic et de moins bons résultats du traitement.
Les symptômes à eux seuls sont de mauvais prédicteurs d’un diagnostic de cancer colorectal. Une revue systématique précédente avait conclu qu’un test immunochimique fécal (FIT) était cliniquement utile et rentable pour le tri des patients présentant des symptômes d’un éventuel cancer colorectal.
Cela a conduit à un changement dans les recommandations de l’Institut national britannique pour la santé et les soins d’excellence (NICE) afin d’inclure l’utilisation du FIT chez les patients symptomatiques. La pandémie de COVID-19 a encore plus limité l’accès à l’endoscopie, favorisant un intérêt accru pour la FIT comme outil de triage pour les patients présentant des symptômes colorectaux.
Trois méta-analyses précédentes de petites études de cohorte ont conclu qu’au seuil d’hémoglobine fécale (f-Hb) de 10 µg Hb/g de selles, le FIT est utile pour exclure le cancer colorectal chez les patients symptomatiques.
Cependant, des études de cohorte plus vastes ont depuis été publiées, une méta-analyse mise à jour est donc nécessaire. De plus, de plus en plus de questions ont été soulevées quant à l’applicabilité du FIT chez les patients présentant des symptômes spécifiques, et il existe des rapports contradictoires sur la manière dont le FIT a influencé la prestation de services.
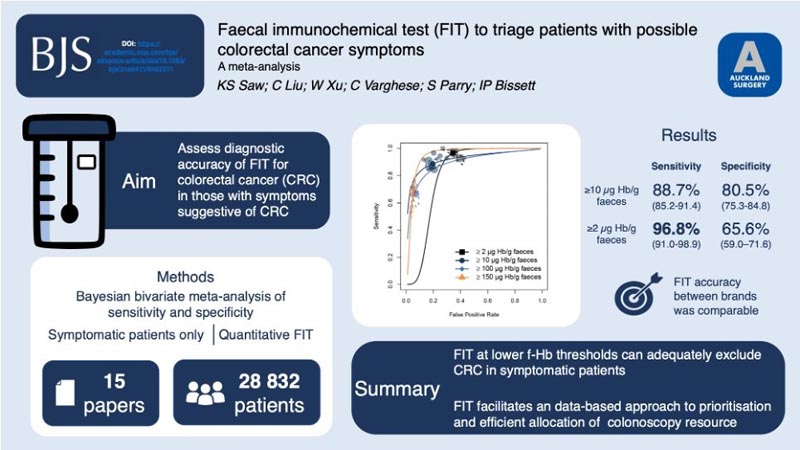
Cette revue a évalué l’utilité du test immunochimique fécal quantitatif unique (FIT) comme outil de triage pour les patients présentant des symptômes d’un éventuel cancer colorectal, l’effet des symptômes sur l’exactitude du FIT et l’impact de l’intégration du FIT sur la prestation de services.
L’ objectif principal de cette méta-analyse était d’évaluer l’utilité du FIT quantitatif comme outil de triage à des seuils de f-Hb inférieurs pour exclure les patients symptomatiques des investigations invasives, et à des seuils de f-Hb plus élevés pour prioriser l’urgence de l’investigation.
Les objectifs secondaires étaient d’évaluer si des symptômes spécifiques ont un impact sur les performances du diagnostic FIT et d’évaluer l’impact de la classification FIT sur la prestation de services.
Méthodes
Cinq bases de données ont été consultées. Des méta-analyses ont été réalisées sur les sensibilités et les spécificités des FIT extraits pour la détection du cancer colorectal aux seuils f-Hb rapportés. Les critères de jugement secondaires comprenaient la sensibilité et la spécificité du FIT pour la néoplasie colorectale avancée et les maladies intestinales graves. Une analyse de sous-groupe a été réalisée par marque FIT et par symptômes.
Résultats
Quinze études de cohortes prospectives ont été incluses, incluant 28 832 patients symptomatiques. Au seuil de positivité f-Hb le plus fréquemment rapporté de ≥ 10 µg Hb/g de selles (n = 13), la sensibilité résumée était de 88,7 % (IC à 95 % entre 85,2 et 91,4) et la spécificité était de 80,5 % (IC à 95 % entre 75,3 et 84,8). ) pour le cancer colorectal.
Aux limites inférieures de détection de ≥ 2 µg Hb/g dans les selles, la sensibilité sommaire était de 96,8 % (IC à 95 % entre 91,0 et 98,9) et la spécificité était de 65,6 % (IC à 95 % entre 59,0 et 71,6).
Aux seuils supérieurs de positivité f-Hb de ≥ 100 µg Hb/g de selles et ≥ 150 µg Hb/g de selles, les sensibilités sommaires étaient de 68,1 % (IC à 95 % entre 59,2 et 75,9) et 66,3 % (IC à 95 % entre 52,2 et 78,0). ), avec des spécificités de 93,4 % (95 % ci 91,3 à 95,1) et 95,1 % (95 % ci 93,6 à 96, 3) respectivement.
La sensibilité du FIT était comparable entre les différentes marques de tests.
Discussion
Notre analyse a montré qu’au niveau le plus bas possible de sang fécal détectable par FIT (≥2 microgrammes d’Hb/g de selles), un test FIT positif détecterait environ 96 cancers colorectaux sur 100. Dans deux des plus grandes études menées au Royaume-Uni, jusqu’à 63 % des patients qui, selon les normes actuelles, subiraient une exploration invasive du côlon en raison de symptômes signalés, pourraient l’éviter.
Lorsque les paramètres sont ajustés pour être conformes aux recommandations actuelles du National Institute for Health and Care Excellence (NICE) (≥ 10 microgrammes d’Hb/g de selles), un test FIT positif détecterait environ 88 cancers colorectaux sur 100.
Si l’on obtient un test FIT négatif dans ce contexte, on estime qu’environ seulement 1 patient sur 243 subissant une investigation invasive du côlon aurait un cancer détecté, ce qui signifie que dans les pratiques contemporaines, 242 patients assumeraient le risque d’une coloscopie. même si je n’ai pas de cancer de l’intestin.
En revanche, si FIT détecte des taux de sang plus élevés dans les selles (tels que ≥ 100 ou ≥ 150 microgrammes d’Hb/g dans les selles), environ 1 patient sur 3 recevra un diagnostic de cancer de l’intestin.
- Pour les patients présentant des symptômes, ces résultats indiquent que lorsque le FIT détecte de très faibles taux de sang dans les selles, les risques de cancer de l’intestin sont suffisamment faibles pour qu’une investigation invasive puisse être évitée .
- Au contraire, si le FIT indique des taux sanguins relativement plus élevés , la probabilité de cancer de l’intestin est très élevée et une investigation urgente du côlon serait idéale pour détecter et traiter le cancer le plus tôt possible.
Aucun test n’est parfait. On estime que l’étalon-or actuellement accepté, la coloscopie, ne permet pas de détecter 5 cancers sur 100. (4) Avec la configuration correcte, notre analyse suggère que FIT se rapproche de cette précision diagnostique sans être invasif, accessible et bon marché. Bien que les tests d’imagerie du côlon jouent un rôle irremplaçable dans le diagnostic du cancer de l’intestin, il serait peut-être plus optimal pour les patients, les médecins et les systèmes de santé de rationaliser l’utilisation de la coloscopie et de la colonographie afin d’éviter les retards. dans le diagnostic et le traitement des personnes considérées comme présentant un risque accru de cancer de l’intestin.
Les résultats de cette revue systématique et de cette méta-analyse suggèrent qu’un seul FIT quantitatif avec de faibles seuils de positivité pour la f-Hb peut exclure de manière adéquate le cancer colorectal chez les patients référés présentant des symptômes d’un éventuel cancer colorectal.
Davantage de données sur les performances du FIT aux seuils supérieurs de f-Hb pourraient valider davantage son utilité en tant qu’outil de priorisation. FIT facilite une approche basée sur les données pour la priorisation et une allocation plus efficace des ressources de coloscopie.
Ces résultats pourraient potentiellement réduire le taux d’examens coliques inutiles et libérer la capacité de coloscopie pour les initiatives de dépistage et de surveillance du cancer colorectal.
Conclusion Un FIT quantitatif unique avec des seuils de positivité f-Hb inférieurs peut exclure de manière adéquate le cancer colorectal chez les patients symptomatiques et fournit une approche basée sur les données pour prioriser les ressources en coloscopie. |