Résumé
Précipitées par un stress psychologique chronique, une dérégulation du système immunitaire et un état hyperinflammatoire, les séquelles du COVID-19 post-aigu (long COVID) comprennent la dépression et l’apparition d’un diabète.
Nous émettons l’hypothèse que l’exercice neutralise les séquelles neuropsychiatriques et endocriniennes du long COVID en induisant la libération de facteurs circulants qui médient la réponse anti-inflammatoire, soutiennent l’homéostasie cérébrale et augmentent la sensibilité à l’insuline.
Mots-clés : exercice, COVID-19, stress psychologique, dérégulation immunitaire, hyperinflammation
Points clés
|
Le coronavirus 2 (SARS-CoV-2) du syndrome respiratoire aigu sévère est l’agent pathogène à l’origine de la maladie à coronavirus 2019 (COVID-19) et a contribué à des millions de décès dans le monde. Dans certains cas, des symptômes persistants et l’apparition de séquelles surviennent 4 à 12 semaines après l’apparition des symptômes aigus du COVID-19 (COVID long).
La réponse en anticorps est compatible avec une immunité durable contre la maladie secondaire au COVID-19. Cependant, l’ARNm et la protéine du SRAS-CoV-2 sont actifs dans l’épithélium de l’intestin grêle de certaines personnes près de 6 mois après le diagnostic du COVID-19.
La physiopathologie sous-jacente du COVID-19 présente de multiples facettes et ses composantes semblent inextricablement liées. La variabilité des trajectoires cliniques de la maladie chez les patients atteints de COVID-19 est marquée par des disparités qui dépassent les points communs. Par conséquent, comprendre les mécanismes cellulaires et évaluer de manière critique la convergence entre les observations devient nécessaire pour parvenir à une stratégie éclairée permettant de gérer le risque de COVID long et de prévenir son escalade.
Le SRAS-CoV-2 se lie au récepteur ACE2 exprimé sur les cellules β pancréatiques et induit des dommages cellulaires qui peuvent aggraver un diabète préexistant ou précipiter l’apparition du diabète. L’acidocétose diabétique généralement observée dans le diabète de type 1, qui est une maladie auto-immune, survient chez des patients sans diagnostic de diabète préexistant des semaines ou des mois après la résolution du COVID-19. Les cytokines telles que l’interleukine-6 (IL-6) et le facteur de nécrose tumorale α (TNF-α) sont élevées chez les patients atteints de COVID-19 sévère.
L’inactivité physique est associée à un risque plus élevé de développer un diabète de type 2 et à des conséquences plus graves de la COVID-19.
Les risques qu’une personne physiquement inactive subisse des conséquences graves à cause du COVID-19 dépassent ceux de la plupart des maladies chroniques (6). Nous émettons l’hypothèse que l’exercice favorise la libération de médiateurs circulants essentiels à l’atténuation des symptômes neuroendocriniens à long terme du COVID-19.
Dans cette revue, nous présentons des informations biologiques sur les schémas de stress inadaptés qui prédisposent les personnes à la dépression clinique et à la dérégulation du glucose caractéristiques du diabète de type 2. Nous évaluons les preuves pour étayer notre hypothèse testable selon laquelle l’exercice peut prévenir ou atténuer les conséquences à long terme du COVID-19.
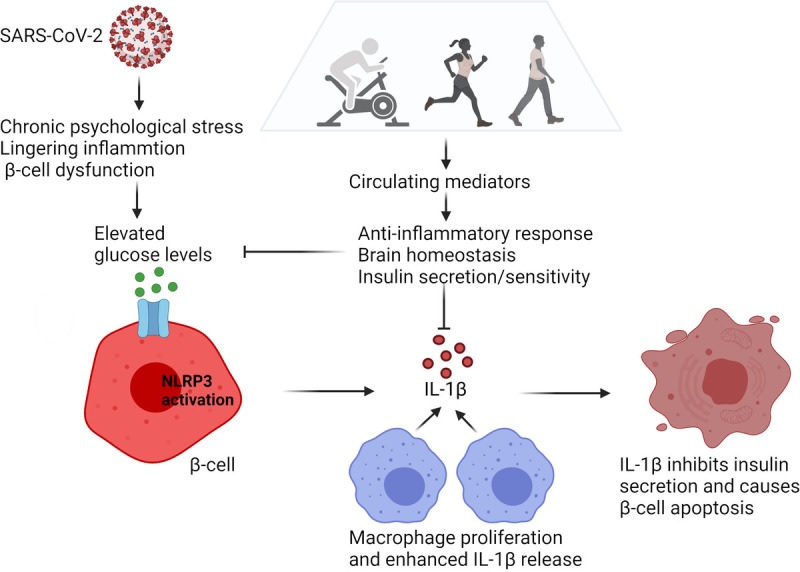
Le développement d’une hyperglycémie résultant d’une perturbation de l’homéostasie métabolique immunitaire dans le cas du COVID-19. Des taux de glucose élevés induits par un stress psychologique, une inflammation persistante et un dysfonctionnement des cellules β peuvent conduire à l’activation de l’inflammasome NLRP3 dans les cellules β pancréatiques. En conséquence, la pro-IL-1β est transformée en IL-1β biologiquement active. L’IL-1β libérée par les cellules β provoque le recrutement et l’activation des macrophages, conduisant à la libération de davantage d’IL-1β. Des concentrations locales élevées d’IL-1β dans le microenvironnement des cellules β peuvent inhiber la sécrétion d’insuline et déclencher un dysfonctionnement et l’apoptose des cellules β. Cela conduit à de nouvelles augmentations des taux de glucose, provoquant ainsi une autostimulation de l’IL-1β et établissant un cercle vicieux. L’exercice induit la libération de facteurs circulants qui médient la réponse anti-inflammatoire, soutiennent l’homéostasie cérébrale et augmentent la sensibilité à l’insuline. L’effet net est la réduction des niveaux de glucose et pourrait être conçu comme une thérapie d’induction de rémission pour contrecarrer les séquelles du COVID-19 (programme graphique : Biorender). IL-1β, interleukine-1β; Protéine 3 contenant les domaines NLRP3, NOD, LRR et pyrine.
Neuropathologie du COVID-19
Environ 30 à 40 % des patients souffrent d’anxiété et de dépression cliniquement significatives à la suite d’une infection au COVID-19, ce qui correspond à des infections graves antérieures à coronavirus. La probabilité d’une nouvelle maladie psychiatrique, telle que l’anxiété et les troubles de l’humeur, dans les 90 jours suivant le diagnostic de COVID-19 était de 5,8 % dans une analyse portant sur 62 354 patients.
Les résultats de l’autopsie montrent que le COVID-19 produit plusieurs types de lésions pathologiques pouvant contribuer aux manifestations neurologiques chez les patients atteints du COVID-19. Des affections parainfectieuses, telles que des maladies auto-immunes postvirales, ont été décrites en association avec divers virus, notamment les coronavirus. Les processus neuropathologiques parainfectieux surviennent généralement après une période de latence consécutive à une maladie infectieuse.
Un domaine en évolution rapide avec des preuves convergentes suggère que le COVID-19 peut induire une auto-immunité chez les personnes prédisposées.
Les recherches en cours sur les virus et l’auto-immunité permettront probablement de déterminer si les auto-anticorps affectent les cellules β pancréatiques. Il est important de noter que la dépression amplifie le handicap causé par des comorbidités telles que le diabète en exacerbant l’inactivité physique et la mauvaise observance des traitements co-prescrits. Cette interaction illustre ce qui se produit avec d’autres comorbidités médicales de la dépression. L’activité physique peut servir à inverser la spirale descendante en réduisant l’inflammation et en améliorant les symptômes de détresse et de résistance à l’insuline.
Modulation de la charge allostatique
Le concept d’ allostasie décrit la capacité d’un organisme à maintenir des systèmes homéostatiques essentiels à la vie face aux changements environnementaux et aux défis stressants en s’adaptant activement aux événements prévisibles et imprévisibles. La charge allostatique représente l’impact cumulatif de l’usure physiologique résultant d’une exposition chronique au stress et prédisposant les individus à la maladie. Les systèmes biologiques impliqués dans l’adaptation physiologique au changement et aux événements stressants comprennent l’axe hypothalamo-hypophyso-surrénalien (HPA), le système nerveux autonome et le système immunitaire.
Activation de l’axe HPA
L’axe HPA est activé en réponse à des facteurs de stress physiologiques ou psychologiques, induisant la libération de cortisol, une hormone glucocorticoïde, par la glande surrénale. La stimulation du système nerveux sympathique accompagne l’activation de l’axe HPA, entraînant une augmentation soudaine des cytokines, notamment les catécholamines et l’IL-6.
La libération de cortisol dépasse les niveaux habituels dans le but de coordonner une réponse temporaire de combat ou de fuite et de compenser une éventuelle exagération de la réponse immunitaire. La résolution de l’événement stressant met fin à la réponse via une boucle de rétroaction négative. La sécrétion de cortisol suit un schéma diurne qui aide à réguler le métabolisme du glucose et la réponse immunitaire.
Le stress chronique peut affecter le retour à la normale de ces systèmes hormonaux, entraînant une élévation du cortisol, des catécholamines et des marqueurs inflammatoires.
Stress psychologique, dépression et diabète de type 2
Le stress psychologique chronique survient lorsque les réponses aux exigences environnementales sont perçues comme dépassant la capacité d’adaptation d’un individu.
La dépression représente un état d’épuisement mental plus important que le stress psychologique chronique, qui est un facteur de risque et une composante de la dépression clinique . Le risque de diabète de type 2 augmente à mesure que la charge psychologique augmente progressivement. Bien que les preuves étayant une association entre le stress psychologique chronique général et le risque de diabète suggèrent une association positive, les résultats ne sont pas entièrement cohérents en raison de variations dans la conception et l’orientation des études.
Cependant, la dépression prédispose à l’apparition et à la progression du diabète de type 2. On estime qu’au moins 10 à 15 % des personnes atteintes de diabète de type 2 souffrent de dépression. De plus, la dépression est deux fois plus susceptible d’être présente chez les personnes atteintes de diabète de type 2 que chez celles sans diabète de type 2, et les personnes souffrant de dépression ont un risque 1,5 fois plus élevé de diabète de type 2.
L’exposition chronique à des niveaux élevés de cortisol affecte la structure et la fonction des récepteurs glucocorticoïdes et des régions cérébrales nécessaires au traitement des fonctions émotionnelles et cognitives. L’association biologique entre la dépression et le diabète de type 2 semble être liée à une hypercortisolémie dérégulée compatible avec un axe HPA hyperactif qui entraîne une adiposité viscérale et crée des déficits de sensibilité et de sécrétion d’insuline.
Le contrôle glycémique et les problèmes de santé associés, tels que la prise de poids, le respect des schémas thérapeutiques et les complications vasculaires, s’aggravent lorsque le diabète de type 2 s’accompagne de dépression. Le diabète de type 2 et les symptômes dépressifs se prédisposent, ce qui suggère un lien bidirectionnel.
Exercice en cas de COVID-19 post-aigu
L’exercice cible les séquelles neuropsychiatriques et endocriniennes du long COVID précipitées par une charge allostatique accrue résultant d’un stress psychologique chronique, d’une dérégulation du système immunitaire et de la stimulation d’un état hyperinflammatoire. La perturbation de l’allostasie, si elle n’est pas traitée, entraîne une dérégulation du glucose et le développement d’un diabète, ce qui peut faire pencher la balance vers une dépression clinique en raison de sa relation bidirectionnelle.
Lenze et coll. ont démontré que l’antidépresseur fluvoxamine, qui a une forte affinité pour le récepteur sigma-1, empêche la progression vers une maladie grave après une infection par le SRAS-CoV-2. Les récepteurs Sigma-1 jouent un rôle clé dans la réplication du virus, et le stress du réticulum endoplasmique (RE) qui en résulte peut favoriser la cascade inflammatoire grâce à son interaction avec la protéine sensible au stress du RE, l’enzyme 1 nécessitant de l’inositol. (IRE1) α. Les ligands du récepteur Sigma-1 atténuent la réponse inflammatoire.
Par conséquent, la fluvoxamine, qui est un puissant agoniste des récepteurs sigma-1, a été sélectionnée pour ses effets sur la régulation de la production de cytokines inflammatoires, et ses effets bénéfiques ont été démontrés dans un essai randomisé contrôlé par placebo mené auprès d’adultes en ambulatoire.
Comme la fluvoxamine, l’exercice a des effets antidépresseurs et immunomodulateurs qui le rendent immédiatement approprié pour une prévention sélective visant à ralentir la cascade d’événements résultant du stress psychologique chronique et conduisant à la dépression et au diabète de type 2. Il est important de noter que l’exercice augmente la sensibilité périphérique à l’insuline en cas d’intolérance au glucose et de diabète de type 2, mesurée par le test de clamp hyperinsulinémique-euglycémique de référence.
Chez les patients atteints de diabète de type 2 préexistant, une glycémie de 6,4 mmol·L−1 était associée à un risque réduit de mortalité toutes causes confondues et d’effets indésirables du COVID-19 par rapport à une glycémie de 10,9 mmol·L−1. Par conséquent, le maintien du contrôle glycémique semble être une recommandation judicieuse pour réduire la gravité de l’infection par le SRAS-CoV-2 et ses conséquences post-aiguës. En modulant le stress psychologique, l’inflammation prolongée et la sensibilité à l’insuline, l’exercice constitue une intervention plausible pour prévenir ou atténuer les effets endocriniens à long terme du COVID-19.
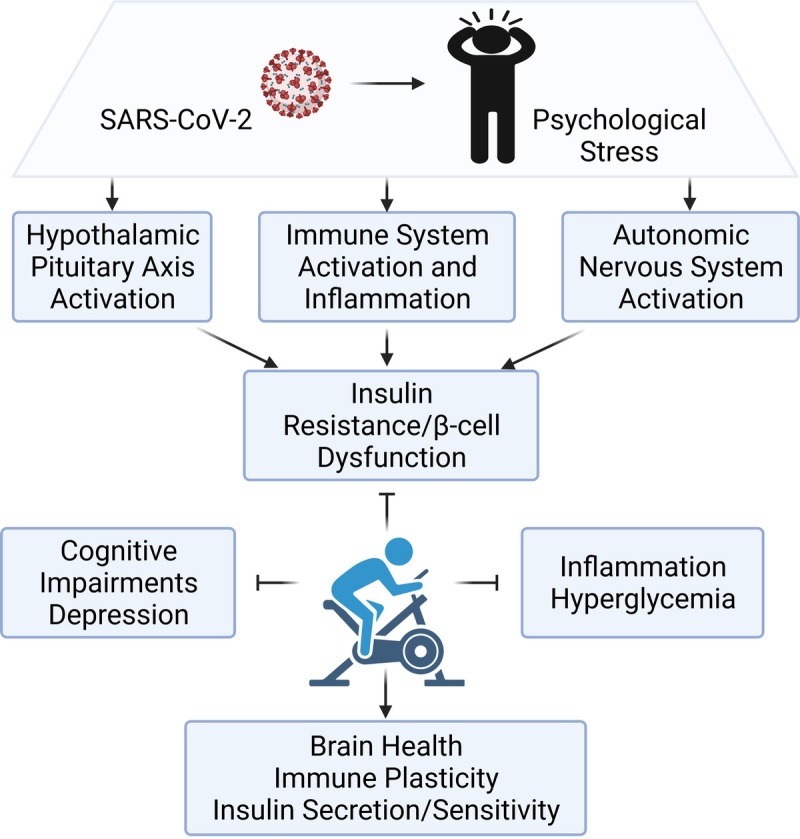
Dérégulation de l’adaptation physiologique aux changements et effets modulateurs de l’exercice. Le stress psychologique qui peut survenir avec le COVID-19 active l’axe hypothalamo-hypophyso-surrénalien (HPA), le système nerveux autonome et le système immunitaire. Un axe HPA dérégulé et hyperactif entraîne l’activation du système nerveux sympathique et une réponse immunitaire exagérée qui favorise la résistance à l’insuline et le dysfonctionnement des cellules β. L’exercice contribue à améliorer l’immunosurveillance et à réduire l’inflammation pour améliorer les résultats en matière de santé mentale et le contrôle glycémique (programme graphique : Biorender).
commentaires
Bien qu’il n’existe aucun traitement médicalement reconnu pour le Long COVID, l’exercice peut briser le cercle vicieux de l’inflammation qui peut conduire au développement du diabète et de la dépression des mois après qu’une personne se soit remise du virus.
"Nous savons qu’un long COVID provoque la dépression et nous savons qu’il peut augmenter la glycémie au point où les personnes développent une acidocétose diabétique, une maladie potentiellement mortelle courante chez les personnes atteintes de diabète de type 1", a déclaré Candida Rebello, Ph. .D. , chercheur scientifique au Pennington Biomedical Research Center. « L’exercice peut aider. "L’exercice neutralise l’inflammation qui conduit à une glycémie élevée ainsi qu’au développement et à la progression du diabète et de la dépression clinique."
On ne sait pas combien de personnes souffrent de Long COVID. Mais les estimations varient entre 15 et 80 pour cent des personnes infectées. Sur la base de ces chiffres, jusqu’à 1 million d’habitants de Louisiane pourraient souffrir du Long COVID.
Le long COVID provoque ce que les Centers for Disease Control décrivent comme « une constellation d’autres symptômes débilitants », notamment un brouillard cérébral, des douleurs musculaires et une fatigue qui peuvent durer des mois après qu’une personne se soit remise de l’infection initiale.
« Par exemple, une personne peut ne pas tomber gravement malade à cause du COVID-19, mais six mois plus tard, longtemps après la disparition de la toux ou de la fièvre, elle développe un diabète », a déclaré le Dr Rebello.
Une solution est l’exercice. Le Dr Rebello et ses co-auteurs décrivent son hypothèse dans « L’exercice en tant que modérateur des symptômes neuroendocriniens persistants du COVID-19 », publié dans la revue Exercise and Sport Sciences Reviews.
"Vous n’êtes pas obligé de courir un kilomètre ou même de marcher un kilomètre à un rythme rapide", a déclaré le Dr Rebello. « Marcher lentement, c’est aussi faire de l’exercice. Idéalement, vous devriez faire une séance d’exercices de 30 minutes. Mais si vous ne pouvez faire que 15 minutes à la fois, essayez de faire deux séances de 15 minutes. Si vous ne pouvez marcher que 15 minutes une fois par jour, faites-le. L’important est d’essayer. Peu importe par où vous commencez. Vous pouvez augmenter progressivement jusqu’au niveau d’exercice recommandé.
« Nous savons que l’activité physique est un élément clé d’une vie saine. "Cette recherche montre que l’exercice peut être utilisé pour briser la réaction en chaîne de l’inflammation qui conduit à des taux de sucre dans le sang élevés, puis au développement ou à la progression du diabète de type 2", a déclaré John Kirwan, Ph.D., PDG de Pennington Biomedical, qui est également un co-auteur de l’article.
Conclusions Le risque d’infection grave par le SRAS-CoV-2 et de mortalité est parmi les plus élevés chez les patients atteints de diabète de type 2 préexistant. La modulation de la charge allostatique résultant du COVID-19, comme le démontrent les séquelles neuropsychiatriques, est impliquée dans la pathogenèse du diabète de type 2, tandis que l’acidocétose diabétique est le résultat d’une glycémie incontrôlée. L’exercice module les principales caractéristiques persistantes d’une infection par le SRAS-CoV-2 qui favorisent l’augmentation des concentrations de glucose dans le sang, notamment l’inflammation et le stress. En modulant les concentrations de glucose dans le sang, l’exercice peut être utilisé pour briser le cercle vicieux de l’inflammation des cellules β conduisant à l’hyperglycémie et ainsi prévenir le développement ou la progression du diabète de type 2. |