Menschliche neuronale Larve migrans, verursacht durch Ascarid Ophidascaris robertsi
Die zentralen Thesen
Zusammenfassung Wir beschreiben einen Fall einer menschlichen Neurallarve migrans in Australien , die durch den Spulwurm Ophidascaris robertsi verursacht wurde und dessen endgültige Wirte australische Teppichpythons sind. Wir stellten die Diagnose, nachdem ein lebender Fadenwurm aus dem Gehirn einer 64-jährigen Frau entfernt worden war, die aufgrund eines 12 Monate zuvor diagnostizierten hypereosinophilen Syndroms immungeschwächt war. |
Ophidascaris- Arten sind Nematoden, die einen indirekten Lebenszyklus aufweisen; Mehrere Gattungen von Alt- und Neuweltschlangen sind Endwirte. O. robertsi-Nematoden sind in Australien beheimatet, wo die endgültigen Wirte Teppichpythons (Morelia spilota) sind. Erwachsene Nematoden leben in der Speiseröhre und im Magen der Python und geben ihre Eier mit dem Kot ab. Die Eier werden von verschiedenen Kleinsäugern aufgenommen, in denen sich die Larven ansiedeln, die als Zwischenwirte dienen . Die Larven wandern in die Brust- und Bauchorgane, wo insbesondere bei Beuteltieren die Larven im dritten Larvenstadium selbst bei kleinen Wirten eine beträchtliche Länge (7–8 cm) erreichen können. Der Lebenszyklus endet, wenn die Pythons die infizierten Zwischenwirte konsumieren. Menschen, die mit O. robertsi-Larven infiziert sind, gelten als zufällige Wirte , obwohl bisher keine Infektionen des Menschen mit einer Ophidascaris-Art gemeldet wurden . Wir präsentieren einen Fall einer menschlichen neuralen Larve migrans, die durch eine Infektion mit O. robertsi verursacht wurde.
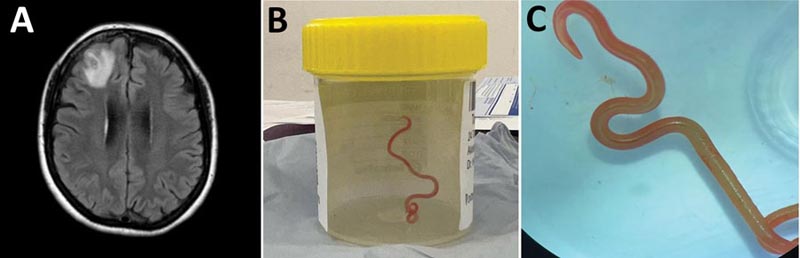
Abbildung : Menschliche neuronale Larve migrans, verursacht durch Ascarid Ophidascaris robertsi. Nachweis einer Nematodeninfektion mit Ophidascaris robertsi bei einer 64-jährigen Frau aus dem Südosten von New South Wales, Australien. A) Die Magnetresonanztomographie des Gehirns des Patienten mit abgeschwächter Inversionswiederherstellung zeigt eine verstärkende Läsion im rechten Frontallappen, 13 × 10 mm. B) Lebende Larvenform im dritten Stadium von Ophidascaris robertsi (80 mm lang, 1 mm Durchmesser), entnommen aus dem rechten Frontallappen des Patienten. C) Lebende Larvenform im dritten Stadium von O. robertsi (80 mm lang, 1 mm Durchmesser) unter einem Stereomikroskop (ursprüngliche Vergrößerung ×10). (CDC-Quelle)
Die klinische Fallstudie
Eine 64-jährige Frau aus dem Südosten von New South Wales, Australien, wurde Ende Januar 2021 nach dreiwöchigen Bauchschmerzen und Durchfall, gefolgt von trockenem Husten und Nachtschweiß, in ein örtliches Krankenhaus eingeliefert. Er hatte eine Eosinophilenzahl im peripheren Blut (PBEC) von 9,8 × 10 9 Zellen/L (Referenzbereich <0,5 × 10 9 Zellen/L), Hämoglobin 99 g/L (Referenzbereich 115–165 g/L), Blutplättchen 617 × 10 9 Zellen/L (Referenzbereich 150–400 × 10 9 Zellen/L) und C-reaktives Protein (CRP) 102 mg/L (Referenzbereich <5 mg/L). Ihre Krankengeschichte umfasste Diabetes mellitus, Hypothyreose und Depressionen . Sie wurde in England geboren und war vor 20 bis 30 Jahren nach Südafrika, Asien und Europa gereist. Sie wurde wegen einer ambulant erworbenen Lungenentzündung mit Doxycyclin behandelt und hatte sich noch nicht vollständig erholt.
Eine Computertomographie (CT) ergab multifokale Lungentrübungen mit umgebenden Milchglasveränderungen sowie Leber- und Milzläsionen. Bei der bronchoalveolären Spülung wurden 30 % Eosinophile ohne Anzeichen von Malignität oder pathogenen Mikroorganismen, einschließlich Helminthen, festgestellt. Serologische Tests waren negativ für Strongyloides. Die Ergebnisse des Screenings auf Autoimmunerkrankungen waren negativ. Die Diagnose des Patienten lautete eosinophile Pneumonie unklarer Ätiologie; Er begann mit der Einnahme von Prednisolon (25 mg/Tag) mit teilweiser Besserung der Symptome.
Drei Wochen später wurde er mit wiederkehrendem Fieber und anhaltendem Husten während der Einnahme von Prednisolon in ein tertiäres Krankenhaus eingeliefert. Die Lungen- und Leberläsionen waren in der Positiv-Emissions-Tomographie 18F-Fluordesoxyglucose-avid. Die Lungenbiopsieprobe war mit einer eosinophilen Pneumonie kompatibel , jedoch nicht mit einer eosinophilen Granulomatose mit Polyangiitis (EGPA). Kulturen von Bakterien, Pilzen und Mykobakterien waren negativ . Es wurden Echinococcus-, Fasciola- und Schistosoman-Antikörper nachgewiesen; Konzentrierte und fixierte Färbetechniken zeigten keine Parasiten in Stuhlproben.
Wir entdeckten eine Genumlagerung des monoklonalen T-Zell-Rezeptors, was auf ein T-Zell-gesteuertes hypereosinophiles Syndrom (HES) schließen lässt. Weitere hämatologische und Vaskulitis-Untersuchungen waren unauffällig. Die Behandlung wurde mit Prednisolon (50 mg/Tag) und Mycophenolat (1 g 2×/Tag) begonnen. Aufgrund seiner Reisegeschichte, der Möglichkeit einer falsch negativen Strongyloides-Serologie und einer erhöhten Immunsuppression erhielt er an zwei aufeinanderfolgenden Tagen Ivermectin (200 µg/kg oral) und nach 14 Tagen eine Wiederholungsdosis.
Ein Mitte 2021 durchgeführter CT-Scan zeigte eine Verbesserung der Lungen- und Leberläsionen, die Milzläsionen veränderten sich jedoch nicht. Im Januar 2022 haben wir Mepolizumab (monoklonaler Interleukin-5-Antikörper, 300 mg alle 4 Wochen) hinzugefügt, da wir die Prednisolon-Dosis nicht unter 20 mg täglich senken konnten, ohne dass Atemwegssymptome auftraten. Als die PBEC wieder in den Normalbereich zurückkehrte, reduzierten wir schrittweise die Prednisolon-Dosis.
Über einen Zeitraum von drei Monaten im Jahr 2022 litt der Patient unter Vergesslichkeit und einer sich verschlimmernden Depression , während er Prednisolon (7,5 mg/Tag) sowie Mycophenolat und Mepolizumab in den gleichen Dosen einnahm. Der CRP betrug 6,4 mg/L. Das Gehirn-MRT zeigte eine Läsion des rechten Frontallappens mit einer peripheren Verstärkung von 13 × 10 mm. Im Juni 2022 wurde eine offene Biopsie durchgeführt. Wir bemerkten eine fadenförmige Struktur innerhalb der Läsion, die wir entfernten; war ein lebender, beweglicher Helminth (80 mm lang, 1 mm Durchmesser). Es wurden eine umlaufende Durotomie und Kortikotomie durchgeführt und es wurden keine anderen Helminthen gefunden. Die histopathologische Untersuchung des Duralgewebes ergab eine gutartig organisierte entzündliche Höhle mit ausgeprägter Eosinophilie.
Wir haben den Helminth vorläufig als Larve im dritten Larvenstadium von Ophidascaris robertsi identifiziert , und zwar aufgrund seiner charakteristischen roten Farbe, drei aktiven ascaridoidartigen Lippen, dem Vorhandensein eines Blinddarms und dem Fehlen eines voll entwickelten Fortpflanzungssystems im Kontext dessen, was bekannt ist .
Eine fortschreitende CT-Untersuchung ergab eine Auflösung der Lungen- und Leberläsionen, jedoch unveränderte Milzläsionen. Der Patient erhielt 2 Tage lang Ivermectin (200 µg/kg/Tag) und 4 Wochen lang Albendazol (400 mg 2×/Tag). Ihm wurde 10 Wochen lang eine Behandlung mit Dexamethason (beginnend mit 4 mg zweimal täglich) verabreicht, während alle anderen Immunsuppressiva abgesetzt wurden. Sechs Monate nach der Operation (drei Monate nach Absetzen von Dexamethason) blieb der PBEC des Patienten normal. Die neuropsychiatrischen Symptome hatten sich verbessert, blieben jedoch bestehen.
Schlussfolgerungen
In diesem Fall wohnte der Patient in der Nähe eines von Teppichpythons bewohnten Bereichs eines Sees . Obwohl er keinen direkten Kontakt mit Schlangen hatte, sammelte er häufig einheimische Vegetation, Warrigalblätter ( Tetragonia tetragonioides ), rund um den See, um sie zum Kochen zu verwenden. Unsere Hypothese ist, dass er versehentlich O. robertsi-Eier verzehrt hat, entweder direkt aus der Vegetation oder indirekt durch Kontamination durch seine Hände oder Küchengeräte.
Der klinische und radiologische Verlauf des Patienten deutet auf einen dynamischen Prozess der Larvenmigration in mehrere Organe hin, begleitet von Eosinophilie im Blut und Gewebe, was auf ein viszerales Larva-migrans-Syndrom hinweist. Wir vermuten, dass es sich bei den Milzläsionen um eine separate Pathologie handelt, da sie stabil blieben und im Gegensatz zu den Lungen- und Leberläsionen nicht PET-affin waren.
Dieser Fall verdeutlicht die Schwierigkeit, eine geeignete Probe für die Parasitendiagnose zu erhalten, und die schwierigen Managemententscheidungen hinsichtlich der Immunsuppression bei lebensbedrohlichem HES. Obwohl eine viszerale Beteiligung bei tierischen Wirten häufig vorkommt, wurde bisher nicht über eine Invasion des Gehirns durch Ophidascaris -Larven berichtet. Die Immunsuppression des Patienten könnte es den Larven ermöglicht haben, in das Zentralnervensystem (ZNS) zu wandern. Das Wachstum der Larve im dritten Larvenstadium im menschlichen Wirt ist bemerkenswert, da frühere experimentelle Studien keine Larvenentwicklung bei domestizierten Tieren wie Schafen, Hunden und Katzen gezeigt haben und ein eingeschränkteres Larvenwachstum bei Vögeln und nicht heimischen Tieren gezeigt haben Säugetiere. . als bei einheimischen Säugetieren.
Nachdem wir die Larve aus ihrem Gehirn entfernt hatten, erhielt die Patientin Anthelminthika und Dexamethason, um mögliche Larven in anderen Organen zu bekämpfen. Es ist bekannt, dass Ophidascaris-Larven lange Zeit in tierischen Wirten überleben; Beispielsweise sind Laborratten seit mehr als vier Jahren mit Larven im dritten Stadium infiziert. Die Begründung für Ivermectin und Albendazol basierte auf Daten aus der Behandlung von Nematodeninfektionen bei Schlangen und Menschen. Albendazol hat eine bessere ZNS-Penetration als Ivermectin. Dexamethason wurde bei anderen menschlichen Nematoden- und Bandwurminfektionen eingesetzt, um schädliche Entzündungsreaktionen des ZNS nach der Behandlung zu verhindern.
Zusammenfassend verdeutlicht dieser Fall das anhaltende Risiko zoonotischer Erkrankungen bei enger Interaktion von Mensch und Tier. Obwohl O. robertsi-Nematoden in Australien endemisch sind, infizieren andere Ophidascaris-Arten Schlangen anderswo, was darauf hindeutet, dass weltweit weitere Fälle beim Menschen auftreten könnten.
Dr. Hossain ist ein Arzt für Infektionskrankheiten in Australien. Sein Forschungsschwerpunkt ist die Parasitologie.
Kommentare
Im weltweit ersten bekannten Fall einer menschlichen Infektion mit einem Parasiten, der bei manchen Pythons häufig vorkommt, entfernten Ärzte einen sich windenden Spulwurm aus dem Gehirn einer Australierin. Es wird angenommen, dass die Frau, bei der sich die Symptome seit mindestens einem Jahr verschlimmerten, sich die Infektion zugezogen hatte, als sie dort Gras suchte und aß, wo eine Schlange ihren Stuhlgang gemacht hatte.
„Dies ist weltweit der erste beschriebene Fall von Ophidascaris beim Menschen “, sagte Dr. Sanjaya Senanayake, ein führender Experte für Infektionskrankheiten an der Australian National University und dem Canberra Hospital, in einer Pressemitteilung der Universität. „Unseres Wissens ist dies auch der erste Fall, an dem das Gehirn einer Säugetierart beteiligt ist, egal ob menschlich oder nicht.“
Es wird vermutet, dass sich in Lunge und Leber der 64-jährigen Frau auch Larven des Spulwurms Ophidascaris robertsi befanden . Ihre Symptome begannen im Januar 2021 mit Bauchschmerzen und Durchfall, gefolgt von Fieber, Husten und Atembeschwerden.
„Rückblickend waren diese Symptome wahrscheinlich auf die Migration von Spulwurmlarven aus dem Darm in andere Organe wie Leber und Lunge zurückzuführen. Es wurden Atemwegsproben und eine Lungenbiopsie durchgeführt; in diesen Proben wurden jedoch keine Parasiten identifiziert“, sagte er Karina Kennedy, Direktorin der klinischen Mikrobiologie am Canberra Hospital.
„Zu dieser Zeit war der Versuch, mikroskopisch kleine Larven zu identifizieren, von denen noch nie zuvor festgestellt wurde, dass sie Infektionen beim Menschen verursachen, wie der Versuch, die Nadel im Heuhaufen zu finden“, sagte er in der Erklärung.
Als die Symptome der Frau fortschritten und leichte Veränderungen im Gedächtnis und in der Gedankenverarbeitung einhergingen, unterzog sie sich einer Gehirn-MRT , bei der eine ungewöhnliche Läsion im Frontallappen ihres Gehirns festgestellt wurde.
Bei einer Gehirnoperation fanden Ärzte den 3,15 Zoll großen Spulwurm. Nachdem die Ärzte den noch lebenden und sich windenden Parasitenexperten entfernt hatten, identifizierten ihn Parasitenexperten anhand seines Aussehens. Molekulare Studien bestätigten ihre Identifizierung.
Die Ärzte sagten, die Frau habe sich die Infektion wahrscheinlich durch die Nahrungssuche und den Verzehr spinatähnlicher Warrigal-Blätter an einem See zugezogen, wo ein Teppichpython den Parasiten über seinen Kot ausgeschieden hatte.
Typischerweise kommen Spulwurmlarven bei kleinen Säugetieren und Beuteltieren vor, die von Teppichpythons gefressen werden, Schlangen, deren Markierungen den Mustern asiatischer Teppiche ähneln. Dadurch kann der Lebenszyklus in der Schlange abgeschlossen werden.
„In den letzten 30 Jahren gab es weltweit etwa 30 Neuinfektionen“, sagte Senanayake. „Von den neu auftretenden Infektionen weltweit sind etwa 75 % zoonotisch, d. h. es kam zu einer Übertragung von der Tierwelt auf die Menschenwelt. Dazu gehören auch Coronaviren.“ Allerdings werde die Ophidascaris- Infektion nicht von Mensch zu Mensch übertragen und werde daher keine Pandemie wie COVID-19 oder Ebola auslösen, sagte Senanayake. Er fügte jedoch hinzu, dass sowohl der Teppichpython als auch der Parasit in anderen Teilen der Welt vorkommen, sodass es in Zukunft wahrscheinlich zu Fällen kommen werde.
Ophidascaris robertsi kommt unter Teppichpythons häufig vor, sagte Senanayake. Der Parasit lebt normalerweise in der Speiseröhre und im Magen der Schlange und seine Eier werden mit dem Kot der Python ausgeschieden. „Spulwürmer sind unglaublich widerstandsfähig und können in einer Vielzahl von Umgebungen gedeihen“, sagte Senanayake. „Beim Menschen können sie Magenschmerzen, Erbrechen, Durchfall, Appetit- und Gewichtsverlust, Fieber und Müdigkeit verursachen.“
Sicherheit sei besonders wichtig bei der Nahrungssuche an Orten, an denen Wildtiere leben, betonten Experten.
„Menschen, die im Garten arbeiten oder Futter sammeln, sollten ihre Hände waschen, nachdem sie im Garten gearbeitet und die geernteten Produkte berührt haben“, sagte Kennedy. „Alle Lebensmittel, die für Salate oder zum Kochen verwendet werden, sollten ebenfalls gründlich gewaschen und Küchenoberflächen und Schneidebretter nach Gebrauch getrocknet und gereinigt werden.“
Spezialisten für Infektions- und Hirnerkrankungen überwachen den Patienten weiterhin. „Es ist nie einfach oder wünschenswert, für irgendetwas der erste Patient auf der Welt zu sein“, sagte Senanayake. „Ich kann unserer Bewunderung für diese Frau, die in diesem Prozess Geduld und Mut gezeigt hat, gar nicht genug Ausdruck verleihen.“
Die Ergebnisse der Forscher wurden in der Septemberausgabe der Zeitschrift Emerging Infectious Diseases des US-amerikanischen Centers for Disease Control and Prevention veröffentlicht.
Was das für die Bevölkerung bedeutet Waschen Sie gepflücktes oder angebautes Gemüse gründlich, insbesondere wenn es aus Wildgebieten stammt, und waschen Sie unbedingt auch Ihre Hände. |
















