Zusammenfassung Mit zunehmendem Alter unserer Bevölkerung treten altersbedingte Pathologien immer häufiger auf. Eine Verschlechterung der Skelettmuskulatur und des Immunsystems äußert sich in Sarkopenie bzw. Immunseneszenz. Die Krankheitslast dieser Pathologien unterstreicht die Notwendigkeit eines besseren Verständnisses der zugrunde liegenden Mechanismen. Die Skelettmuskulatur ist zu einem starken Regulator der Funktion des Immunsystems geworden. Daher könnte die Skelettmuskulatur der zentrale Integrator zwischen Sarkopenie und Immunseneszenz in einem alternden biologischen System sein. Therapieansätze, die auf die Skelettmuskulatur abzielen, könnten die Funktion sowohl des Muskels als auch des Immunsystems wiederherstellen. In diesem Aufsatz beschreiben wir daher das aktuelle, wenn auch noch bruchstückhafte Wissen über die möglichen Kommunikationswege des Muskels und des Immunsystems. wie sie von alternder Skelettmuskulatur betroffen sind und diskutieren mögliche Behandlungsstrategien. Die Übersicht dient der Hypothesengenerierung und soll daher weitere Forschungen auf diesem wichtigen wissenschaftlichen Gebiet anregen. |
Skelettmuskel als potenzieller zentraler Zusammenhang zwischen Sarkopenie und Immunseneszenz
Einführung
Unter biologischem Alter versteht man den Verlust der physiologischen Integrität. Fast jedes Organ im menschlichen Körper ist von den schädlichen Auswirkungen des Alterns betroffen. Skelettmuskeln sind keine Ausnahme. Muskelmasse und -funktion nehmen mit zunehmendem Alter ab. Dieser altersabhängige Verlust der Muskelqualität und -quantität definiert laut der Europäischen Arbeitsgruppe für Sarkopenie bei älteren Menschen den sarkopenischen Phänotyp .
Seit 2018 gilt Sarkopenie als Muskelerkrankung und die Muskelkraft ist der Muskelmasse überlegen, wenn es darum geht, unerwünschte Folgen vorherzusagen. Daher gilt die Muskelkraft als der Hauptparameter, der die Sarkopenie definiert.
Die Bedeutung einer klinischen Definition zur Identifizierung von Sarkopeniepatienten wird durch eine zunehmend alternde Bevölkerung deutlich. Derzeit gelten etwa 10 % der älteren Patienten als sarkopenisch. Es wird erwartet, dass diese Zahl dramatisch ansteigt. In Europa wird bis 2045 mit einem Anstieg der Zahl der Sarkopenie-Patienten um 72 % gerechnet, der die Lebensqualität stark beeinträchtigen wird.
Ein genaues Verständnis der zugrunde liegenden Mechanismen, die zur Sarkopenie führen, und ihrer klinischen Folgen fehlt jedoch noch. Immunschwäche und chronische Entzündungen wurden in der vielschichtigen Pathogenese der Sarkopenie diskutiert. Es wurde angenommen, dass die Interaktion zwischen dem Immunsystem und dem Muskelkompartiment einseitig ist.
Es wurde gezeigt, dass die Skelettmuskulatur Immunprozesse und die Entzündungsreaktion reguliert.
Was die Immunfunktion betrifft, so wird der Begriff „ Immunseneszenz“ üblicherweise verwendet, um den altersabhängigen Rückgang des Immunsystems zusammenzufassen, auch wenn es keine eindeutige Definition gibt. Hauptmerkmale der Immunseneszenz sind Thymusatrophie, Akkumulation seneszenter T-Zellen, beeinträchtigte Funktion angeborener Immunzellen wie NK-Zellen, Makrophagen und Neutrophilen sowie fehlerhafte Aufrechterhaltung und funktionelle Reaktion von Lymphozyten
Es wurden auch altersabhängige Veränderungen der Immunfunktion der Skelettmuskulatur beobachtet. Daher könnten Sarkopenie und Immunseneszenz über die Skelettmuskulatur miteinander verbunden sein bzw. interagieren. Die mögliche zentrale Rolle der Skelettmuskulatur bei der Regulierung ihrer eigenen Funktion und des Immunsystems während des Alterns wird diskutiert.
Die Belastung durch Sarkopenie: ein Risikofaktor für Infektionen
Kürzlich wurden mehrere unerwünschte Folgen der Sarkopenie festgestellt. Dazu gehören unter anderem ein erhöhtes Sturzrisiko, das zu Brüchen, Behinderungen und Funktionseinschränkungen, Dysphagie, geringerer Lebensqualität und Gesamtmortalität führt.
Sarkopenie ist ein Hinweis auf das Infektionsrisiko nach einer Operation. Darüber hinaus zeigten Patienten mit diagnostizierter Sarkopenie nach dreiwöchigem Krankenhausaufenthalt ein zweifach erhöhtes Risiko, nosokomiale Infektionen zu entwickeln. Der Einfluss der Sarkopenie auf das Infektionsrisiko bei in Wohngemeinschaften lebenden Patienten ist weniger klar, da das Fehlen epidemiologischer Studien eine schlüssige Aussage unmöglich macht. Allerdings ist die Sarkopenie sowohl ein Hinweis auf das Risiko einer ambulant erworbenen Lungenentzündung bei älteren Menschen als auch auf die 90-Tage-Mortalität bei Patienten mit Aspirationspneumonie.
Obwohl die oben beschriebenen Studien keinen Kausalzusammenhang belegen, deuten sie auf einen Zusammenhang zwischen veränderter Muskelfunktion und einer veränderten Immunantwort auf Krankheitserreger hin. Angesichts der hohen Inzidenz von Sarkopenie und des erhöhten Infektionsrisikos bei älteren Patienten sind die Auswirkungen tiefgreifend, da Sarkopenie sowohl ein klinischer Prädiktor für gefährdete Patienten als auch ein mögliches therapeutisches Ziel zur Verbesserung der mit Infektionen verbundenen Morbidität bei älteren Patienten darstellen könnte.
Skelettmuskel als potenzieller zentraler Regulator der Funktion des Immunsystems
In den letzten zwei Jahrzehnten hat sich die Wahrnehmung der Skelettmuskulatur als reine Bewegungseinheit verändert. Muskeln werden zunehmend als Organ mit immunregulatorischen Eigenschaften anerkannt. Daher modulieren Skelettmuskelzellen die Immunfunktion, indem sie Signale über verschiedene lösliche Faktoren, Zelloberflächenmoleküle oder Zell-Zell-Interaktionen senden. Obwohl unser Wissen über die Interaktion zwischen Muskel und Immunsystem erheblich fortgeschritten ist, ist der Einfluss des Alters relativ unbekannt.
Sarkopenie kann diese Wechselwirkung erheblich stören und eine mögliche Erklärung für die klinischen Ergebnisse liefern, die bei Patienten mit Sarkopenie beobachtet werden.
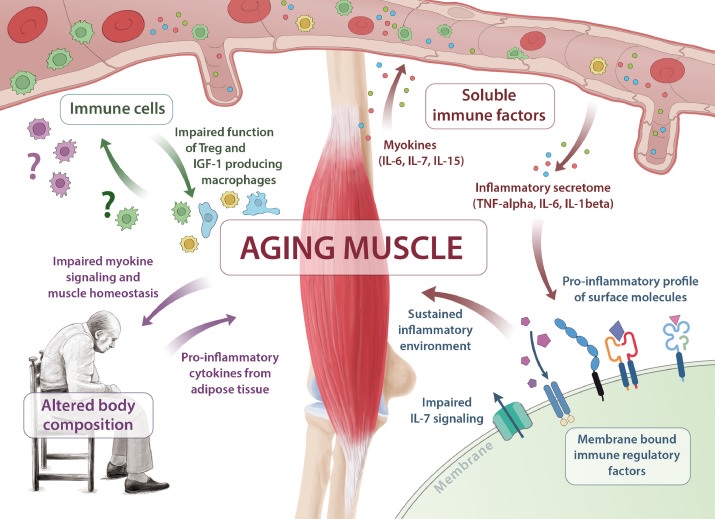 Die Alterung der Skelettmuskulatur ist für die Pathogenese von Immunseneszenz und Sarkopenie von wesentlicher Bedeutung. Mehrere Signalwege sind betroffen, darunter eine unzureichende Myokinsignalisierung (IL-6, IL-7, IL-15), eine Verschiebung membrangebundener immunregulatorischer Faktoren hin zu einem entzündungsfördernden Profil, eine veränderte Funktion der Immunzellen und eine veränderte Körperzusammensetzung .
Die Alterung der Skelettmuskulatur ist für die Pathogenese von Immunseneszenz und Sarkopenie von wesentlicher Bedeutung. Mehrere Signalwege sind betroffen, darunter eine unzureichende Myokinsignalisierung (IL-6, IL-7, IL-15), eine Verschiebung membrangebundener immunregulatorischer Faktoren hin zu einem entzündungsfördernden Profil, eine veränderte Funktion der Immunzellen und eine veränderte Körperzusammensetzung .
Sarkopenie und Immunoseneszenz: eine bidirektionale Verbindung
Skelettmuskeln weisen immunregulierende Eigenschaften auf und chronische, geringfügige Entzündungen können zum Verlust von Muskelmasse führen. Das Konzept der Skelettmuskulatur als Regulator der Immunfunktion ist relativ neu und verleiht der Verbindung zwischen Muskel und Immunsystem eine neue Komplexitätsebene.
Folglich könnte die Verbindung zwischen Muskel und Immunsystem bidirektional sein : Eine chronische, geringgradige Entzündung induziert Muskelkatabolismus durch pleiotrope Mechanismen, die durch das Entzündungssekretom vermittelt werden. Gleichzeitig ist die Homöostase der Skelettmuskulatur teilweise für eine gesunde Immunfunktion verantwortlich.
Bei einer Fehlregulierung können jedoch eine unzureichende Myokinsignalisierung, eine Veränderung membrangebundener Faktoren hin zu einem entzündungsfördernden Profil und eine beeinträchtigte Regenerationsfähigkeit von Immunzellen zu einer Störung der Funktion des Immunsystems führen.
Wir schlagen vor, dass die biologische Alterung das Gleichgewicht der Homöostase des Muskelimmunsystems verändern kann, wobei die Skelettmuskulatur als potenzielle zentrale Verbindung zwischen Sarkopenie und Immunseneszenz fungiert. Eine gesunde Muskelfunktion geht in einem alternden biologischen System aufgrund von körperlicher Inaktivität, Stoffwechselveränderungen und der Anhäufung chronischer, geringgradiger Entzündungen allmählich verloren.
Eine beeinträchtigte Muskelfunktion wiederum schränkt die Signalübertragung der Skelettmuskelzellen ein, die für die Regulierung und Aufrechterhaltung des Immunsystems notwendig ist, und führt zu einem Teufelskreis, in dem sich Immunsystem und Muskelfunktionsstörungen gegenseitig unterstützen.
Patienten mit Sarkopenie haben ein erhöhtes Infektionsrisiko, was auf ein klinisches Korrelat einer veränderten Immunfunktion schließen lässt.
Der Einfluss von Sarkopenie auf die Immunfunktion im Hinblick auf Autoimmunerkrankungen und Krebs ist weniger klar. Die Häufigkeit von Krebs und Autoimmunerkrankungen nimmt mit zunehmendem Alter zu, während die Muskelmasse im Durchschnitt abnimmt. Obwohl dies naheliegend ist, kann eine Kausalität nicht abgeleitet werden. Es sind Längsschnittstudien erforderlich, die den Einfluss der Sarkopenie auf die Inzidenz von Krebs und Autoimmunerkrankungen untersuchen.
Abschluss Die Skelettmuskulatur reguliert die Funktionen des Immunsystems durch Myokinsignale und die Expression immunmodulatorischer Oberflächenmoleküle. Immunzellen wiederum haben entscheidenden Einfluss auf Muskelmasse und -funktion. Daher kann die Skelettmuskulatur als zentraler Integrator zwischen Sarkopenie und Immunseneszenz fungieren. Angesichts ihrer individuellen und sozioökonomischen Belastung sind innovative Therapieansätze dringend erforderlich und könnten, wenn sie auf die Skelettmuskulatur abzielen, sowohl die Skelettmuskulatur als auch die Funktion des Immunsystems bei alternden Menschen wiederherstellen. |















