Les manifestations extrapulmonaires du coronavirus 2 (SARS-CoV-2) du syndrome respiratoire aigu sévère sont désormais largement reconnues et ont des implications cliniques importantes. À notre connaissance, l’association du SARS-CoV-2 avec les muscles respiratoires n’a pas été étudiée. Ceci est surprenant, puisque les muscles respiratoires pilotent la ventilation alvéolaire et que leur faiblesse provoque une insuffisance respiratoire aiguë.
Chez les patients gravement malades sous ventilation, la faiblesse des muscles respiratoires prolonge la ventilation mécanique et augmente la mortalité.
L’ objectif de cette étude était d’étudier l’association de la maladie grave à coronavirus 2019 (COVID-19) avec les muscles respiratoires chez les patients gravement malades et de comparer les résultats avec ceux obtenus chez des patients gravement malades non-COVID-19.
Méthodes
Notre étude s’est concentrée sur le diaphragme , principal muscle respiratoire. Des échantillons consécutifs de muscle du diaphragme ont été collectés lors de l’autopsie des cadavres de 26 patients gravement malades du COVID-19 dans 3 centres médicaux universitaires aux Pays-Bas (connus sous le nom de COVID-19 - unité de soins intensifs [USI]). en avril et mai 2020.
En tant que groupe témoin , des échantillons de diaphragme d’autopsie ont été prélevés sur les cadavres de 8 patients gravement malades sans COVID-19 (appelés USI témoin).
Des échantillons du diaphragme médico-costal gauche ont été utilisés pour les analyses.
Cette étude a été approuvée par le comité d’éthique médicale de l’UMC d’Amsterdam et le consentement éclairé écrit a été fourni par le plus proche parent du défunt. Les données ont été analysées avec SPSS, version 22 (IBM) et visualisées avec GraphPad Prism, version 7.0 (GraphPad). La signification statistique a été fixée à p <0,05.
Résultats
L’âge médian des patients atteints de COVID-19 en soins intensifs était de 71 ans (intervalle interquartile : 61-74 ans) et 21 (81 %) étaient des hommes.
Vingt-quatre patients (92,3 %) ont reçu une ventilation mécanique invasive pendant une durée médiane de 12 jours (intervalle interquartile : 6 à 25 jours). Le nombre de jours de ventilation mécanique invasive et la durée du séjour en soins intensifs étaient comparables entre les patients COVID-19 – soins intensifs et témoins – soins intensifs.
COVID-19 : les patients en soins intensifs avaient un indice de masse corporelle plus élevé (calculé comme le poids en kilogrammes divisé par la taille en mètres carrés) et étaient moins susceptibles d’être traités avec des stéroïdes.
Aucun patient des deux groupes n’avait de maladie neuromusculaire préexistante.
Nous rapportons l’enzyme de conversion de l’angiotensine 2 (ACE-2) dans le diaphragme des patients atteints de COVID-19 - ICU et contrôle - ICU. L’ACE-2 est principalement localisé dans la membrane des myofibres, fournissant un point d’entrée au SRAS-CoV-2 pour infecter les myofibres du diaphragme. Des preuves d’ARN viral du SRAS-CoV-2 ont été trouvées dans le diaphragme chez 4 patients (15,4 %).
D’autres analyses, pour lesquelles nous avons appliqué l’hybridation in situ de l’ARN , ont indiqué que l’ARN viral était localisé dans les myofibres du diaphragme. Les analyses de séquençage d’ARN ont montré que 315 gènes étaient régulés positivement et 281 régulés négativement dans le diaphragme des patients COVID-19 en soins intensifs par rapport aux patients témoins en soins intensifs.
Des analyses plus approfondies de tous les gènes régulés positivement et négativement ont révélé l’activation des voies de fibrose (signalisation du facteur de croissance des fibroblastes).
Conformément à ces résultats, la fibrose épimysiale et périmysiale était plus de 2 fois plus élevée dans les diaphragmes des patients atteints de COVID-19 en soins intensifs par rapport aux patients témoins en soins intensifs.
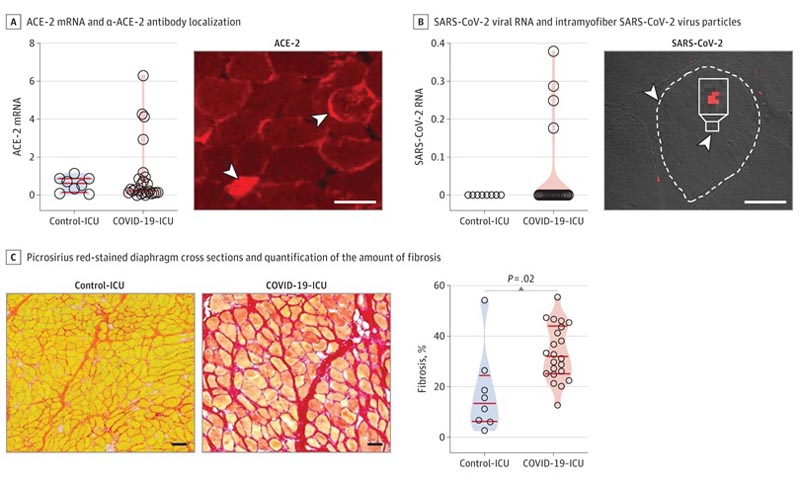
A, panneau de gauche : ARNm ACE-2 dans des échantillons de diaphragme déterminés par réaction en chaîne par polymérase quantitative (qPCR) et normalisés par rapport au gène domestique TBP. Panneau de droite : localisation de l’anticorps α-ACE-2 par microscopie à fluorescéine dans des coupes transversales du diaphragme ; les pointes de flèches montrent la localisation cytosolique et membranaire (barre = 50 μm). B, panneau de gauche : L’ARN viral du coronavirus 2 du syndrome respiratoire aigu sévère (SRAS-CoV-2), déterminé par qPCR et normalisé par rapport au gène de ménage TBP, est détecté dans le diaphragme du 4 coronavirus 2019 (COVID-19) - unité de soins intensifs (USI) patients (patients 7, 9, 33 et 36). Panneau de droite : l’hybridation in situ à l’aide de RNAscope chez le patient n° 7 montre des particules intramfibres du virus SARS-CoV-2 (points rouges, indiqués par des pointes de flèches) ; un bord de myofibre est mis en évidence par une ligne pointillée (barre = 30 μm). C, panneaux de gauche : images représentatives de coupes transversales du diaphragme colorées en rouge picrosirius pour mettre en évidence la fibrose ; les patients n°22 et 3 sont représentés (barre = 100 μm). Panneau de droite : quantification de l’ampleur de la fibrose.
Discussion
Dans cette étude, nous fournissons des preuves uniques de l’expression de l’ACE-2 dans le diaphragme humain et de l’infiltration virale du SRAS-CoV-2 dans le diaphragme d’un sous-ensemble de patients COVID-19 - USI.
Chez les patients atteints de COVID-19 - USI, nous rapportons une expression accrue de gènes impliqués dans la fibrose et des preuves histologiques du développement de la fibrose dans le diaphragme. Ce phénotype myopathique était clairement différent de celui des patients témoins en soins intensifs, avec une durée comparable de ventilation mécanique et de séjour en soins intensifs.
Il reste à établir si la myopathie diaphragmatique est un effet direct du SRAS-CoV-2. Seuls 3 patients du groupe témoin en soins intensifs (37,5 %) souffraient d’une maladie pulmonaire virale et l’association de la pneumonie virale avec les muscles du diaphragme est inconnue.
| Nous émettons l’hypothèse qu’une myopathie diaphragmatique sévère associée au COVID-19, telle que décrite dans cette étude, peut entraîner une faiblesse du diaphragme et pourrait contribuer à l’échec du sevrage du ventilateur, à une dyspnée persistante et à la fatigue chez les patients atteints de COVID-19 qui survivent à leur séjour en soins intensifs. . |