Résumé Nous suggérons l’utilisation de MicroCLOTS (syndrome thromboinflammatoire obstructif pulmonaire microvasculaire COVID-19) comme nouveau nom pour la maladie pulmonaire grave à coronavirus 2019 (COVID-19). Nous émettons l’hypothèse que, chez les individus prédisposés, les lésions virales alvéolaires sont suivies d’une réaction inflammatoire et d’une thrombose pulmonaire microvasculaire. Ce syndrome thrombo-inflammatoire endothélial progressif peut également impliquer le lit microvasculaire du cerveau et d’autres organes vitaux, entraînant une défaillance multiviscérale et la mort. Les étapes futures de la compréhension de la maladie et de l’identification des traitements pourraient bénéficier de cette définition et de cette séquence hypothétique d’événements. |
L’infection par le coronavirus 2 du syndrome respiratoire aigu sévère (SRAS-CoV-2) représente une urgence pandémique aux proportions dramatiques.1
L’évolution clinique de l’infection par le SRAS-CoV-2 répond souvent aux critères du syndrome de détresse respiratoire aiguë (SDRA), avec une gravité progressive conduisant finalement à une mort rapide.1-3
La physiopathologie du SDRA dans les cas graves d’infection par le SRAS-CoV-2 est attribuée à une réaction hyperimmune de l’hôte.3 Dès les premières descriptions, il semble que l’aggravation progressive de la fonction pulmonaire chez les patients infectés par le SRAS-CoV-2 soit potentiellement entraînée par la réponse immunitaire de l’hôte.
Le SRAS-CoV-2 pénètre dans les cellules cibles via le récepteur de l’enzyme de conversion de l’angiotensine 2 (ACE2) à la surface des cellules, qui est exprimé à la surface des cellules épithéliales pulmonaires et des entérocytes de l’intestin grêle.
Les récepteurs ACE2 sont également présents sur les cellules endothéliales artérielles et veineuses et sur les cellules musculaires lisses artérielles de plusieurs organes.5 Leur réplication provoque des dommages cellulaires directs et la libération d’alarmes pro-inflammatoires par les cellules mourantes.6
En plus de cet effet direct, les particules virales peuvent provoquer des réponses immunitaires innées de l’hôte par différents mécanismes, notamment l’activation des macrophages alvéolaires et la cascade du complément via la voie des lectine.
En outre, les complexes immuns formés localement peuvent jouer un rôle dans l’activation ultérieure du système du complément et dans l’augmentation de la réponse inflammatoire, comme le suggère la découverte récente d’un grand nombre de plasmocytes activés dans le lavage broncho-alvéolaire d’un patient atteint d’une maladie grave à coronavirus. Pneumonie de 2019 (COVID -19).7
L’activation de la cascade du complément provoque non seulement des lésions endothéliales directes, mais recrute également des leucocytes via la formation de C3a et C5a, responsables d’une libération locale massive de cytokines proinflammatoires telles que l’interleukine (IL)-1, l’IL-6, l’IL-8 et l’interféron. . -γ.8
| Dans le cadre de cette réponse immunitaire massive de l’hôte, les lymphocytes, les macrophages résidents, les monocytes et les neutrophiles exercent leurs puissantes fonctions pro-inflammatoires, provoquant des lésions graves supplémentaires des tissus collatéraux et des dommages massifs aux cellules épithéliales endothéliales et alvéolaires vasculaires ainsi qu’une thrombose microvasculaire. 9.10 |
Les implications fonctionnelles de cette pathogenèse particulière du SDRA comprennent une aggravation progressive des déséquilibres ventilation/perfusion et une perte des réflexes de vasoconstriction hypoxiques, avec une composante marquée de thrombose pulmonaire microvasculaire , comme le suggèrent les élévations de la lactate déshydrogénase et des D-dimères. onze
| Aux stades avancés du SDRA, la progression des lésions endothéliales accompagnées d’ une thrombose microvasculaire peut se propager localement dans les poumons et potentiellement étendre la réaction inflammatoire systémique impliquant le lit microvasculaire des reins, du cerveau et d’autres organes vitaux.12 |
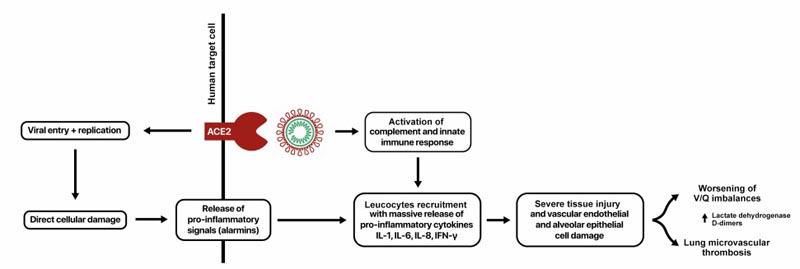 Figure 1. MicroCLOTS (syndrome thromboinflammatoire obstructif microvasculaire pulmonaire microvasculaire COVID-19) comme hypothèse de travail pour le syndrome de détresse respiratoire aiguë atypique
Figure 1. MicroCLOTS (syndrome thromboinflammatoire obstructif microvasculaire pulmonaire microvasculaire COVID-19) comme hypothèse de travail pour le syndrome de détresse respiratoire aiguë atypique
Depuis le début de la pandémie en Italie, notre hôpital a subi une profonde réorganisation pour faire face à l’urgence, et nous avons admis dans notre institution plus de 700 patients atteints d’une pneumonie sévère induite par le SRAS-CoV-2 nécessitant une oxygénothérapie, dont plus de 100 patients admis. . à l’unité de soins intensifs.13
Après notre expérience dans la prise en charge des patients et grâce à un apport multidisciplinaire approfondi, nous proposons désormais un mécanisme de lésion pulmonaire , principalement expliqué par des lésions endothéliales alvéolaires dramatiques conduisant à un syndrome endothélial pulmonaire progressif avec thrombose microvasculaire, et suggérons MicroCLOTS (syndrome thrombo-inflammatoire pulmonaire obstructif microvasculaire (COVID -19) comme hypothèse de travail du SDRA atypique (Figure 1).
















