L’aumento della rilevazione del cancro polmonare non a piccole cellule periferico (NSCLC) ha rinnovato l’interesse per la resezione sublobare invece che per la lobectomia.
Abbiamo condotto uno studio multicentrico di non inferiorità di fase 3 in cui pazienti con NSCLC stadiato clinicamente come T1aN0 (dimensione del tumore, ≤2 cm) sono stati assegnati in modo casuale a sottoporsi a resezione sublobare o resezione lobare dopo conferma intraoperatoria di malattia con linfonodi negativi.
L’ endpoint primario era la sopravvivenza libera da malattia, definita come il tempo intercorso tra la randomizzazione e la recidiva della malattia o la morte per qualsiasi causa.
Gli endpoint secondari erano la sopravvivenza globale, la recidiva locoregionale e sistemica e le funzioni polmonari.
Da giugno 2007 a marzo 2017, un totale di 697 pazienti sono stati assegnati a essere sottoposti a resezione sublobare (340 pazienti) o lobare (357 pazienti).
Dopo un follow-up mediano di 7 anni, la resezione sublobare è risultata non inferiore alla resezione lobare in termini di sopravvivenza libera da malattia (hazard ratio per recidiva di malattia o morte, 1,01; intervallo di confidenza [CI] al 90%, da 0,83 a 1,24). Inoltre, la sopravvivenza globale dopo resezione sublobare era simile a quella dopo resezione lobare (rapporto di rischio di morte, 0,95; IC al 95%, da 0,72 a 1,26).
La sopravvivenza libera da malattia a 5 anni è stata del 63,6% (IC al 95%, da 57,9 a 68,8) dopo resezione sublobare e del 64,1% (IC al 95%, da 58,5 a 69). ,0) dopo la resezione lobare. La sopravvivenza globale a 5 anni è stata dell’80,3% (IC al 95%, da 75,5 a 84,3) dopo resezione sublobare e del 78,9% (IC al 95%, da 74,1 a 82,3) dopo resezione sublobare. 9) dopo resezione lobare.
Non sono state osservate differenze sostanziali tra i due gruppi nell’incidenza di recidive locoregionali o a distanza. A 6 mesi dall’intervento, è stata misurata una differenza tra i gruppi di 2 punti percentuali nella percentuale media del volume espiratorio forzato previsto in 1 secondo, a favore del gruppo sottoposto a resezione sublobare.
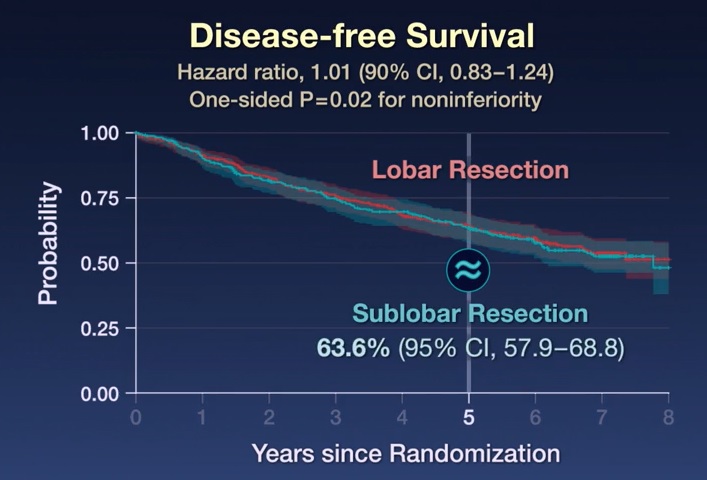
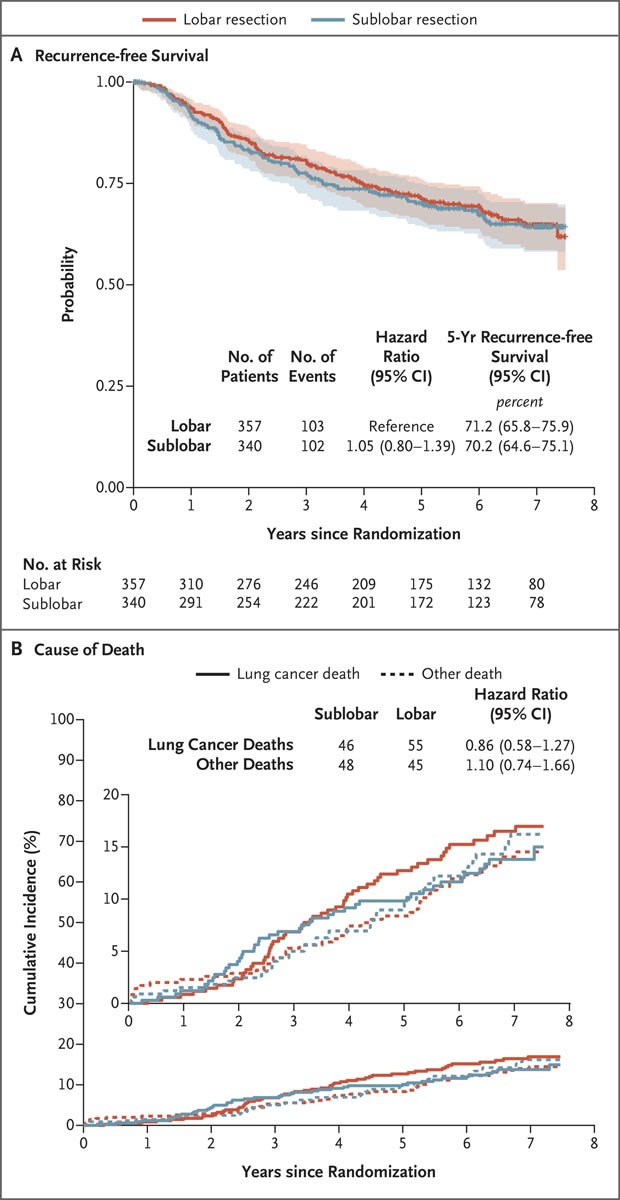
Figura: Sopravvivenza libera da recidiva e causa di morte
Il pannello A mostra la sopravvivenza libera da recidiva nella popolazione intention-to-treat. La sopravvivenza libera da recidiva è stata definita come il tempo intercorso tra la randomizzazione e il verificarsi di una recidiva locoregionale o a distanza; tutti gli altri eventi, inclusa la morte per qualsiasi causa, furono censurati quando si verificarono questi eventi. Le aree ombreggiate indicano intervalli di confidenza al 95%. Il pannello B mostra le funzioni di incidenza cumulativa per la morte correlata al cancro del polmone rispetto alla morte non correlata al cancro del polmone; Quattro pazienti con causa di morte sconosciuta (tre nel gruppo della resezione lobare e uno nel gruppo della resezione sublobare) sono stati esclusi dall’analisi. In entrambi i panel, l’ampiezza degli intervalli di confidenza non è stata aggiustata per la molteplicità e non può essere utilizzata al posto della verifica delle ipotesi.
Nei pazienti con carcinoma polmonare periferico non a piccole cellule (NSCLC) con una dimensione del tumore pari o inferiore a 2 cm e malattia linfonodale negativa confermata patologicamente nei linfonodi ilari e mediastinici, la resezione sublobare è risultata non inferiore alla lobectomia per quanto riguarda la sopravvivenza libera da malattia .
La sopravvivenza globale è stata simile con entrambe le procedure.
In questo ampio studio randomizzato, abbiamo scoperto che nei pazienti con NSCLC in stadio clinico periferico T1aN0 (≤2 cm), la resezione sublobare era non inferiore alla lobectomia rispetto alla sopravvivenza libera da malattia (endpoint primario). Abbiamo anche riscontrato che la sopravvivenza globale (endpoint secondario) era simile con le due procedure. I risultati delle analisi esplorative post hoc che esaminavano l’associazione tra variabili cliniche e demografiche rilevanti e la sopravvivenza libera da malattia e globale erano coerenti con i risultati complessivi dello studio.
Tuttavia, data la piccola dimensione del campione e i pochi eventi in ciascun sottogruppo, questi risultati dovrebbero essere interpretati con cautela. Inoltre, non sono state osservate differenze sostanziali tra i due gruppi nell’incidenza o nei modelli di recidiva della malattia. Le recidive locoregionali erano numericamente leggermente più elevate dopo resezione sublobare rispetto a dopo lobectomia (13,4% vs 10,0%), ma la differenza non era clinicamente significativa. Sebbene non abbiamo richiesto l’estensione della dissezione linfonodale oltre al campionamento delle principali stazioni ilari e di due linfonodi mediastinici, la recidiva regionale si è verificata nell’1,8% dei pazienti dopo resezione sublobare e nel 2,6% dei pazienti dopo lobectomia.
È importante che questi risultati siano interpretati rigorosamente entro i limiti dei criteri di ammissibilità richiesti dallo studio.
(Finanziato dal National Cancer Institute e altri; numero CALGB 140503 ClinicalTrials.gov, NCT00499330. si apre in una nuova scheda.)
















