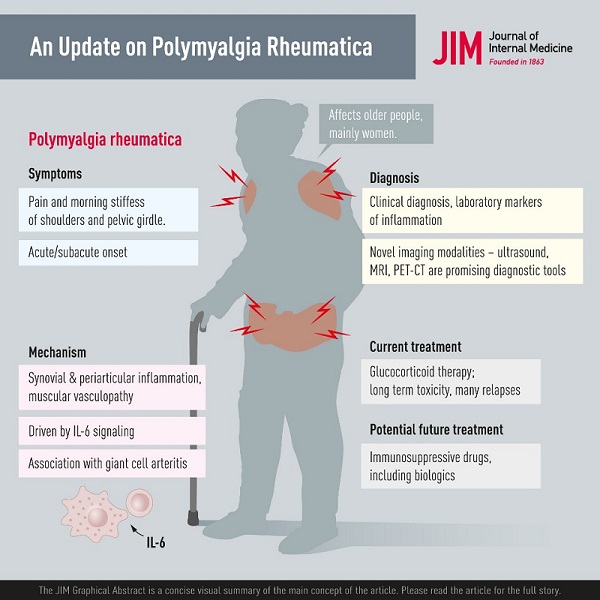
Zusammenfassung Polymyalgia rheumatica (PMR) ist die häufigste entzündlich-rheumatische Erkrankung bei Menschen über 50 Jahren und kommt bei Frauen zwei- bis dreimal häufiger vor. Die häufigsten Symptome sind morgendliche Schmerzen und Steifheit im Schulter- und Beckengürtel. Der Beginn kann akut sein oder sich über einige Tage oder Wochen entwickeln. Es können allgemeine Symptome wie Müdigkeit, Fieber und Gewichtsverlust auftreten, die wahrscheinlich durch die systemische IL-6-Signalübertragung verursacht werden. Die Pathologie umfasst synoviale und periartikuläre Entzündungen sowie muskuläre Vaskulopathie. Eine neue Beobachtung ist, dass PMR als Nebenwirkung einer Krebsbehandlung mit Checkpoint-Inhibitoren auftreten kann. Die Diagnose einer PMR basiert in erster Linie auf Symptomen und Anzeichen in Kombination mit Labor-Entzündungsmarkern. Bildgebende Verfahren, darunter Ultraschall, Magnetresonanztomographie und Positronenemissionstomographie, erweisen sich bei der Untersuchung des Verdachts auf PMR als vielversprechend. Sie sind jedoch immer noch aufgrund der Verfügbarkeit, der hohen Kosten und der unklaren Leistung bei der Diagnosearbeit begrenzt. Die Glukokortikoid-Therapie (GC) ist bei PMR wirksam und die meisten Patienten reagieren schnell auf 15 bis 25 mg Prednisolon pro Tag. Die Behandlung von Patienten mit PMR ist mit Herausforderungen verbunden, da es zu Rückfällen kommt und Patienten mit PMR möglicherweise über längere Zeiträume auf GC bleiben müssen. Dies ist mit einer hohen Rate GC-bedingter Komorbiditäten wie Diabetes und Osteoporose verbunden, und es liegen nur begrenzte Daten zum Einsatz krankheitsmodifizierender Antirheumatika und Biologika als GC-schonende Wirkstoffe vor. Schließlich geht PMR mit einer Riesenzellarteriitis einher, die den Krankheitsverlauf erschweren kann und eine intensivere und längere Behandlung erfordert. |
| Epidemiologie |
Polymyalgia rheumatica (PMR) ist eine rheumatische Erkrankung, die mit Schmerzen des Bewegungsapparates und Steifheit im Nacken-, Schulter- und Hüftbereich einhergeht. Die Ätiologie ist nicht vollständig geklärt, es gibt jedoch damit verbundene Umwelt- und genetische Faktoren.
Die Inzidenz von PMR nimmt mit zunehmendem Alter zu und wird bei Menschen unter 50 Jahren selten beobachtet. Frauen sind etwa zwei- bis dreimal häufiger betroffen.
PMR ist zwei- bis dreimal häufiger als Riesenzellarteriitis (GCA) und tritt bei etwa 50 % der GCA-Patienten auf. Der PMR kann dem ACG vorausgehen, ihn begleiten oder ihm folgen.
Die Inzidenz ist in skandinavischen Ländern und bei Menschen nordeuropäischer Abstammung am höchsten. Die geschätzte Inzidenz und Prävalenz von PMR sind in anderen Teilen der Welt deutlich geringer, obwohl alle Rassen und ethnischen Gruppen betroffen sein können.
Mehrere mögliche Ursachen für PMR werden untersucht. Einige der Theorien beziehen sich auf die genetische Variante HLA-DR4. HLA-DR4-Subtypen wurden mit rheumatoider Arthritis (RA) in Verbindung gebracht, und solche Allele sind auch in vielen Fällen vorhanden, in denen PMR und GCA zusammen auftreten. Es wird vermutet, dass das plötzliche Auftreten von PMR und die Art der Symptome wie Gelenkschmerzen, Fieber und Unwohlsein auf durch Viren verursachte Infektionen zurückzuführen sind.
Schäden an oberflächlichen Arterien durch starke Einwirkung ultravioletter Strahlung der Sonne sind eine weitere vermutete Ursache für die Entwicklung von PMR. Einige Studien deuten darauf hin, dass elastische Fasern in Arterien und Synovialmembranen durch ultraviolette Strahlen beschädigt werden. Diese geschädigten Gewebe können mit Viren infiziert werden, die lange Zeit inaktiv bleiben und später reaktivieren können, was zu PMR führt. Ihr plötzlicher Ausbruch und die in verschiedenen Teilen der Welt gemeldeten großen Unterschiede in der Inzidenz lassen darauf schließen, dass ein oder mehrere Umwelteinflüsse, genetische Faktoren oder beides eine Rolle spielen.
Es wurde auch vermutet, dass PMR und GCA durch die saisonale Grippeimpfung ausgelöst werden könnten. Eine andere Studie berichtete über den ersten Fall eines PMR-ähnlichen Syndroms 7 Tage nach der Impfung. Mehrere Studien haben jedoch berichtet, dass die Symptome in solchen Fällen im Allgemeinen schnell verschwinden.
| Pathogenese und Pathophysiologie |
Die typischen Symptome von Schmerzen und Steifheit der proximalen Muskulatur bei PMR können durch synoviale und periartikuläre Entzündungen in den zentralen Gelenken erklärt werden. Biopsien von unbehandelten PMR-Patienten zeigten eine Synovitis mit Infiltration von Leukozyten (Makrophagen und Gedächtnis-T-Zellen sowie einige B-Zellen) und Gefäßproliferation.
Darüber hinaus kann die Aktivierung des Gefäßendothels für die Pathogenese wichtig sein, da in Synovialbiopsien eine erhöhte Expression des Gefäßendothelwachstumsfaktors (VEGF) beobachtet wurde. Dies kann zur Rekrutierung von Entzündungszellen in diesen Läsionen beitragen. Es wurde gezeigt, dass vasoaktives intestinales Peptid (VIP) in der Synovialmembran von Patienten mit PMR im Vergleich zu Patienten mit RA oder Arthrose in größerem Maße exprimiert wird. Es wurde vermutet, dass Nozizeption im Zusammenhang mit der lokalen VIP-Produktion zu den typischen Schulterbeschwerden bei PMR beitragen könnte.
Darüber hinaus haben Ultraschalluntersuchungen bei der Mehrzahl der Patienten mit PMR eine subakromial-subdeltoide Bursitis und eine Sehnenentzündung des langen Kopfes der Bizeps-Brachii ergeben. Immunfluoreszenzmikroskopische Untersuchungen von Biopsien dieses Muskels zeigten Ablagerungen von Fibrinogen und IgA im perifaszikulären Bereich des Perimysiums. Bei unbehandelter früher PMR wurde eine erhöhte Muskelmikrovaskularisierung beobachtet.
Es wurde gezeigt, dass die Plasmaspiegel von IL-6, jedoch nicht von TNF-α, sowohl bei GCA als auch bei PMR erhöht sind. Die Hauptquelle dieser IL-6-Freisetzung sind CD4+ T-Zellen. Darüber hinaus wurde gezeigt, dass zirkulierende Spiegel des löslichen IL-6-Rezeptors zukünftige Rückfälle bei Patienten mit PMR vorhersagen, was die Bedeutung der IL-6-Signalübertragung in diesem Zusammenhang weiter unterstreicht.
Störungen der zirkulierenden T-Zell- und B-Zell-Untergruppen wurden bei PMR beschrieben, jedoch mit inkonsistenten Ergebnissen. Da es sich bei PMR um eine Erkrankung älterer Menschen handelt, können diese Muster die Alterung des Immunsystems widerspiegeln. Erhöhte Monozytenzahlen im peripheren Blut wurden sowohl bei PMR als auch bei ACG beobachtet, mit einem signifikanten Rückgang nach der Behandlung bei PMR, nicht jedoch bei ACG. Im Gegensatz zu vielen anderen rheumatischen Erkrankungen wurde kein Autoantikörper konsistent mit PMR oder GCA in Verbindung gebracht. Die kombinierten Erkenntnisse belegen eine Wechselwirkung zwischen dem angeborenen und dem adaptiven zellulären Immunsystem.
Während metabolische Eigenschaften (niedrigerer BMI, niedrigerer Nüchternglukosespiegel), die zur Immunregulation beitragen können, nachweislich mit der späteren Entwicklung von GCA in Zusammenhang stehen, muss der Zusammenhang zwischen solchen Faktoren und dem PMR-Risiko noch geklärt werden. wurde nicht untersucht.
| Klinisches Erscheinungsbild und Krankheitsverlauf |
Ein charakteristisches Merkmal von PMR ist ein neues, relativ akutes Auftreten von proximalen Muskelschmerzen und Steifheit im Nacken, in den Schultern, in den Oberarmen, in den Hüften und in den Oberschenkeln. Die Patienten leiden oft unter einer ausgeprägten Morgensteifheit und haben Schwierigkeiten, morgens ins Bett oder aus dem Bett zu kommen. Später am Tag kommt es zu einer spontanen Linderung der Symptome. Steifheit wirkt sich auch auf andere körperliche Aktivitäten am Morgen aus, beispielsweise auf das Anziehen oder andere tägliche Aktivitäten.
Die Symptome entwickeln sich in der Regel innerhalb weniger Tage bis Wochen vollständig. Manchmal ist der Beginn schleichender und kann zu unspezifischen Symptomen wie Müdigkeit, Arthralgie, Appetitlosigkeit, Gewichtsverlust oder Fieber führen. Es ist nicht ungewöhnlich, dass sich einige Patienten einer Untersuchung auf Verdacht auf Malignität unterziehen, bevor eine PMR-Diagnose gestellt werden kann.
Ein unspezifisches klinisches Erscheinungsbild und das Fehlen spezifischer Laborbefunde oder serologischer Merkmale führen häufig zu einer gewissen Verzögerung der Diagnose.
PMR stellt eine erhebliche Belastung für den Alltag älterer Menschen dar. Die psychologischen Auswirkungen sind erheblich, einschließlich Angstzuständen im Zusammenhang mit einer aktiven Erkrankung und Nebenwirkungen der Glukokortikoid-Behandlung (GC).
| Assoziation mit Arteriitis temporalis |
PMR und Arteriitis temporalis (TA) treten oft gleichzeitig auf, was auf gemeinsame prädisponierende Faktoren und gemeinsame Krankheitsmechanismen schließen lässt. Da die typische Histopathologie von TA in TA-Biopsien das Vorhandensein von Riesenzellen umfasst, wird die Krankheit oft als GCA bezeichnet.
Die Riesenzellarteriitis (GCA) ist eine systemische Vaskulitis, die mehrere große Gefäße betreffen kann, häufig, aber nicht immer, einschließlich der Schläfenarterie.
Eine Begleitdiagnose einer GCA sollte bei einem Patienten mit PMR vermutet werden, der außerdem neu auftretende Kopfschmerzen, Kiefer-Claudicatio, neue und ungeklärte visuelle Symptome oder schwere konstitutionelle Symptome (Fieber unbekannter Ursache, Gewichtsverlust, Müdigkeit usw.) hat. Solche Symptome können beim ersten Auftreten einer PMR oder später im Krankheitsverlauf auftreten.
Bei Patienten mit PMR kann es auch zu einer subklinischen Arteriitis kommen. In systematischen Studien an Patienten mit einem typischen klinischen Phänotyp der PMR, aber ohne Anzeichen oder Symptome, die mit einer GCA vereinbar sind, wurden histopathologische Befunde einer Vaskulitis in Schläfenarterienbiopsien bei bis zu 21 % und sonographische Merkmale einer TA bei bis zu 32 % gefunden. %. Das Wiederauftreten von PMR-Symptomen ist ein häufiges Merkmal eines GCA-Rückfalls.
| Diagnose- und Klassifizierungskriterien |
Es wurden viele verschiedene diagnostische Kriterien vorgeschlagen. Der Zweck dieser Kriterien besteht darin, Ärzten bei der Diagnose von PMR bei einzelnen Patienten zu helfen. Die meisten dieser Kriterien basieren auf demografischen, klinischen und Labormerkmalen der PMR. Die EULAR/ACR-Kriterien sind in Tabelle 1 zusammengefasst. Die Klassifizierungskriterien sollen in epidemiologischen Studien verwendet werden und nicht dazu, eine Diagnose bei einzelnen Patienten zu stellen.
Tabelle 1. Vorläufige EULAR/ACR-Klassifizierungskriterien für Polymyalgia rheumatica (modifiziert nach Dasgupta et al.)
| Kriterien | Punkte |
Dauer der Morgensteifigkeit > 45 Min Hüftschmerzen oder eingeschränkte Bewegungsfreiheit Fehlen von RF und/oder Anti-CCP Fehlen einer anderen gemeinsamen Beteiligung Mindestens eine Schulter mit Schleimbeutelentzündung subdeltoideus und/oder Bizepssehnenscheidenentzündung und/oder glenohumerale Synovialitis (entweder posterior oder axillär) und mindestens eine Hüfte mit Synovitis und/oder Trochanterschleimbeutelentzündung Beide Schultern mit Bursitis subdeltoideus, Bizeps-Tenosynovitis oder Glenohumeral-Synovitis |
2 1 2 1 0/1*
0/1* |
| Hinweis: Zur Klassifizierung der Polymyalgia rheumatica erforderliche Punktzahl: 4 oder mehr ohne Ultraschall und 5 oder mehr im Algorithmus mit Ultraschall. Erforderliche Kriterien: Alter ≥ 50 Jahre, beidseitige Schulterschmerzen und abnormale C-reaktive Protein- und/oder Erythrozytensedimentationsrate. * Ohne/mit Ultraschall. Abkürzungen: Anti-CCP, antizyklischer citrullinierter Peptid-Antikörper; ACR, American College of Rheumatology; EULAR, Europäische Allianz der Rheumatologie-Vereinigungen; RF, Rheumafaktor. |
|
Die Sensitivität und Spezifität der Kriterien hängt davon ab, ob die PMR alle Erkrankungen unterscheidet, einschließlich RA oder Erkrankungen, die die Schultern betreffen. Sensitivität und Spezifität variieren auch je nachdem, ob Ultraschall verwendet wird oder nicht. Ein Score ≥4 hatte eine Sensitivität von 68 % und eine Spezifität von 78 %. Bei der Unterscheidung von Schulterbeschwerden bei PMR stieg die Spezifität auf 88 %, während sie bei der Unterscheidung zwischen RA und PMR nur 65 % betrug. Unter Verwendung von Ultraschall hatte ein Score ≥5 eine Sensitivität von 66 % und eine Spezifität von 81 %.
| Diagnose |
Es gibt keinen Goldstandard für die Diagnose von PMR und im Gegensatz zu vielen anderen rheumatischen Syndromen gibt es keine spezifischen klinischen Manifestationen, Serologie oder andere Laborbefunde. Daher kann die Diagnose eine Herausforderung sein.
Diagnose In der täglichen Praxis basiert die Diagnose einer PMR hauptsächlich auf der folgenden Kombination: neu auftretende Symptome von Morgensteifheit und Schmerzen im Schulter- und Beckengürtel bei einer Person ab 50 Jahren, Hinweise auf eine systemische Entzündung mit erhöhter Blutsenkungsgeschwindigkeit ( ESR) und/oder CRP, keine andere Krankheit, die das klinische Erscheinungsbild und schließlich die abrupte Reaktion auf GCs besser erklärt. Bei einigen diagnostischen Kriterien gibt es weitere spezifische Anforderungen, wie z. B. eine Symptomdauer von 2 Wochen oder negative Tests auf Rheumafaktoren oder antinukleäre Antikörper. |
Die Diagnose einer PMR sollte klinisch geprüft werden.
Der typische Fall ist eine ältere Frau, die morgens als erstes beidseitige Schulterschmerzen und Steifheit hat. Ähnliche Symptome treten häufig im Beckengürtel auf. Die Symptome lassen normalerweise im Laufe des Tages nach. Bei etwa einem Drittel der Patienten können systemische Manifestationen wie Fieber, Müdigkeit, Appetitlosigkeit und Gewichtsverlust auftreten.
Andere Entzündungsparameter können erhöht sein, beispielsweise die Anzahl der weißen Blutkörperchen oder der Blutplättchen, und manchmal können Leberenzyme oder alkalische Phosphatase als Zeichen einer systemischen Entzündung erhöht sein. Bei der klinischen Untersuchung wird häufig eine tiefe Palpationsempfindlichkeit der Muskeln im Schulter- und Oberschenkelbereich festgestellt. Darüber hinaus besteht in der Regel eine eingeschränkte Beweglichkeit der Schultern ohne Muskelschwund oder -schwäche. Gelegentlich können Anzeichen einer Synovitis in den Schultern, Handgelenken und Knien beobachtet werden. Schließlich reagieren die meisten Patienten bei PMR schnell und dramatisch auf GCs, und nach bestimmten Kriterien ist diese Reaktion für die Diagnose notwendig.
| Bildgebende Studien |
Aufgrund der unspezifischen Symptome oder Laborbefunde der PMR besteht ein ungedeckter Bedarf an anderen Modalitäten zur Bestätigung der Diagnose. Bei der PMR kommen verschiedene bildgebende Verfahren zum Einsatz, darunter konventionelle Radiologie, Szintigraphie, Computertomographie (CT), Magnetresonanztomographie (MRT), Ultraschall und Positronenemissionstomographie mit CT (PET-CT).
Ziel bildgebender Untersuchungen bei PMR ist nicht nur die Bestätigung der Diagnose, sondern auch der Ausschluss von Differenzialdiagnosen oder Komorbiditäten und in manchen Fällen auch das Vorliegen einer Vaskulitis großer Gefäße.
Ultraschall ist bei PMR aufgrund der Art der extraartikulären Weichteilbeteiligung nützlich . Die häufigsten Befunde sind Entzündungen und Ergüsse der Bursa subacromialis-subdeltoideus, Tenosynovitis des Bizeps, Entzündungen des Glenohumeralgelenks sowie Synovitis und Trochanteritis der Hüfte. Ultraschall ist auch nützlich, um andere Differentialdiagnosen auszuschließen und um eine Vaskulitis großer Gefäße und eine kraniale Arteriitis zu erkennen, wenn der Verdacht besteht, dass sie gleichzeitig mit einer PMR vorliegen.
Auch die MRT wurde eingesetzt, allerdings ist ihr Einsatz in der Forschung noch begrenzt. Zu den Befunden gehört ein charakteristisches Muster symmetrischer Entzündungen im Trochanter major, im Acetabulum und im Sitzbeinhöcker, über das in einer Studie bei 64 % der Patienten mit PMR berichtet wurde. In einer anderen Studie wiesen alle Patienten mit neu aufgetretener PMR mindestens eine Stelle einer myofaszialen Entzündung auf. Zu den Vorteilen der MRT gegenüber der Ultraschalluntersuchung gehört, dass die MRT spezifischer ist und bei der Beurteilung einer Vaskulitis weniger Unterschiede zwischen den Beobachtern aufweist. Zu den Nachteilen zählen Verfügbarkeit und Kosten.
PET- CT wird in der Onkologie und bei der Erforschung entzündlicher Erkrankungen eingesetzt. Bei Patienten mit Verdacht auf PMR wird die Verwendung der PET-CT als Routineuntersuchung aufgrund von Einschränkungen wie Kosten und Verfügbarkeit nicht empfohlen. Zusätzlich zu ihrer Rolle bei der Visualisierung von Entzündungen im artikulären und extraartikulären Gewebe ist die PET-CT äußerst nützlich, um den Verdacht auf eine Vaskulitis großer Gefäße zu bestätigen und zwischen PMR und anderen Erkrankungen wie bösartigen Tumoren oder anderen rheumatischen Erkrankungen zu unterscheiden. Sein Einsatz ist bei Patienten gerechtfertigt, die auf die Erstbehandlung mit GC nicht angesprochen haben. Die mangelnde Reaktion könnte durch eine gleichzeitig bestehende Vaskulitis großer Gefäße, andere zugrunde liegende rheumatische Erkrankungen oder bösartige Erkrankungen erklärt werden.
> Andere Bildgebungsstudien
Konventionelle Radiographie wurde in diesem Zusammenhang bereits früher eingesetzt, insbesondere bei Patienten mit Verdacht auf PMR und periphere Gelenkerkrankung. Arthritis bei PMR ist in der Regel nicht erosiv, was sie von der destruktiven Arthritis unterscheidet, die für RA oder andere arthritische Erkrankungen wie Chondrokalzinose typisch ist. Die Szintigraphie wird derzeit nicht eingesetzt.
| Laborbefunde |
Es liegen keine serologischen oder sonstigen spezifischen Laborbefunde vor, die die Diagnose einer PMR mit absoluter Sicherheit bestätigen können.
Der häufigste und wichtigste Befund ist die Erhöhung von Entzündungsparametern wie ESR oder CRP. Eine normale ESR schließt jedoch die Diagnose einer PMR nicht aus. Weitere Befunde sind normozytäre normochrome Anämie, Thrombozytose und Leukozytose.
| Differenzialdiagnose |
Erkrankungen, die Menschen ab 50 Jahren betreffen und mit beidseitigen Schulterschmerzen einhergehen, sollten in die Differenzialdiagnose der PMR einbezogen werden. Die Differenzialdiagnose sollte sowohl rheumatische als auch nicht-rheumatische Erkrankungen umfassen.
> Rheumatoide Arthritis
Zu den wichtigsten rheumatischen Erkrankungen in der Differenzialdiagnose der PMR gehört die seronegative RA. Dies gilt insbesondere zu Beginn der RA-Erkrankung, bei der es zu einer Prodromalphase einer beidseitigen Arthritis des Schultergelenks kommen kann. Darüber hinaus können sowohl RA als auch PMR mit Arthritis in den Handgelenken einhergehen, und wenn bei Patienten ein negativer Rheumafaktor und/oder antizyklisches citrulliniertes Peptid (Anti-CCP) festgestellt wird, ist die Unterscheidung zwischen diesen beiden Erkrankungen möglicherweise nicht einfach.
Das Vorliegen einer symmetrischen Arthritis kleiner Gelenke sollte jedoch die Diagnose einer RA begünstigen. Sowohl RA als auch PMR können erfolgreich mit Prednisolon behandelt werden, was den Nutzen dieses Medikaments bei der Differenzierung einschränkt. Typische extraartikuläre Manifestationen (z. B. rheumatische Knötchen, kutane Vaskulitis, Serositis usw.) und positive RF/Anti-CCP begünstigen die Diagnose einer RA statt einer PMR.
> Myositis
Polymyositis (PM ) ist eine weitere Krankheit, die fälschlicherweise als PMR diagnostiziert werden kann und umgekehrt. Beide Erkrankungen betreffen die proximalen Muskelgruppen der oberen und unteren Extremitäten. Allerdings ist das Vorhandensein von Muskelschwäche anstelle von Steifheit und Schmerzen ein wichtiges Unterscheidungsmerkmal von PM. Darüber hinaus ist PM im Allgemeinen mit erhöhten Serumspiegeln von Muskelenzymen verbunden, was kein Merkmal von PMR ist. Weitere Merkmale, die die Möglichkeit einer PM begünstigen, sind das Vorhandensein von Myositis-spezifischen Autoantikörpern und extramuskuläre Manifestationen. Schluckbeschwerden begünstigen die Diagnose PM. Reine Muskelschwäche ist nicht typisch für PMR.
> Schmerzsyndrome
Die Unterscheidung zwischen PMR und Schmerzsyndromen wie Fibromyalgie dürfte im Vergleich zu anderen Differenzialdiagnosen einfacher sein. Fibromyalgie tritt im Allgemeinen in jüngeren Altersgruppen auf. Darüber hinaus gibt es keine erhöhten Laborwerte, die auf eine entzündliche Erkrankung hinweisen. Es ist wichtig, zwischen diesen beiden Erkrankungen zu unterscheiden, um den unnötigen Einsatz von GC bei Patienten mit Fibromyalgie und Schmerzsyndromen zu vermeiden.
> Malignität
Eine wichtige Differenzialdiagnose bei PMR sind bösartige Erkrankungen.
PMR-Manifestationen könnten ein paraneoplastisches Symptom darstellen. Patienten mit PMR, die nicht auf eine tägliche Prednisolondosis von 15 bis 25 mg ansprechen oder bei denen direkt nach dem Ausschleichen der GCs ein schnelles Wiederauftreten der Symptome auftritt, sollten den behandelnden Arzt auf die Möglichkeit einer zugrunde liegenden bösartigen Erkrankung aufmerksam machen.
Die remittierende seronegative symmetrische Synovitis mit Lochfraßödem ist ein klinisches Syndrom, das durch die Entwicklung einer symmetrischen kleinen Gelenkarthritis mit Ödemen an Händen und Füßen gekennzeichnet ist, typischerweise bei älteren Männern mit negativem Rheumafaktor. Dieser Zustand spricht in der Regel gut auf eine kurze orale GC an und sollte eine der wichtigen Differenzialdiagnosen für PMR sein. Ein ähnlicher Phänotyp lässt sich bei paraneoplastischen Syndromen beobachten.
> Andere
Nicht entzündliche degenerative Erkrankungen wie zervikale Spondylose und Arthrose des Hüftgelenks können das Erscheinungsbild einer PMR mit Symptomen wie Schmerzen und Morgensteifheit imitieren. Der radiologische Nachweis von Osteoarthrose (OA) oder Spondylose sowie das Fehlen aktiver Entzündungsparameter begünstigen die Diagnose von Spondylose und OA anstelle der PMR. Hypothyreose ist eine häufige Erkrankung bei Frauen mit diffusen Schmerzen, Müdigkeit und einem Fibromyalgie-ähnlichen Syndrom.
| PMR als Ereignis im Zusammenhang mit der Verwendung von Immun-Checkpoint-Inhibitoren in der Krebsbehandlung |
Immun-Checkpoint-Inhibitoren (ICIs) werden zunehmend in der Krebstherapie eingesetzt, um die Antitumor-Immunantwort zu verstärken. Die Behandlung mit monoklonalen Antikörpern, die das CTLA-4-Protein, den Rezeptor (PD-1) oder seinen Liganden PD-L1 blockieren, wurde mit der Entwicklung einer Reihe von Autoimmunerkrankungen in Verbindung gebracht. PMR ist eine der rheumatischen Erkrankungen, über die in diesem Zusammenhang als entsprechendes Ereignis berichtet wurde.
Darüber hinaus gibt es mehrere Berichte über Fälle einer „PMR-ähnlichen Erkrankung“ mit einigen atypischen Merkmalen nach der Behandlung mit ICIs. Eine sorgfältige Charakterisierung solcher Fälle könnte uns dabei helfen, die Rolle des adaptiven Immunsystems in der Pathophysiologie der PMR zu verstehen.
| Behandlung |
> Mündliche GC
Der Grundstein bei der Behandlung von PMR ist die orale GC. Alle PMR-Symptome reagieren im Allgemeinen schnell auf GCs. Die empfohlene tägliche Anfangsdosis von Prednisolon bei PMR beträgt 12,5 bis 25 mg gemäß der neuesten ACR/EULAR-Empfehlung. Eine Anfangsdosis von 20 mg ist besser als 10 mg, geht jedoch mit mehr Nebenwirkungen einher. Bei der Auswahl im Bereich von 12,5 bis 25 mg sollten die Entzündungsaktivität, das Rückfallrisiko und das Risiko einer GC-Toxizität aufgrund von Komorbiditäten wie Diabetes oder Herz-Kreislauf-Erkrankungen berücksichtigt werden.
Die Prednisolondosis sollte schrittweise um etwa 2,5 mg pro Monat auf 10 mg pro Tag reduziert werden, danach wird die langsamere Ausschleichung fortgesetzt. Ein schlechtes Ansprechen auf die Behandlung sollte dazu führen, mögliche Differenzialdiagnosen zu überdenken. Die GC-Behandlung sollte von unterstützenden Maßnahmen begleitet werden, um Langzeittoxizität wie Osteoporose zu minimieren.
Im Allgemeinen ist die Prognose der PMR gut und die Krankheit heilt in der Regel innerhalb weniger Jahre aus. In dieser Zeit sollte GC eingenommen werden, um die Krankheit und ihre Symptome zu kontrollieren. Einige Patienten haben einen komplizierteren Verlauf mit einer verbleibenden Entzündung während der Behandlung und einem Wiederauftreten der Symptome beim Versuch, die GC-Dosis zu reduzieren. In einer Studie von Healey waren nur 30 % der Patienten in der Lage, die GC-Behandlung abzubrechen und innerhalb von zwei Jahren nach der Nachuntersuchung asymptomatisch zu bleiben, während nur 2 % in der Lage waren, die GC-Behandlung innerhalb von 6 Monaten vollständig zu beenden.
> injizierbares GC
Intramuskuläres Methylprednisolon (IMPM) wurde hinsichtlich Wirksamkeit und Sicherheit mit oralen GCs bei der Behandlung von PMR verglichen. In einer Studie von Dasgupta et al. war die Remissionsrate nach einer 12-wöchigen Doppelblindphase ähnlich, aber die mittlere kumulative GC-Dosis in der Gruppe mit intramuskulärem Methylprednisolon betrug nach 96 Wochen 56 % derjenigen in der Gruppe mit intramuskulärem Methylprednisolon. mündliche GC-Gruppe. Die IM-Gruppe hatte weniger langfristige unerwünschte Ereignisse. MPim ist wahrscheinlich eine geeignete Alternative zu oralen GCs bei älteren Patienten, die mehrere Medikamente einnehmen, sowie bei Patienten, bei denen es zu Problemen bei der Einhaltung des Zeitplans zur oralen GC-Ausschleichung kommt, und bei Patienten mit Adhärenzproblemen.
> Krankheitsmodifizierende Antirheumatika und biologische Produkte
Aufgrund der Toxizität einer langfristigen GC-Therapie besteht ein klarer Bedarf an alternativen Strategien bei Patienten mit PMR. Antirheumatika, die bei der Behandlung von RA und mehreren anderen rheumatischen Erkrankungen große Erfolge erzielt haben, wurden bei PMR jedoch nicht umfassend untersucht.
Es gibt Hinweise auf einen Nutzen von Methotrexat (MTX) bei Patienten mit PMR. In einer doppelblinden, randomisierten, kontrollierten Studie (RCT) wurde bei Patienten mit neu aufgetretener PMR, die MTX zusätzlich zu einem regulären GC-Regime einnahmen, im Vergleich zur Vergleichsgruppe ein geringeres Rückfallrisiko und eine höhere Wahrscheinlichkeit eines Abbruchs der GC nachgewiesen. der GC + Placebo einnahm. Die Wirksamkeit von MTX bei wiederkehrender und langjähriger PMR wurde nicht systematisch evaluiert.
Basierend auf dieser Art von Beweisen empfahl das ACR/EULAR-Gremium unter Vorbehalt, die frühzeitige Einführung von MTX in Betracht zu ziehen, insbesondere bei Patienten mit hohem Rückfallrisiko und/oder längerer Therapie, beispielsweise weiblichen Patienten mit hoher Ausgangs-BSR (>40 mm/h). , periphere Arthritis und/oder Komorbiditäten, die durch die GC-Therapie verschlimmert werden können.
Es liegen nur sehr begrenzte Daten zur Verwendung von Azathioprin bei der Behandlung von PMR vor. Trotz begrenzter Beweise wurde Azathioprin bei einigen Patienten mit refraktärer PMR eingesetzt. Die ACR/EULAR-Empfehlungen zur Behandlung von PMR schließen Azathioprin nicht ein. Eine retrospektive Studie von geringer Qualität zeigte, dass das Malariamittel Hydroxychloroquin, das bei anderen Erkrankungen eingesetzt wird, Rückfälle bei PMR nicht wirksam verhindert.
Da sich gezeigt hat, dass der monoklonale Anti-IL-6-Rezeptor-Antikörper Tocilizumab bei GCA wirksam ist, gibt es gute Gründe, ihn als Therapie für PMR zu untersuchen. Viele Fallberichte und Fallserien deuten auf die Wirksamkeit von intravenösem Tocilizumab bei einzelnen Patienten mit PMR hin. Eine retrospektive Kohortenstudie zur Tocilizumab- oder MTX-Behandlung bei rezidiviertem PMR in Japan zeigte einen signifikanten Effekt von Tocilizumab auf die GC-Erhaltung, nicht jedoch von MTX. Placebokontrollierte RCTs der TNF-Inhibitoren Infliximab oder Etanercept zeigten keinen signifikanten Nutzen bei Patienten mit PMR und werden daher nicht zur Behandlung von PMR empfohlen.
> Unterstützende Therapien
Die langfristige Anwendung von GC ist ein wichtiger Faktor, der zu mehreren Komorbiditäten bei Patienten mit rheumatischen Erkrankungen wie systemischer Vaskulitis, PMR und GCA beiträgt. Es wird empfohlen, dass alle Patienten mit PMR zu Beginn ihrer Erkrankung andere unterstützende Therapien wie Kalzium/Vitamin D und Bisphosphonate erhalten, um Osteoporose vorzubeugen.
| Komorbiditäten |
Es liegen nur begrenzte Informationen zu Komorbiditäten bei Patienten mit PMR aus großen epidemiologischen Studien vor. Bei einer systematischen Durchsicht der Literatur gab es einige Hinweise auf ein erhöhtes Risiko für Komorbiditäten bei Patienten mit diagnostizierter PMR. Diese Komorbiditäten können in Gefäßerkrankungen, Krebs und andere Krankheiten eingeteilt werden, zu letzteren zählen Hypothyreose und Divertikelkrankheit.
Die häufigste Komorbidität, über die nach der Diagnose einer PMR berichtet wird, ist eine Gefäßerkrankung. Zu den Gefäßerkrankungen zählen Schlaganfall, Myokardinfarkt und periphere Gefäßerkrankungen. Dies steht im Einklang mit einem erhöhten Risiko für Herz-Kreislauf-Erkrankungen bei anderen chronisch entzündlichen Erkrankungen wie RA.
Während einige Studien von einem erhöhten Krebsrisiko berichteten, berichteten andere von einem geringeren Risiko oder die Ergebnisse waren nicht eindeutig. Bezüglich anderer Komorbiditäten gibt es widersprüchliche Daten zu einem Zusammenhang mit Hypothyreose. Es gibt einige Berichte über ein erhöhtes Risiko für Depressionen, die mit chronischen Schmerzen oder einer GC-Behandlung verbunden sein können.
Daten aus einer aktuellen nationalen Kohortenstudie im Vereinigten Königreich belegen das erhöhte Risiko für Gefäßerkrankungen nach der PMR-Diagnose. Darüber hinaus bestand nach der Diagnose PMR auch das Risiko für Atemwegs-, Nieren- und Autoimmunerkrankungen. Zumindest für die letzten beiden könnte die Erklärung Überwachungsvoreingenommenheit sein.
Patienten mit PMR haben eine hohe Rate an Komorbiditäten im Zusammenhang mit der GC-Behandlung, wie z. B. Osteoporose, Wirbelfrakturen, Infektionen, Katarakte und Glaukom. In einer Kohortenstudie in Olmstead, Minnesota, USA, traten jedoch bei Patienten mit PMR, die durchschnittlich 5,8 Jahre lang beobachtet wurden, nur Katarakte häufiger auf als bei alters- und geschlechtsangepassten Vergleichspatienten ohne PMR.
Möglicherweise könnte das nicht erhöhte Risiko für Osteoporose und Frakturen auf die häufige Anwendung der Osteoporoseprophylaxe bei dieser Patientengruppe mit geplanter Langzeitbehandlung mit GC und anderen Risikofaktoren für Osteoporose zurückzuführen sein. Solche Muster können vom Zugang zur Gesundheitsversorgung in verschiedenen Bevölkerungsgruppen abhängen.
| Sterblichkeit |
Angesichts der hohen Komorbiditätslast bei Patienten mit PMR ist es wichtig festzustellen, ob die Diagnose einer PMR mit einem erhöhten Mortalitätsrisiko verbunden ist. Eine kürzlich durchgeführte systematische Überprüfung ergab, dass Patienten mit PMR im Vergleich zu Kontrollpersonen gleichen Alters und Geschlechts eine höhere Belastung durch komorbide Erkrankungen hatten. Drei frühere Studien berichteten jedoch über eine verringerte Mortalität bei Patienten mit diagnostizierter PMR.
Eine mögliche Erklärung hierfür könnte Überwachungsbias sein. Bei Patienten mit chronischen Erkrankungen (und insbesondere PMR, bei denen eine regelmäßige Beurteilung und Überwachung empfohlen wird) ist die Wahrscheinlichkeit höher, dass ihr Zustand und sich entwickelnde Morbiditäten aktiv überwacht werden, was zu einer Behandlung der Krankheit in einem frühen Stadium führt.
Eine weitere Studie, bekanntermaßen die größte Studie zur Abschätzung der Auswirkungen einer PMR-Diagnose auf die Lebenserwartung, zeigte, dass eine PMR-Diagnose keinen signifikanten Einfluss auf die Lebenserwartung hat. Daher scheint die Diagnose PMR das Risiko eines vorzeitigen Todes nicht zu erhöhen.
Abschluss
|















