Arrière-plan
Le vaccin ChAdOx1 nCoV-19 (AZD1222) a été approuvé pour une utilisation d’urgence par l’autorité de réglementation britannique, l’Agence de réglementation des médicaments et des produits de santé, avec un schéma thérapeutique de deux doses standard administrées à 4 à 12 semaines d’intervalle. Le déploiement prévu au Royaume-Uni impliquera de vacciner immédiatement les personnes appartenant aux catégories à haut risque avec leur première dose et d’administrer la deuxième dose 12 semaines plus tard.
Nous fournissons ici une analyse groupée prédéfinie supplémentaire des tests ChAdOx1 nCoV-19 et des analyses exploratoires de l’impact sur l’immunogénicité et l’efficacité de l’allongement de l’intervalle entre les doses d’amorçage et de rappel. De plus, nous montrons l’immunogénicité et la protection apportées par la première dose , avant qu’une dose de rappel ne soit proposée.
Méthodes
Nous présentons les données de trois essais contrôlés randomisés en simple aveugle : une étude de phase 1/2 au Royaume-Uni (COV001), une étude de phase 2/3 au Royaume-Uni (COV002) et une étude de phase 3 au Brésil (COV003). . et une étude de phase 1/2 en double aveugle en Afrique du Sud (COV005).
Comme décrit ci-dessus, les personnes âgées de 18 ans ou plus ont été randomisées selon un rapport 1:1 pour recevoir deux doses standard de ChAdOx1 nCoV-19 (5 × 1010 particules virales) ou un vaccin témoin ou un placebo salin. Dans l’essai britannique, un sous-ensemble de participants a reçu une dose plus faible (2,2 × 1010 particules virales) de ChAdOx1 nCoV-19 pour la première dose.
Le critère de jugement principal était une maladie symptomatique à COVID-19 confirmée virologiquement, définie comme un test d’amplification des acides nucléiques sur écouvillon (TAAN) positif associé à au moins un symptôme admissible (fièvre ≥ 378°C, toux, essoufflement ou anosmie ou agueusie). que 14 jours après la deuxième dose.
Les analyses secondaires d’efficacité incluaient les cas survenus au moins 22 jours après la première dose. Les réponses en anticorps mesurées par dosage immunologique et par neutralisation du pseudovirus étaient des résultats exploratoires.
Tous les cas de COVID-19 positifs sur écouvillon TAAN ont été évalués pour inclusion dans l’analyse par un comité indépendant d’examen des paramètres en aveugle.
L’analyse principale a inclus tous les participants qui étaient séronégatifs pour la protéine N du SRAS-CoV-2 au départ, qui avaient bénéficié d’un suivi d’au moins 14 jours après la deuxième dose et qui n’avaient aucun signe d’infection antérieure par le SRAS-CoV-2. 2 par écouvillon TAAN.
L’innocuité a été évaluée chez tous les participants ayant reçu au moins une dose. Les quatre essais sont enregistrés auprès de ISRCTN89951424 (COV003) et ClinicalTrials.gov, NCT04324606 (COV001), NCT04400838 (COV002) et NCT04444674 (COV005).
Résultats
Entre le 23 avril et le 6 décembre 2020, 24 422 participants ont été recrutés et vaccinés dans les quatre études, dont 17 178 ont été inclus dans l’analyse primaire (8 597 ont reçu ChAdOx1 nCoV-19 et 8 581 ont reçu le vaccin témoin). La date limite des données pour ces analyses était le 7 décembre 2020. 332 infections positives au TAAN ont atteint le critère d’évaluation principal d’une infection symptomatique plus de 14 jours après la deuxième dose.
L’ efficacité globale du vaccin plus de 14 jours après la deuxième dose était de 66 % (IC 95 % : 57,4-74,0), avec 84 (10 %) cas chez les 8 597 participants du groupe ChAdOx1 nCoV-19 et 248 ( 2,9%) chez les 8 581 participants du groupe témoin.
Il n’y a eu aucune hospitalisation pour COVID-19 dans le groupe ChAdOx1 nCoV-19 après la période d’exclusion initiale de 21 jours, et 15 dans le groupe témoin. 108 (0,9 %) des 12 282 participants du groupe ChAdOx1 nCoV-19 et 127 (11 %) des 11 962 participants du groupe témoin ont présenté des événements indésirables graves.
Il y a eu sept décès considérés comme non liés à la vaccination (deux dans le groupe ChAdOx1 nCov-19 et cinq dans le groupe témoin), dont un décès lié au COVID-19 chez un participant du groupe témoin.
Des analyses exploratoires ont montré que l’efficacité du vaccin après une dose standard unique du jour 22 au jour 90 après la vaccination était de 76,0 % (59,3–85,9). Notre analyse de modélisation a indiqué que la protection n’a pas diminué au cours de cette période initiale de trois mois.
De même, les niveaux d’anticorps ont été maintenus pendant cette période avec une baisse minime au jour 90 (rapport de moyenne géométrique [GMR] 0,66 [IC à 95 % 0,59-0,74]).
Chez les participants ayant reçu deux doses standards, après la deuxième dose, l’efficacité était plus grande chez ceux avec un intervalle d’amorçage plus long (efficacité du vaccin 81,3 % [IC à 95 % 60,3-91,2] à ≥12 semaines) que chez ceux avec un intervalle court (efficacité du vaccin 81,3 % [IC à 95 % 60,3-91,2] à ≥12 semaines ) efficacité 55,1 % [33,0–69,9] en <6 semaines).
Ces observations sont étayées par des données d’immunogénicité qui ont montré que les réponses en anticorps de liaison ont plus que doublé après un intervalle de 12 semaines ou plus, par rapport à un intervalle de moins de 6 semaines chez les personnes âgées de 18 à 55 ans (GMR 2,32 [2·01–2· 68]).
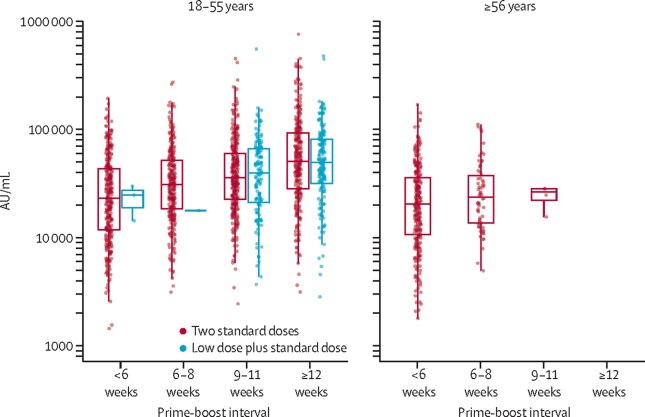
Réponses IgG anti-SARS-CoV-2 maximales par test immunologique multiplex 28 jours après la deuxième dose chez les participants recevant deux doses standard ou une faible dose plus une dose standard, par intervalle d’amorçage-rappel (n = 3 337)
Interprétation Les résultats de cette analyse primaire de deux doses de ChAdOx1 nCoV-19 étaient cohérents avec ceux observés lors de l’analyse intermédiaire des essais et confirment que le vaccin est efficace, avec des résultats variant selon l’intervalle de dose dans les analyses exploratoires. Un intervalle d’administration de trois mois pourrait présenter des avantages par rapport à un calendrier d’intervalle d’administration court pour le déploiement du vaccin contre la pandémie afin de protéger le plus grand nombre de personnes dans la population le plus rapidement possible lorsque les approvisionnements sont restreints, tout en améliorant en même temps la protection après avoir reçu une deuxième dose. |
Recherche en contexte
Données probantes antérieures à cette étude
Le vaccin ChAdOx1 nCoV-19 (AZD1222) a été approuvé pour une autorisation d’utilisation d’urgence au Royaume-Uni sur la base des résultats intermédiaires d’efficacité de 131 cas de COVID-19 symptomatique primaire, avec une efficacité basée sur deux des quatre essais du vaccin. Le déploiement prévu du vaccin au Royaume-Uni implique l’administration de deux doses à 12 semaines d’intervalle, une politique qui a reçu de nombreux retours.
Valeur ajoutée de cette étude
Ce rapport fournit des résultats d’efficacité primaires mis à jour après un mois supplémentaire de collecte de données. Le rapport intermédiaire comprenait 131 cas de COVID-19 symptomatique primaire. Les derniers résultats avec un suivi supplémentaire incluent 332 cas de COVID-19 symptomatique primaire. Les estimations d’efficacité incluent désormais les données des quatre études sur le vaccin menées dans trois pays, tandis que l’analyse intermédiaire n’incluait que deux études dans les évaluations d’efficacité en raison du petit nombre de cas dans les études plus petites.
En plus de l’évaluation primaire de l’efficacité, des analyses exploratoires post-hoc ont été ajoutées, notamment une répartition de l’efficacité par intervalle d’amorçage et de rappel et l’efficacité d’une dose unique de vaccin.
Implications de toutes les preuves disponibles
L’analyse principale confirme les conclusions de l’analyse intermédiaire selon lesquelles le vaccin est efficace et sûr.
Des analyses exploratoires montrent qu’une plus grande efficacité du vaccin est obtenue avec un intervalle de rappel plus long et qu’une seule dose de vaccin est efficace au cours des 90 premiers jours, fournissant ainsi une preuve supplémentaire de la politique actuelle.
Les programmes de vaccination visant à vacciner une grande partie de la population avec une dose unique, avec une deuxième dose administrée après une période de 3 mois , pourraient constituer une stratégie efficace pour réduire la maladie et pourraient présenter des avantages par rapport à un programme doté d’une courte fenêtre de déploiement initiale. d’un vaccin pandémique lorsque les approvisionnements sont insuffisants à court terme. Deux doses de ChAdOx1 nCoV-19 se sont révélées efficaces pour prévenir le COVID-19 symptomatique. Ces résultats confirment ceux observés lors de l’analyse intermédiaire des essais. |