Sfondo
Il vaccino ChAdOx1 nCoV-19 (AZD1222) è stato approvato per l’uso di emergenza dall’autorità di regolamentazione del Regno Unito, l’Agenzia di regolamentazione dei medicinali e dei prodotti sanitari, con un regime di due dosi standard somministrate a distanza di 4-12 settimane . L’implementazione prevista nel Regno Unito comporterà la vaccinazione immediata delle persone appartenenti a categorie ad alto rischio con la prima dose e la somministrazione della seconda dose 12 settimane dopo.
Qui, forniamo un’ulteriore analisi combinata prespecificata dei test ChAdOx1 nCoV-19 e analisi esplorative dell’impatto sull’immunogenicità e sull’efficacia dell’estensione dell’intervallo tra le dosi di priming e quelle di richiamo. Inoltre, mostriamo l’immunogenicità e la protezione fornite dalla prima dose , prima che venga offerta una dose di richiamo.
Metodi
Presentiamo i dati di tre studi randomizzati controllati in singolo cieco: uno studio di fase 1/2 nel Regno Unito (COV001), uno studio di fase 2/3 nel Regno Unito (COV002) e uno studio di fase 3 in Brasile (COV003). . e uno studio di fase 1/2 in doppio cieco in Sud Africa (COV005).
Come descritto sopra, gli individui di età pari o superiore a 18 anni sono stati randomizzati 1:1 per ricevere due dosi standard di ChAdOx1 nCoV-19 (5 × 1010 particelle virali) o un vaccino di controllo o un placebo salino. Nello studio britannico, un sottogruppo di partecipanti ha ricevuto una dose inferiore (2 2 × 1010 particelle virali) di ChAdOx1 nCoV-19 per la prima dose.
L’ outcome primario era la malattia COVID-19 sintomatica confermata virologicamente, definita come un test positivo di amplificazione dell’acido nucleico (NAAT) su tampone combinato con almeno un sintomo qualificante (febbre ≥ 378°C, tosse, respiro corto o anosmia o ageusia). più di 14 giorni dopo la seconda dose.
Le analisi di efficacia secondarie includevano casi verificatisi almeno 22 giorni dopo la prima dose. Le risposte anticorpali misurate mediante dosaggio immunologico e mediante neutralizzazione dello pseudovirus erano risultati esplorativi.
Tutti i casi COVID-19 positivi al tampone NAAT sono stati aggiudicati per l’inclusione nell’analisi da un comitato di revisione dei parametri indipendente in cieco.
L’analisi primaria ha incluso tutti i partecipanti che erano sieronegativi per la proteina N SARS-CoV-2 al basale, avevano almeno 14 giorni di follow-up dopo la seconda dose e non avevano evidenza di precedente infezione da SARS-CoV-2. 2 tamponi NAAT.
La sicurezza è stata valutata in tutti i partecipanti che hanno ricevuto almeno una dose. I quattro studi sono registrati con ISRCTN89951424 (COV003) e ClinicalTrials.gov, NCT04324606 (COV001), NCT04400838 (COV002) e NCT04444674 (COV005).
Risultati
Tra il 23 aprile e il 6 dicembre 2020, 24.422 partecipanti sono stati reclutati e vaccinati nei quattro studi, di cui 17.178 sono stati inclusi nell’analisi primaria (8.597 hanno ricevuto ChAdOx1 nCoV-19 e 8.581 hanno ricevuto il vaccino di controllo). Il cut-off dei dati per queste analisi è stato il 7 dicembre 2020. 332 infezioni positive alla NAAT hanno raggiunto l’endpoint primario di infezione sintomatica più di 14 giorni dopo la seconda dose.
L’ efficacia complessiva del vaccino più di 14 giorni dopo la seconda dose è stata del 66% (IC 95%: 57 4-74 0), con 84 casi (10%) negli 8597 partecipanti nel gruppo ChAdOx1 nCoV-19 e 248 ( 2,9%) negli 8581 partecipanti al gruppo di controllo.
Non ci sono stati ricoveri ospedalieri per COVID-19 nel gruppo ChAdOx1 nCoV-19 dopo il periodo di esclusione iniziale di 21 giorni e 15 nel gruppo di controllo. 108 (0,9%) su 12.282 partecipanti nel gruppo ChAdOx1 nCoV-19 e 127 (11%) su 11.962 partecipanti nel gruppo di controllo hanno avuto eventi avversi gravi.
Ci sono stati sette decessi considerati non correlati alla vaccinazione (due nel gruppo ChAdOx1 nCov-19 e cinque nel gruppo di controllo), incluso un decesso correlato a COVID-19 in un partecipante al gruppo di controllo.
Le analisi esplorative hanno mostrato che l’efficacia del vaccino dopo una singola dose standard di vaccino dal giorno 22 al giorno 90 dopo la vaccinazione era del 76,0% (59,3-85,9). La nostra analisi di modellazione ha indicato che la protezione non è diminuita durante questo periodo iniziale di 3 mesi.
Allo stesso modo, i livelli anticorpali sono stati mantenuti durante questo periodo con un calo minimo entro il giorno 90 (rapporto medio geometrico [GMR] 0,66 [IC 95% 0,59-0,74]).
Nei partecipanti che hanno ricevuto due dosi standard, dopo la seconda dose, l’efficacia è stata maggiore in quelli con un intervallo di priming più lungo (efficacia del vaccino 81,3% [IC 95% 60,3-91,2] a ≥ 12 settimane) rispetto a quelli con un intervallo breve (intervallo di vaccinazione efficacia 55,1% [33,0–69,9] in <6 settimane).
Queste osservazioni sono supportate da dati di immunogenicità che hanno mostrato che le risposte anticorpali leganti sono più che raddoppiate dopo un intervallo di 12 o più settimane rispetto a un intervallo inferiore a 6 settimane nei soggetti di età compresa tra 18 e 55 anni (GMR 2 32 [2·01–2· 68]).
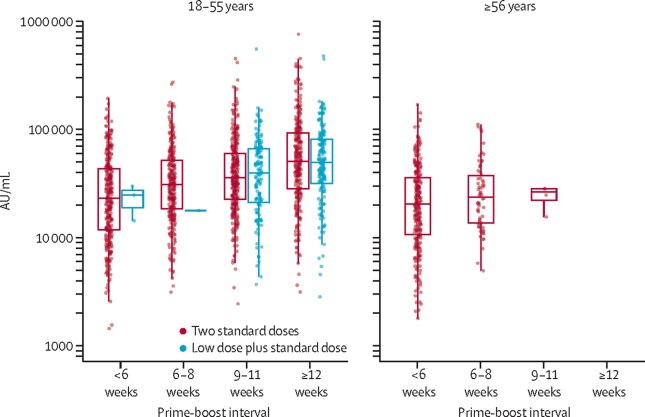
Picco delle risposte IgG anti-SARS-CoV-2 mediante test immunologico multiplex a 28 giorni dopo la seconda dose nei partecipanti che hanno ricevuto due dosi standard o una dose bassa più una dose standard, per intervallo prime-boost (n = 3337)
Interpretazione I risultati di questa analisi primaria di due dosi di ChAdOx1 nCoV-19 erano coerenti con quelli osservati nell’analisi provvisoria degli studi e confermano che il vaccino è efficace, con risultati che variano in base all’intervallo di dose nelle analisi esplorative. Un intervallo di dosaggio di 3 mesi potrebbe presentare vantaggi rispetto a un programma di intervalli di dosaggio brevi per il lancio del vaccino pandemico per proteggere il maggior numero di persone nella popolazione il più rapidamente possibile quando le scorte sono scarse, e allo stesso tempo migliorare la protezione dopo aver ricevuto una seconda dose. |
Ricerca nel contesto
Prove prima di questo studio
Il vaccino ChAdOx1 nCoV-19 (AZD1222) è stato approvato per l’autorizzazione all’uso di emergenza nel Regno Unito sulla base dei risultati provvisori di efficacia di 131 casi di COVID-19 sintomatico primario, con efficacia basata su due dei quattro studi del vaccino. Il lancio previsto del vaccino nel Regno Unito prevede la somministrazione di due dosi a 12 settimane di distanza l’una dall’altra, una politica che ha ricevuto feedback sostanziali.
Valore aggiunto di questo studio
Questo rapporto fornisce risultati aggiornati sull’efficacia primaria dopo un ulteriore mese di raccolta dei dati. Il rapporto provvisorio includeva 131 casi di COVID-19 sintomatico primario. Gli ultimi risultati con ulteriore follow-up includono 332 casi di COVID-19 sintomatico primario. Le stime di efficacia ora includono i dati di tutti e quattro gli studi sul vaccino provenienti da tre paesi, mentre l’analisi provvisoria includeva solo due studi nelle valutazioni di efficacia a causa del numero limitato di casi negli studi più piccoli.
Oltre alla valutazione primaria dell’efficacia, sono state aggiunte analisi esplorative post-hoc, inclusa una ripartizione dell’efficacia per intervallo prime-boost e l’efficacia di una singola dose di vaccino.
Implicazioni di tutte le prove disponibili
L’analisi primaria supporta i risultati riportati nell’analisi intermedia secondo cui il vaccino è efficace e sicuro.
Le analisi esplorative mostrano che una maggiore efficacia del vaccino si ottiene con un intervallo di richiamo più lungo e che una singola dose di vaccino è efficace nei primi 90 giorni, fornendo ulteriori prove per la politica attuale.
I programmi di vaccinazione volti a vaccinare un’ampia percentuale della popolazione con una singola dose, con una seconda dose somministrata dopo un periodo di 3 mesi , potrebbero rappresentare una strategia efficace per ridurre la malattia e potrebbero presentare vantaggi rispetto a un programma con una breve finestra iniziale di implementazione. di un vaccino pandemico quando le scorte scarseggiano a breve termine. Due dosi di ChAdOx1 nCoV-19 si sono rivelate efficaci nel prevenire la comparsa di COVID-19 sintomatico. Questi risultati confermano quelli osservati nell’analisi provvisoria degli studi. |