Sfondo
Il nitazoxanide è ampiamente disponibile ed esercita un’attività antivirale ad ampio spettro in vitro. Tuttavia, non vi è alcuna prova del suo impatto sull’infezione da sindrome respiratoria acuta grave da coronavirus 2 (SARS-CoV-2).
Metodi
In uno studio multicentrico, randomizzato, in doppio cieco, controllato con placebo, sono stati arruolati pazienti adulti che presentavano fino a 3 giorni dopo l’insorgenza dei sintomi della malattia da coronavirus 2019 (COVID-19) (tosse secca, febbre e/o affaticamento).
Dopo la conferma dell’infezione da SARS-CoV-2 mediante PCR con trascrittasi inversa su tampone nasofaringeo, i pazienti sono stati randomizzati 1:1 a ricevere nitazoxanide (500 mg) o placebo, tre volte al giorno, per 5 giorni.
L’outcome primario era la completa risoluzione dei sintomi. Gli esiti secondari erano la carica virale, i test di laboratorio, i biomarcatori sierici di infiammazione e il tasso di ospedalizzazione. Sono stati valutati anche gli eventi avversi.
Risultati
Dall’8 giugno al 20 agosto 2020 sono stati esaminati 1.575 pazienti. Di questi, 392 sono stati analizzati (198 placebo, 194 nitazoxanide). Il tempo mediano (intervallo interquartile) dall’insorgenza dei sintomi alla prima dose del farmaco in studio è stato di 5 (4-5) giorni.
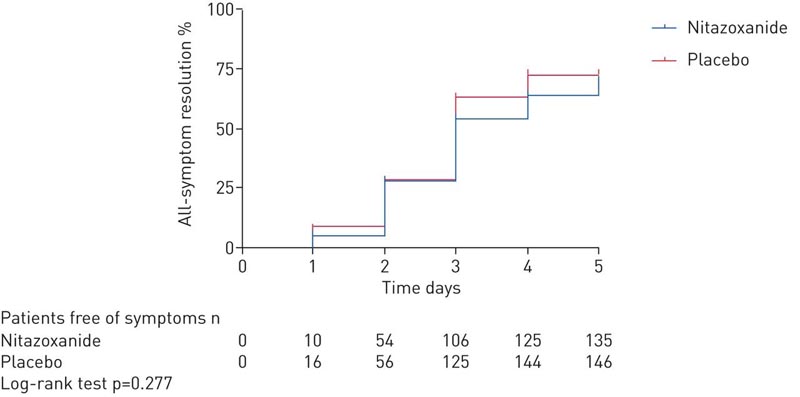
Alla visita di studio di 5 giorni, la risoluzione dei sintomi non differiva tra il braccio nitazoxanide e quello placebo.
I tamponi raccolti erano negativi per SARS-CoV-2 nel 29,9% dei pazienti nel gruppo nitazoxanide rispetto al 18,2% nel gruppo placebo (p = 0,009).
La carica virale è stata ridotta dopo nitazoxanide rispetto al placebo (p = 0,006).
La riduzione percentuale della carica virale dal basale alla fine del trattamento è stata maggiore con nitazoxanide (55%) rispetto al placebo (45%) (p = 0,013).
Altri esiti secondari non erano significativamente differenti. Non sono stati osservati eventi avversi gravi.
Discussione
In questo studio multicentrico, in doppio cieco, randomizzato, controllato con placebo su pazienti con COVID-19 lieve, abbiamo scoperto che la risoluzione dei sintomi (tosse secca, febbre e affaticamento) non differiva tra nitazoxanide e placebo dopo 5 giorni di terapia.
La nitazoxanide si è rivelata sicura, ha ridotto significativamente la carica virale e ha aumentato la percentuale di pazienti risultati negativi al test SARS-CoV-2 dopo 5 giorni di terapia rispetto al placebo. La nitazoxanide non ha impedito il ricovero in ospedale né ha prodotto alcun cambiamento nell’emocromo completo, nei livelli di PCR o nei biomarcatori sierici di infiammazione. Inoltre, il nitazoxanide è poco costoso, ampiamente disponibile e, ad oggi, altre terapie raccomandate non hanno dimostrato di fornire alcun beneficio in questa popolazione.
C’è un urgente bisogno di farmaci farmacoterapeutici basati sull’evidenza per COVID-19. Nel difficile contesto di una pandemia, il riutilizzo dei farmaci può ridurre il lungo processo di sviluppo dei farmaci e consentire una rapida implementazione di terapie efficaci per la popolazione.
Prima dell’implementazione di questo studio, è stata esaminata la biblioteca della National Institutes of Health Clinical Collection, una raccolta di 727 farmaci o composti simili a farmaci approvati dalla Food and Drug Administration (FDA) statunitense con una storia di utilizzo in studi clinici sull’uomo. attività antivirale in vitro contro SARS-CoV-2 (Figura supplementare S1). Nitazoxanide e tizoxanide, il suo metabolita attivo, hanno ridotto significativamente la carica virale in Vero E6, cellule renali embrionali umane (HEK 293T) ed epiteliali polmonari (Calu-3) infettate con SARS-CoV-2, senza indurre la perdita di vitalità cellulare.
Il profilo degli effetti avversi del nitazoxanide è ben noto, poiché è disponibile in commercio e utilizzato clinicamente dal 1996; infatti, in questo studio è stata utilizzata una formulazione commerciale. Un regime posologico di 500 mg ogni 12 ore è approvato e comunemente prescritto per il trattamento della parassitosi intestinale, con pochi eventi avversi segnalati.
Nel nostro studio, è stata somministrata la stessa dose, ma ogni 8 ore, sulla base degli studi farmacologici in vitro del nostro gruppo e dei dati pubblicati sulla concentrazione plasmatica, al fine di massimizzare la potenziale inibizione di SARS-CoV-2 in vivo. Abbiamo ipotizzato che rapporti elevati tra la concentrazione sierica massima a dosi sicure nell’uomo e la concentrazione antivirale massima efficace in vitro si tradurrebbero in un maggiore potenziale per ottenere la soppressione virale alle dosi approvate.
La nitazoxanide non è riuscita a soddisfare l’esito primario nei pazienti con COVID-19 lieve quando valutati dopo 5 giorni di trattamento. Coerentemente con i dati in vitro, abbiamo osservato riduzioni significative della carica virale dopo un ciclo di 5 giorni di nitazoxanide in pazienti con COVID-19 lieve. Questo effetto può avere un impatto epidemiologico, riducendo potenzialmente la diffusione comunitaria di SARS-CoV-2, morbilità e mortalità.
Conclusioni Nei pazienti con COVID-19 lieve, la risoluzione dei sintomi non differiva tra i gruppi nitazoxanide e placebo dopo 5 giorni di trattamento. Tuttavia, la terapia precoce con nitazoxanide si è rivelata sicura e ha ridotto significativamente la carica virale. |