Médecine du Michigan - Université du Michigan
Résumé
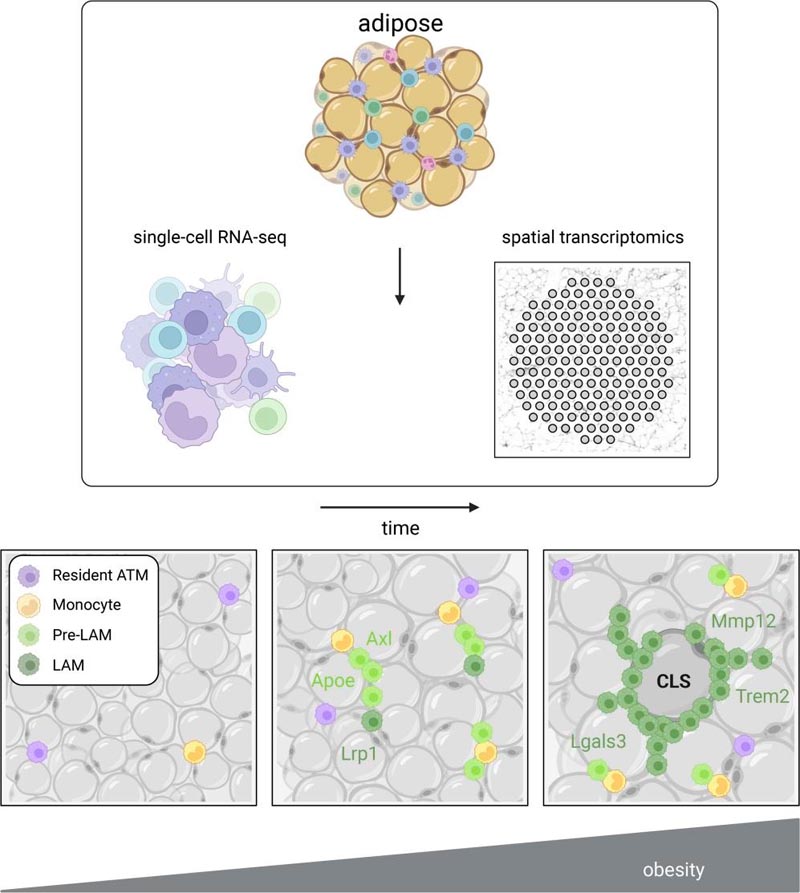
L’infiltration de macrophages du tissu adipeux (ATM) est associée au dysfonctionnement du tissu adipeux et à la résistance à l’insuline chez la souris et l’homme. Des données unicellulaires récentes mettent en évidence une hétérogénéité accrue de l’ATM dans l’obésité, mais ne fournissent pas de contexte spatial pour la dynamique du phénotype ATM. Nous avons intégré l’ARN-Seq unicellulaire, la transcriptomique spatiale et l’imagerie du tissu adipeux murin dans une étude temporelle de l’obésité induite par l’alimentation. Dans l’ensemble, les cellules immunitaires pro-inflammatoires prédominaient dans l’obésité précoce, tandis que les ATM anti-inflammatoires non résidents prédominaient dans l’obésité chronique. Un sous-ensemble de ces ATM anti-inflammatoires étaient intermédiaires sur le plan transcriptomique entre les monocytes et les macrophages matures (LAM) associés aux lipides et étaient cohérents avec un précurseur du LAM (pré-LAM). Les pré-LAM étaient spatialement associés à des structures en forme de couronne (CLS) d’obésité précoce, indiquant un dysfonctionnement du tissu adipeux. Les données spatiales ont montré une colocalisation des transcrits ligand-récepteur liés à la signalisation lipidique entre les monocytes, pré-LAM et LAM, notamment Apoe, Lrp1, Lpl et App. L’expression pré-LAM de ces ligands dans l’obésité précoce suggère une signalisation vers LAM dans le microenvironnement CLS. Nos résultats affinent la compréhension de la diversité des macrophages du tissu adipeux (ATM) et fournissent un aperçu de la dynamique de la lignée LAM au cours du développement des maladies métaboliques. |
commentaires
Le tissu adipeux , même s’il a été vilipendé, est un organe corporel incroyablement complexe et essentiel impliqué, entre autres fonctions, dans le stockage de l’énergie et la production d’hormones. Cependant, les modes de vie modernes ont conduit à une épidémie mondiale d’obésité et à une augmentation correspondante de maladies associées telles que le diabète de type 2 et les maladies cardiovasculaires.
Les chercheurs tentent de découvrir les bases de la structure du tissu adipeux, et plus particulièrement l’ inflammation associée à l’obésité , dans l’espoir de découvrir le lien entre l’accumulation de graisse et de mauvais résultats pour la santé.
Une nouvelle étude menée par Lindsey Muir, Ph.D., doctorant Cooper Stansbury et ses collègues utilise l’analyse unicellulaire de l’expression des gènes combinée à la transcriptomique spatiale pour révéler des types de cellules immunitaires et des interactions jusqu’alors méconnus au sein du tissu adipeux. La transcriptomique spatiale est une technologie plus récente qui capture toute l’expression des gènes dans de petits points d’une fine section entière de tissu.
Étudier la graisse est plus facile à dire qu’à faire. Dans les tissus organisés en couches définies, par exemple la moelle épinière ou le cerveau, « il est plus facile de vérifier ses données et d’identifier telle ou telle couche comme un type cellulaire particulier et de savoir qu’elle doit exprimer les gènes X, Y et Z », a déclaré Muir, professeur adjoint de recherche au Département de médecine computationnelle et de bioinformatique.
"Avec le tissu adipeux, c’est beaucoup plus difficile car les types de cellules sont répartis uniformément dans tout le tissu, sans couches cellulaires définies." En cas d’obésité, les cellules graisseuses ou adipocytes se développent et peuvent atteindre une limite qui finit par provoquer la mort cellulaire et conduire à une inflammation.
Pour mieux comprendre les types de cellules immunitaires dans le tissu adipeux et où elles se rencontrent dans l’obésité, l’équipe a nourri des souris avec un régime riche en graisses pendant 14 semaines, a récolté les tissus adipeux, puis a utilisé des analyses spatiales et unicellulaires pour produire une lecture de tous les ARNm présents dans l’échantillon.
En utilisant un processus informatique connu sous le nom de regroupement sur des données unicellulaires , ils ont pu regrouper des cellules dont la constitution génétique était plus similaire les unes aux autres que les autres groupes ou l’échantillon global.
Ils ont découvert quelque chose de surprenant à propos de la population de macrophages des échantillons , une cellule immunitaire dont le rôle est de nettoyer les cellules mortes et les débris.
"Nous savions que les macrophages auraient probablement plusieurs sous-types, ce qui nous a surpris était le nombre qui émergeait, qui étaient très différents les uns des autres et apparaissaient à des moments différents et devenaient plus dominants au fil du temps."
Ils ont identifié cinq types, qu’ils ont appelés Mac1, 2, 3, 4 et 5. Mac1 résidait dans les tissus de souris maigres suivant un régime alimentaire normal et de souris obèses. Mac2 et Mac3, identifiés par leurs gènes pro-inflammatoires , ont culminé après 8 semaines de régime riche en graisses.
Cependant, à mesure que le régime riche en graisses avançait jusqu’à 14 semaines, les cellules Mac4 et Mac5, qui présentaient une faible expression de gènes pro-inflammatoires, prédominaient, tandis que les cellules pro-inflammatoires Mac2 et Mac3 diminuaient.
« L’idée dans ce domaine était que le type de macrophages qui s’accumulent dans l’obésité favorise un état inflammatoire . Sur la base de ces données, l’histoire est bien plus complexe », a déclaré Muir.
Leur hypothèse est que Mac4 et Mac5 sont les macrophages associés aux lipides (LAM) décrits dans leurs propres travaux antérieurs et par d’autres chercheurs et pourraient indiquer que le corps tente de réprimer un niveau d’inflammation nocif provenant des macrophages pro-inflammatoires et adipocytes mourants. .
Ensuite, une coupe minutieuse de tissus adipeux frais congelés a permis une analyse par transcriptomique spatiale. Chaque point d’analyse de la méthode spatiale possède un code-barres unique qui est attaché à l’ARNm dans le tissu situé au-dessus de ce point, de sorte que l’expression des gènes peut ensuite être cartographiée à des emplacements spécifiques du tissu en utilisant les codes-barres comme coordonnées. Dans cette méthode, les sections sont également imagées juste avant la collecte d’ARNm. L’étude a examiné ces images à la recherche de marqueurs révélateurs appelés structures en forme de couronne , structures associées à la résistance à l’insuline .
"Une fois que les structures en forme de couronne apparaissent, elles mettent beaucoup de temps à disparaître et leur apparition indique un dysfonctionnement des tissus", a déclaré Muir. "En utilisant le traitement d’images, nous avons identifié, sur la base de la densité de ces régions, ce qui serait probablement une structure en forme de couronne, puis vérifié que nous pouvions les voir visuellement", a déclaré Muir. Ces structures avaient une expression génique indiquant la présence de LAM Mac4 et Mac5.
Avec plus d’informations sur la composition cellulaire et l’organisation spatiale du tissu adipeux dans le contexte de l’obésité, la prochaine étape, a déclaré Muir, consiste à examiner les processus de signalisation et les protéines associés au développement de la LAM et des troubles métaboliques.
Conclusions Nos données examinent la compréhension actuelle des changements phénotypiques ATM dans l’obésité. Nous identifions des étapes importantes dans le développement du MN-LAM et fournissons un contexte spatial pour la signalisation myéloïde impliquée dans le dysfonctionnement métabolique . Notre étude apporte des éclaircissements sur les types de cellules et la signalisation impliqués dans la formation et l’accumulation de structures en forme de couronne (CLS), y compris la dynamique spatiale du développement de la LAM dans l’obésité. |
Référence : « Une lignée de macrophages associés aux lipides recâble le paysage spatial du tissu adipeux dans l’obésité précoce », JCI Insight, DOI : /10.1172/jci.insight.171701
















