Riepilogo strutturato
I disturbi neuropsichiatrici e le malattie mentali sono la principale causa di carico di malattie negli Stati Uniti. Decine di migliaia di varianti di sequenza nel genoma umano sono state collegate all’eziologia di queste condizioni. Tuttavia, chiarire il ruolo delle varianti di rischio identificate rimane impegnativo perché la maggior parte di esse si trova al di fuori delle regioni codificanti le proteine e attualmente non dispone di annotazioni funzionali. È probabile che queste varianti di rischio di malattia esercitino la loro influenza perturbando gli elementi regolatori trascrizionali, modulando così l’espressione genica in tipi cellulari rilevanti per i disturbi neuropsichiatrici. I recenti progressi nelle tecnologie unicellulari hanno rivelato un elevato grado di eterogeneità cellulare in tutto il cervello umano. Tuttavia, le sequenze regolatrici trascrizionali che governano l’identità e la funzione di ogni singolo tipo di cellula cerebrale non sono state ancora delineate, ostacolando la nostra capacità di interpretare le varianti di rischio di malattia non codificanti.
Motivo fondamentale
Convenzionalmente, le sequenze regolatrici della trascrizione possono essere determinate dall’evidenza dell’accessibilità della cromatina che tipicamente accompagna il legame del fattore di trascrizione e il rimodellamento della cromatina. Tuttavia, i cataloghi precedenti degli elementi regolatori trascrizionali mancano di informazioni sulle attività specifiche del tipo cellulare di ciascun elemento a causa dell’uso di campioni di tessuto sfuso. I recenti progressi tecnologici ci hanno permesso di analizzare l’accessibilità della cromatina a livello di singola cellula, consentendo la creazione di mappe specifiche del tipo cellulare di elementi regolatori trascrizionali per organi complessi come il cervello umano.
Risultati
In questo studio, presentiamo un’analisi completa dell’accessibilità della cromatina nel cervello umano a livello di singola cellula, che comprende una raccolta di 1,1 milioni di cellule provenienti da 42 distinte regioni cerebrali in tre soggetti adulti neurotipici. Abbiamo utilizzato questo atlante della cromatina per definire 107 tipi distinti di cellule cerebrali e scoperto lo stato di accessibilità della cromatina di 544.735 presunti elementi regolatori trascrizionali in questi tipi di cellule.
Un numero considerevole di questi elementi regolatori hanno mostrato anche conservazione della sequenza e accessibilità della cromatina nelle cellule cerebrali dei topi , sottolineandone l’importanza funzionale. Attraverso l’analisi integrativa, abbiamo collegato molti presunti elementi regolatori trascrizionali a potenziali geni bersaglio. Inoltre, abbiamo sfruttato questo atlante per prevedere i tipi di cellule rilevanti per 19 tratti e disturbi neuropsichiatrici. Infine, abbiamo sviluppato modelli di apprendimento automatico per prevedere la funzione regolatoria delle varianti di rischio della malattia. Abbiamo reso questo atlante disponibile al pubblico gratuitamente attraverso il portale web interattivo CATLAS (www.catlas.org).
Conclusioni L’ atlante della cromatina unicellulare del cervello umano rappresenta una risorsa preziosa per la comunità delle neuroscienze. Fornisce approfondimenti sui programmi di regolazione genetica che modellano la diversità dei tipi di cellule cerebrali e aiuta a interpretare i ruoli funzionali delle varianti di rischio di malattia situate al di fuori delle regioni codificanti le proteine. Questo atlante, in combinazione con altri dati molecolari e anatomici, promette di far progredire la nostra comprensione della funzione cerebrale e della neuropatologia e, in definitiva, offre strade per approcci più efficaci per affrontare i disturbi neuropsichiatrici . |
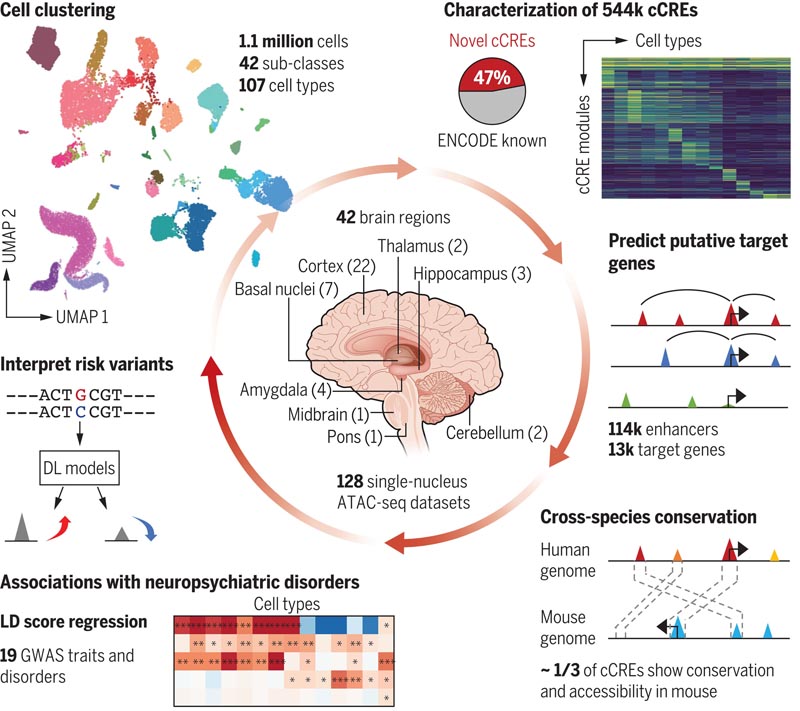
Figura: Analisi di una singola cellula dell’accessibilità della cromatina del cervello umano . Gli elementi candidati cis-regolatori (cCRE) specifici per diversi tipi di cellule cerebrali umane sono stati identificati utilizzando un test single-core per la cromatina accessibile alla trasposasi mediante sequenziamento (snATAC-seq) e collegati a presunti geni bersaglio mediante analisi integrativa. L’uso di cCRE è stato sfruttato per prevedere i tipi di cellule cerebrali rilevanti per tratti e disturbi neuropsichiatrici e per addestrare modelli di apprendimento automatico per interpretare la funzione delle varianti di rischio non codificanti. UMAP, Approccio e Proiezione Multipla Uniforme; DL, apprendimento profondo; LD, disequilibrio del collegamento; GWAS, studio di associazione sull’intero genoma.
Commenti
I ricercatori mappano gli interruttori genetici e i tipi di cellule cerebrali associati alla schizofrenia, al disturbo bipolare, al morbo di Alzheimer e alla depressione maggiore.
In un ampio sforzo multi-istituzionale condotto dall’Università della California, a San Diego, i ricercatori hanno analizzato più di un milione di cellule cerebrali umane per produrre mappe dettagliate degli interruttori genetici nei tipi di cellule cerebrali e hanno rivelato collegamenti tra specifici tipi di cellule e diversi fattori. comune ai disturbi neuropsichiatrici. Il team ha inoltre sviluppato strumenti di intelligenza artificiale per prevedere l’influenza delle singole varianti genetiche ad alto rischio tra queste cellule e il modo in cui potrebbero contribuire alla malattia.
Il nuovo lavoro, pubblicato in un numero speciale di Science , fa parte della Brain Research del National Institutes of Health attraverso l’Advancing Innovative Neurotechnologies Initiative, o BRAIN Initiative, lanciata nel 2014. L’iniziativa mira a rivoluzionare la comprensione del cervello dei mammiferi, in parte, sviluppando nuove neurotecnologie per caratterizzare i tipi di cellule neuronali.
Ogni cellula del cervello umano contiene la stessa sequenza di DNA, ma diversi tipi di cellule utilizzano geni diversi e in quantità diverse. Questa variazione produce molti tipi diversi di cellule cerebrali e contribuisce alla complessità dei circuiti neurali. Imparare come questi tipi di cellule differiscono a livello molecolare è fondamentale per comprendere come funziona il cervello e sviluppare nuovi modi per trattare le malattie neuropsichiatriche.
"Il cervello umano non è omogeneo ", ha detto l’autore senior Bing Ren, PhD, professore alla UC San Diego School of Medicine. "È costituito da una rete estremamente complessa di neuroni e cellule non neuronali, ciascuna delle quali svolge funzioni diverse. La mappatura dei diversi tipi di cellule nel cervello e la comprensione di come lavorano insieme ci aiuterà infine a scoprire nuove terapie che possono colpire ai tipi cellulari individuali rilevanti per malattie specifiche.
Nel nuovo studio, i ricercatori hanno analizzato più di 1,1 milioni di cellule cerebrali in 42 diverse regioni cerebrali di tre cervelli umani. Hanno identificato 107 diversi sottotipi di cellule cerebrali e sono stati in grado di correlare aspetti della loro biologia molecolare con un’ampia gamma di malattie neuropsichiatriche, tra cui la schizofrenia, il disturbo bipolare, il morbo di Alzheimer e la depressione maggiore . I ricercatori utilizzano quindi questi dati per creare modelli di apprendimento automatico per prevedere come determinate variazioni di sequenza nel DNA possano influenzare la regolazione genetica e contribuire alla malattia.
Sebbene questi nuovi risultati offrano importanti informazioni sul cervello umano e sulle sue patologie, gli scienziati sono ancora lontani dall’aver completato la mappatura del cervello. Nel 2022, l’UC San Diego si è unita al Salk Institute e ad altri per lanciare un Centro Atlante Multi-Omico delle cellule cerebrali umane, che mira a studiare le cellule di più di una dozzina di cervelli umani e sollevare domande su come il cervello cambia durante lo sviluppo. durante tutta la vita delle persone e con la malattia.
"Espandere il nostro lavoro a un livello ancora maggiore di dettaglio in un numero maggiore di cervelli ci porterà un passo avanti verso la comprensione della biologia dei disturbi neuropsichiatrici e di come possono essere riabilitati", ha detto Ren.
Gli autori principali dello studio includono: Yang Eric Li, Sebastian Preissl, Michael Miller, Zihan Wang, Henry Jiao, Chenxu Zhu, Zhaoning Wang, Yang Xie, Olivier Poirion, Colin Kern, Lin Lin, Qian Yang, Quan Zhu, Nathan Zemke. , Sarah Espinoza, Jingbo Shang e Allen Wang presso UC San Diego, Nicholas D. Johnson Antonio Pinto-Duarte, Wei Tian Nora Emerson, Julia Osteen, Jacinta Lucero, M. Margarita Behrens e Joseph R. Ecker presso il Salk Institute for Biological Studies , Kimberly Silett e Sten Linnarsson del Karolinksa Institute Anna Marie Yanny, Julie Nyhus, Nick Dee, Tamara Casper, Nadiya Shapovalova, Daniel Hirschstein, Rebecca D. Hodge Trygve Bakken, Boaz Levi e Ed Lein dell’Allen Institute for Brain Sciences and C Dirk Keene presso l’Università di Washington Seattle.
Lo studio è stato sostenuto dal National Institutes of Health (sovvenzioni UM1MH130994, U01MH114812, U54HG012510 e S10 OD026929), dalla National Science Foundation (sovvenzione OIA-2040727); il Nancy and Buster Alford Endowment, la Life Sciences Research Foundation, nonché donazioni di Google, Adobe e Teradata.