Résumé structuré
Les troubles neuropsychiatriques et les maladies mentales constituent la principale cause de morbidité aux États-Unis. Des dizaines de milliers de variantes de séquences dans le génome humain ont été associées à l’ étiologie de ces pathologies. Cependant, élucider le rôle des variantes de risque identifiées reste difficile car la plupart d’entre elles sont situées en dehors des régions codantes pour les protéines et manquent actuellement d’annotation fonctionnelle. Ces variantes de risque de maladie sont susceptibles d’exercer leur influence en perturbant les éléments de régulation transcriptionnelle, modulant ainsi l’expression des gènes dans les types de cellules concernés par les troubles neuropsychiatriques. Les progrès récents dans les technologies unicellulaires ont révélé un degré élevé d’hétérogénéité cellulaire dans l’ensemble du cerveau humain. Cependant, les séquences régulatrices transcriptionnelles qui régissent l’identité et la fonction de chaque type de cellule cérébrale individuelle n’ont pas encore été délimitées, ce qui entrave notre capacité à interpréter les variantes non codantes du risque de maladie.
Raison fondamentale
Classiquement, les séquences régulatrices de la transcription peuvent être déterminées par la preuve de l’accessibilité de la chromatine qui accompagne généralement la liaison du facteur de transcription et le remodelage de la chromatine. Cependant, les catalogues précédents d’éléments régulateurs de la transcription manquent d’informations sur les activités spécifiques au type cellulaire de chaque élément en raison de l’utilisation d’échantillons de tissus en vrac. Les progrès technologiques récents nous ont permis d’analyser l’accessibilité de la chromatine au niveau d’une seule cellule, permettant ainsi la création de cartes spécifiques au type de cellule des éléments de régulation transcriptionnelle pour des organes complexes tels que le cerveau humain.
Résultats
Dans cette étude, nous présentons une analyse complète de l’accessibilité de la chromatine dans le cerveau humain au niveau unicellulaire, englobant une collection de 1,1 million de cellules provenant de 42 régions cérébrales distinctes chez trois sujets adultes neurotypiques. Nous avons utilisé cet atlas de la chromatine pour définir 107 types de cellules cérébrales distinctes et découvert le statut d’accessibilité à la chromatine de 544 735 éléments régulateurs transcriptionnels putatifs dans ces types de cellules.
Un nombre important de ces éléments régulateurs présentaient également une conservation de séquence et une accessibilité à la chromatine dans les cellules cérébrales de souris , soulignant leur importance fonctionnelle. Grâce à une analyse intégrative, nous avons lié de nombreux éléments putatifs de régulation transcriptionnelle à des gènes cibles potentiels. De plus, nous avons exploité cet atlas pour prédire les types de cellules pertinents pour 19 traits et troubles neuropsychiatriques. Enfin, nous avons développé des modèles d’apprentissage automatique pour prédire la fonction régulatrice des variantes du risque de maladie. Nous avons mis cet atlas à la disposition du public gratuitement via le portail Web interactif CATLAS (www.catlas.org).
Conclusions L’ atlas de la chromatine unicellulaire du cerveau humain représente une ressource précieuse pour la communauté des neurosciences. Il fournit des informations sur les programmes de régulation génétique qui façonnent la diversité des types de cellules cérébrales et aide à interpréter les rôles fonctionnels des variantes de risque de maladie situées en dehors des régions codantes pour les protéines. Cet atlas, en combinaison avec d’autres données moléculaires et anatomiques, promet de faire progresser notre compréhension de la fonction cérébrale et de la neuropathologie et, à terme, ouvre la voie à des approches plus efficaces pour traiter les troubles neuropsychiatriques . |
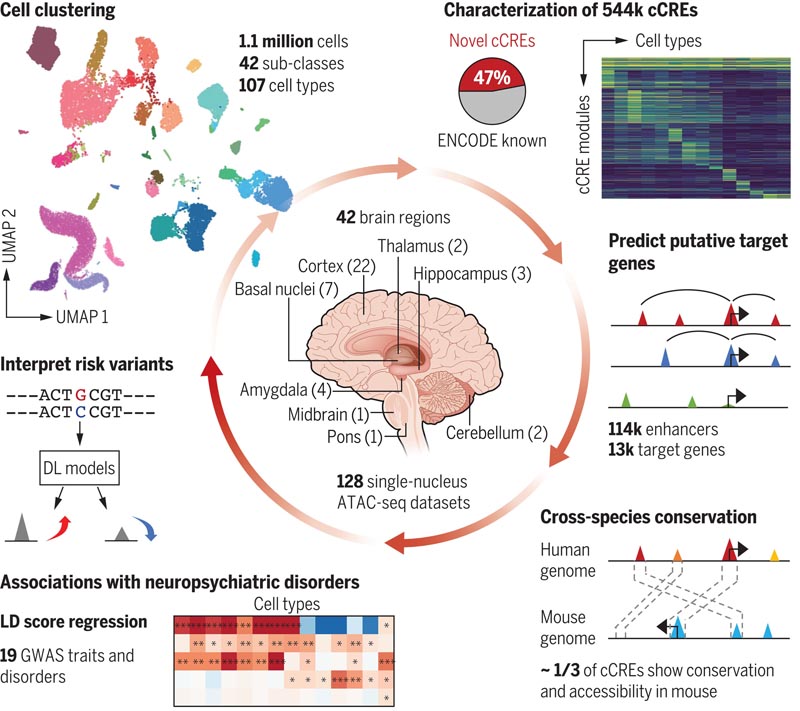
Figure : Analyse unicellulaire de l’accessibilité de la chromatine du cerveau humain . Les éléments cis-régulateurs candidats (cCRE) spécifiques à différents types de cellules cérébrales humaines ont été identifiés à l’aide d’un test monocœur pour la chromatine accessible à la transposase par séquençage (snATAC-seq) et liés à des gènes cibles putatifs par analyse intégrative. L’utilisation du cCRE a été exploitée pour prédire les types de cellules cérébrales pertinentes pour les traits et troubles neuropsychiatriques et pour former des modèles d’apprentissage automatique afin d’interpréter la fonction des variantes de risque non codantes. UMAP, approche et projection uniformes multiples ; DL, apprentissage profond ; LD, déséquilibre de liaison ; GWAS, étude d’association pangénomique.
commentaires
Les chercheurs cartographient les changements génétiques et les types de cellules cérébrales associés à la schizophrénie, au trouble bipolaire, à la maladie d’Alzheimer et à la dépression majeure.
Dans le cadre d’un vaste effort multi-institutionnel dirigé par l’Université de Californie à San Diego, les chercheurs ont analysé plus d’un million de cellules cérébrales humaines pour produire des cartes détaillées des changements génétiques dans les types de cellules cérébrales et ont révélé des liens entre des types de cellules spécifiques et plusieurs facteurs. commun aux troubles neuropsychiatriques. L’équipe a également développé des outils d’intelligence artificielle pour prédire l’influence de variantes génétiques individuelles à haut risque parmi ces cellules et comment elles peuvent contribuer à la maladie.
Le nouveau travail, publié dans un numéro spécial de Science , fait partie de l’initiative de recherche sur le cerveau des National Institutes of Health à travers l’initiative Advancing Innovative Neurotechnologies, ou BRAIN Initiative, lancée en 2014. L’initiative vise à révolutionner la compréhension du cerveau des mammifères, en partie, en développant de nouvelles neurotechnologies pour caractériser les types de cellules neuronales.
Chaque cellule du cerveau humain contient la même séquence d’ADN, mais différents types de cellules utilisent des gènes différents et en quantités différentes. Cette variation produit de nombreux types différents de cellules cérébrales et contribue à la complexité des circuits neuronaux. Apprendre comment ces types de cellules diffèrent au niveau moléculaire est essentiel pour comprendre le fonctionnement du cerveau et développer de nouvelles façons de traiter les maladies neuropsychiatriques.
"Le cerveau humain n’est pas homogène ", a déclaré l’auteur principal Bing Ren, PhD, professeur à la faculté de médecine de l’UC San Diego. "Il est constitué d’un réseau extrêmement complexe de neurones et de cellules non neuronales, dont chacun remplit des fonctions différentes. Cartographier les différents types de cellules du cerveau et comprendre comment elles fonctionnent ensemble nous aidera à terme à découvrir de nouvelles thérapies pouvant cibler à des types de cellules individuelles pertinents pour des maladies spécifiques.
Dans la nouvelle étude, les chercheurs ont analysé plus de 1,1 million de cellules cérébrales dans 42 régions cérébrales différentes de trois cerveaux humains. Ils ont identifié 107 sous-types différents de cellules cérébrales et ont pu établir une corrélation entre certains aspects de leur biologie moléculaire et un large éventail de maladies neuropsychiatriques, notamment la schizophrénie, le trouble bipolaire, la maladie d’Alzheimer et la dépression majeure . Les chercheurs utilisent ensuite ces données pour créer des modèles d’apprentissage automatique afin de prédire comment certaines variations de séquence de l’ADN peuvent influencer la régulation des gènes et contribuer à la maladie.
Même si ces nouveaux résultats offrent des informations importantes sur le cerveau humain et sa pathologie, les scientifiques sont encore loin d’en avoir fini avec la cartographie cérébrale. En 2022, l’UC San Diego a rejoint le Salk Institute et d’autres pour lancer un centre Multi-Omic Atlas des cellules cérébrales humaines, qui vise à étudier les cellules de plus d’une douzaine de cerveaux humains et à soulever des questions sur la façon dont le cerveau change au cours du développement. tout au long de la vie des gens et avec la maladie.
"Élargir notre travail à un niveau de détail encore plus détaillé sur un plus grand nombre de cerveaux nous rapprochera de la compréhension de la biologie des troubles neuropsychiatriques et de la manière dont ils peuvent être réhabilités", a déclaré Ren.
Les principaux auteurs de l’étude sont : Yang Eric Li, Sebastian Preissl, Michael Miller, Zihan Wang, Henry Jiao, Chenxu Zhu, Zhaoning Wang, Yang Xie, Olivier Poirion, Colin Kern, Lin Lin, Qian Yang, Quan Zhu, Nathan Zemke. , Sarah Espinoza, Jingbo Shang et Allen Wang à l’UC San Diego, Nicholas D. Johnson Antonio Pinto-Duarte, Wei Tian Nora Emerson, Julia Osteen, Jacinta Lucero, M. Margarita Behrens et Joseph R. Ecker au Salk Institute for Biological Studies , Kimberly Silett et Sten Linnarsson de l’Institut Karolinksa Anna Marie Yanny, Julie Nyhus, Nick Dee, Tamara Casper, Nadiya Shapovalova, Daniel Hirschstein, Rebecca D. Hodge Trygve Bakken, Boaz Levi et Ed Lein de l’Allen Institute for Brain Sciences and C . Dirk Keene de l’Université de Washington à Seattle.
L’étude a été soutenue par les National Institutes of Health (subventions UM1MH130994, U01MH114812, U54HG012510 et S10 OD026929), la National Science Foundation (subvention OIA-2040727) ; le Nancy and Buster Alford Endowment, la Life Sciences Research Foundation, ainsi que les dons de Google, Adobe et Teradata.