Höhepunkte Welche klinische Frage wird behandelt? Wir untersuchten das Risiko einer leichten kognitiven Beeinträchtigung nach der Diagnose Vorhofflimmern im Vereinigten Königreich. Was ist die wichtigste Erkenntnis? Unsere Studie zeigte, dass Vorhofflimmern (AF) mit einem um 45 % erhöhten Risiko einer leichten kognitiven Beeinträchtigung verbunden war und dass kardiovaskuläre Risikofaktoren und Multikomorbidität offenbar mit diesem Ergebnis verbunden sind. |
Einführung
Eine leichte kognitive Beeinträchtigung (MCI) ist ein frühes Stadium des Rückgangs der kognitiven Funktion, der größer ist als bei gesundem Alter, aber nicht ausreichend ausgeprägt ist, um die Kriterien für Demenz zu erfüllen. Die Ursachen von MCI sind heterogen, und obwohl MCI bei manchen Personen reversibel sein kann, kann sie mit einer jährlichen Konversionsrate von etwa 20 % auf frühe pathologische Prozesse im Zusammenhang mit Demenz zurückzuführen sein.
Faktoren, die mit der Entwicklung oder dem Schutz vor einer leichten kognitiven Beeinträchtigung bei Patienten mit Vorhofflimmern (AF) und der anschließenden Entwicklung einer Demenz verbunden sind, sind nicht vollständig geklärt.
Wir untersuchten den Zusammenhang von Vorhofflimmern mit leichter kognitiver Beeinträchtigung und nachfolgender Demenz anhand von Daten aus routinemäßig erfassten primären elektronischen Gesundheitsakten (EHRs) im Vereinigten Königreich.
Wir haben die in Großbritannien ansässige verknüpfte elektronische Gesundheitsakte (EHR) von 4,3 Millionen Menschen zwischen dem 1. Januar 1998 und dem 31. Mai 2016 verwendet. Alle Personen mit Vorhofflimmern wurden einbezogen und das Indexdatum wurde als Datum der ersten aufgezeichneten Vorhofflimmern-Diagnose definiert .
Für jeden Fall wählten wir zufällig eine Person ohne Vorhofflimmern als Kontrolle aus der Studienkohorte aus, die zum Zeitpunkt der Diagnose dem Geschlecht und Alter der Person mit Vorhofflimmern entsprach.
AF wurde als I48 der International Statistical Classification of Diseases, 10. Revision (ICD-10) und entsprechende Begriffe aus der Clinical Practice Research Datalink Version 2 definiert.
Das primäre Ergebnis der Studie war das Auftreten einer leichten kognitiven Beeinträchtigung, definiert als ICD-10-Codes G31.8 und F06.7 und entsprechende Lesebegriffe.
Die Nachverfolgung endete mit dem Tod, dem Ende der Praxisregistrierung, der Einstellung der Datenbeiträge zum CPRD oder dem Ende des Studienzeitraums.
Wir untersuchten den Zusammenhang zwischen Vorhofflimmern (AF) und leichter kognitiver Beeinträchtigung (MCI) in relevanten Untergruppen, einschließlich Alter bei AF-Diagnose, Geschlecht, sozioökonomischen Kategorien, Schlaganfall und Behandlung mit Digoxin, oralen Antikoagulanzien und Behandlung mit Amiodaron.
Wir untersuchten den Zusammenhang zwischen AF und MCI im Cox-Proportional-Hazards-Modell, das auf konkurrierendes Risiko kontrolliert wurde. Widersprüchliche Ereignisse (z. B. Tod) wurden als zensierte Beobachtungen behandelt . Es wurden Anpassungen vorgenommen für Alter, Geschlecht, Kalenderjahr bei Studienbeginn, sozioökonomischen Status, Rauchen, Bluthochdruck, Diabetes, Fettleibigkeit, Hypercholesterinämie, Hörverlust, Schilddrüsenerkrankung, Depression, atherosklerotische Herzkrankheit, periphere arterielle Verschlusskrankheit, Herzinsuffizienz, Schlaganfall, Krebs, chronische Nierenerkrankung, Lebererkrankung und chronisch obstruktive Lungenerkrankung. Wir haben die gleiche Methode angewendet, um die spätere Inzidenz von Demenz bei Teilnehmern zu untersuchen, die eine MCI entwickelten.
Wir haben Daten von 4.309.245 berechtigten Personen im Vereinigten Königreich analysiert und 233.833 (5,4 %) Personen mit Vorhofflimmern und insgesamt 233.747 ohne Vorhofflimmern identifiziert. Das Durchschnittsalter betrug 74,2 Jahre sowohl bei Patienten mit Vorhofflimmern als auch bei Patienten ohne Vorhofflimmern.
Während einer durchschnittlichen Nachbeobachtungszeit von 5,3 Jahren kam es zu insgesamt 4.269 Zwischenfällen von MCI sowohl bei Patienten mit Vorhofflimmern als auch bei Patienten ohne Vorhofflimmern. Menschen mit Vorhofflimmern hatten ein höheres MCI-Risiko als Menschen ohne Vorhofflimmern, mit einer angepassten HR von 1,45 (95 %-KI: 1,35–1,56).
Zusätzlich zu Vorhofflimmern waren Risikofaktoren wie höheres Alter, weibliches Geschlecht, größere sozioökonomische Deprivation, klinische Vorgeschichte von Depressionen, Schlaganfall und Multimorbidität mit einem erhöhten MCI-Risiko verbunden (Risikoverhältnis zwischen 1,08 (Alter in Jahren) und …). 1,44 (Depressionsgeschichte zu Studienbeginn), alle P < 0,001).
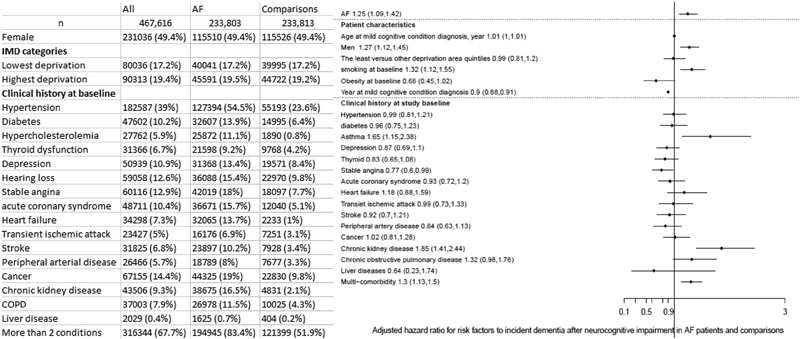
Abbildung 1 Studienpopulation und Risikofaktoren für das Auftreten von Demenz nach der Diagnose einer leichten kognitiven Beeinträchtigung. (Links) Merkmale von Teilnehmern mit Vorhofflimmern und alters- und geschlechtsangepassten Kontrollpersonen; (rechts) Angepasste HR, die mit jedem Risikofaktor für die Inzidenz von Demenz nach MCI-Diagnose verbunden ist. AF = Vorhofflimmern; COPD = chronisch obstruktive Lungenerkrankung; IMD = Index der mehrfachen Deprivation.
Analysen zeigten ähnliche Ergebnisse in der Bevölkerung, geschichtet nach Alter bei Vorhofflimmern-Diagnose, Geschlecht, sozioökonomischer Benachteiligung und Schlaganfallgeschichte. Bei Patienten mit Vorhofflimmern, die eine Digoxin-Behandlung erhielten, bestand kein erhöhtes Risiko einer leichten kognitiven Beeinträchtigung (HR: 0,97, 95 %-KI: 0,53–1,78).
Während das MCI-Risiko bei Patienten mit Vorhofflimmern, die keine Behandlung mit oralen Antikoagulanzien und keine Behandlung mit Amiodaron erhielten, höher war, bestand bei Patienten mit Vorhofflimmern, die eine Behandlung mit oralen Antikoagulanzien und einer Behandlung mit Amiodaron erhielten, kein Risiko für MCI.
Unter den Menschen, die eine MCI entwickelten, gab es im Studienzeitraum 1.117 Demenzdiagnosen während oder nach der MCI-Diagnose . Menschen mit Vorhofflimmern waren auch mit einem erhöhten Risiko für Demenz verbunden, wenn sie MCI entwickelten (mehrfach angepasste HR: 1,25 (95 %-KI: 1,09–1,42). Risikofaktoren, die mit dem Risiko einer Demenz verbunden waren, waren Sex, Rauchen, Asthma und chronische Erkrankungen Nierenerkrankungen und Multikomorbidität.
Unsere Studie zeigte, dass Vorhofflimmern in einer realen, landesweit repräsentativen Kohorte mit einem um 45 % erhöhten MCI-Risiko verbunden war.
Die Ergebnisse zeigten, dass das Alter, eine größere soziodemografische Benachteiligung und eine Schlaganfallgeschichte mit einem erhöhten MCI-Risiko verbunden waren, den Zusammenhang zwischen FA und MCI jedoch nicht veränderten. Sowohl Vorhofflimmern als auch MCI wurden häufig bei Menschen über 74 Jahren diagnostiziert, wenn eine Multikomorbidität vorlag, und wir fanden heraus, dass Diabetes, Hypercholesterinämie, Depression und periphere arterielle Verschlusskrankheit ebenfalls mit einem erhöhten MCI-Risiko verbunden sind.
Der Übergang von einer leichten kognitiven Beeinträchtigung zur Demenz scheint zumindest teilweise durch kardiovaskuläre Risikofaktoren und das Vorhandensein mehrerer Komorbiditäten bedingt zu sein. Stille Schlaganfälle kommen in der VHF-Population häufig vor und wurden früher mit kognitiven Dysfunktionen in Verbindung gebracht.
Einige Einschränkungen müssen anerkannt werden: Wie bei allen Studien zu elektronischen Patientenakten stellt der potenzielle Mangel an Datengranularität und Detaillierungsgrad im Datensatz eine potenzielle Einschränkung dar. Es ist auch notwendig, das Risiko nicht gemessener Risikofaktoren oder Komorbiditäten zu berücksichtigen. Wir hoffen, dieses Problem durch eine detaillierte Charakterisierung der Stichprobe und die Darstellung von 16 häufig assoziierten Komorbiditäten minimiert zu haben. Die Unterberichterstattung über kognitive Beeinträchtigungen aufgrund der Subtilität/Unspezifität der Symptome und der suboptimalen Nutzung kognitiver Tests ist ein Problem für die Forschung auf diesem Gebiet, das auch für EHR festgestellt wurde. 5 Allerdings wurde der ICD-10 bereits früher in Studien zu leichten kognitiven Beeinträchtigungen mit akzeptabler Leistung eingesetzt.
Schließlich wurde bei Menschen mit Vorhofflimmern, die eine Behandlung mit Digoxin oder Amiodaron erhielten , kein erhöhtes Risiko einer leichten kognitiven Beeinträchtigung beobachtet, wobei das Risiko bei diesen Patienten mit dem ihrer Altersgenossen ohne Vorhofflimmern vergleichbar war . Das Beobachtungsdesign dieser Studie und das sehr breite Konfidenzintervall für diese Untergruppen von Patienten (die nur 10–20 % der AF-Stichprobe ausmachen) erlauben es uns jedoch nicht, starke Rückschlüsse auf die Kausalität zu ziehen, eine mögliche Schutzfunktion dieser Medikamente oder nicht gemessene Störfaktoren.
Unsere Ergebnisse betonen den Zusammenhang von Multikomorbidität und kardiovaskulären Risikofaktoren mit der Entwicklung einer leichten kognitiven Beeinträchtigung aufgrund von Vorhofflimmern und dem Fortschreiten der Demenz in der Vorhofflimmerpopulation. Diese Daten stützen die frühere Hypothese einer integrierten Vorhofflimmern-Versorgung (Kombination von Antikoagulation, Symptomen und Komorbiditätsmanagement) als Möglichkeit, kognitiven Verfall und das Fortschreiten zur Demenz zu verhindern, und unterstreichen die Notwendigkeit einer bestätigenden klinischen Studie.
Fußnoten
Die Studie wurde vom unabhängigen wissenschaftlichen Beratungsausschuss der Regulierungsbehörde für Arzneimittel und Gesundheitsprodukte (UK) genehmigt [18_228]. Dr. Chung wird durch die Zuschüsse NIHR131227 und NIHR129463 des National Institute of Health and Care Research (NIHR) unterstützt. Dr. Providencia wird vom University College London British Heart Foundation Research Accelerator AA/18/6/34223 und dem NIHR-Stipendium NIHR129463 unterstützt. Alle anderen Autoren haben angegeben, dass sie keine für den Inhalt dieses Artikels relevanten Beziehungen haben, die sie offenlegen möchten.
















