Résumé Assurer une couverture vaccinale élevée et même une couverture vaccinale de rappel est essentiel pour prévenir la maladie grave à coronavirus 2019 (COVID-19). Parmi les différents vaccins contre la COVID-19 actuellement utilisés, les vaccins à ARNm ont démontré une efficacité notable. Cependant, les événements indésirables (EI) systémiques, tels que la fatigue post-vaccination, sont fréquents après la vaccination par ARNm et leur cause n’est pas connue. Ici, nous avons constaté qu’une expression de base plus élevée des gènes liés à l’épuisement et à la suppression des cellules T et NK était positivement corrélée au développement d’une fatigue modérément sévère après la vaccination avec Pfizer-BioNTech BNT162b2 ; L’expression accrue des gènes associés à l’épuisement et à la suppression des cellules T et NK qui répondaient à la vaccination était associée à des niveaux plus élevés d’activation immunitaire innée un jour après la vaccination. De plus, nous avons constaté, dans un modèle murin, que la modification de la voie de vaccination d’intramusculaire (im) à sous-cutanée (sc) pourrait diminuer la réponse pro-inflammatoire et, par conséquent, l’étendue des EI systémiques ; la réponse immunitaire humorale à la vaccination BNT162b2 n’a pas été compromise. Au lieu de cela, il est possible que la voie sc puisse améliorer les réponses des lymphocytes T CD8 cytotoxiques à la vaccination BNT162b2. Par conséquent, nos résultats donnent un aperçu des bases moléculaires de la fatigue post-vaccination due à la vaccination par ARNm et suggèrent une solution facilement traduisible pour minimiser les événements indésirables systémiques. |
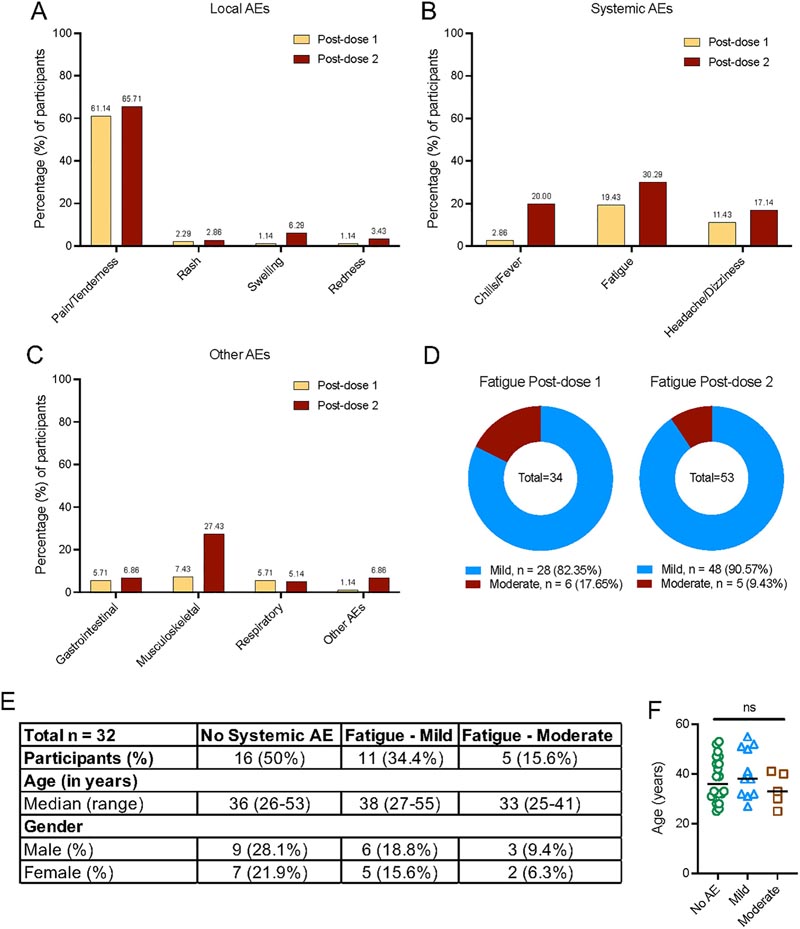
EI locaux et systémiques signalés après la vaccination avec le vaccin Pfizer-BioNTech (BNT162b2) (n = 175). (A) Pourcentage de participants signalant des événements indésirables locaux au site d’injection après les doses 1 et 2 de vaccination. (B) Pourcentage de participants signalant des EI systémiques après les doses 1 et 2 de vaccination. (C) Pourcentage de participants signalant des EI associés à des EI respiratoires, gastro-intestinaux, musculo-squelettiques et autres qui n’appartenaient à aucune catégorie. (D) Pourcentage de participants signalant une fatigue classée par gravité (légère et modérément sévère) après les doses 1 et 2 de vaccination. (E) Données démographiques des participants sélectionnés dans l’étude cas-témoins imbriquée. (F) Âge des participants classés en fonction de la gravité de la fatigue. Les données sous-jacentes à ce chiffre se trouvent dans S1 Data. EI, événement indésirable.
commentaires
Malgré leur forte efficacité contre le SRAS-CoV-2, les vaccins contre la COVID-19 à base d’ARNm sont associés à des effets indésirables post-vaccination tels que la fatigue ; Comment cela peut-il être évité ?
Dans une nouvelle étude publiée dans la revue en libre accès PLOS Biology , Ayesa Syenina de la Duke-NUS Medical School à Singapour et ses collègues rapportent qu’une nouvelle analyse d’échantillons de sang provenant de personnes vaccinées contre le COVID-19 a identifié des caractéristiques moléculaires distinctes liées à une probabilité plus élevée de fatigue post-vaccination. De plus, des expériences sur des souris suggèrent qu’un changement de stratégie d’injection du vaccin pourrait atténuer ces effets indésirables.
Les événements indésirables post-vaccination peuvent influencer la volonté des gens de se faire vacciner ou de recevoir une dose de rappel, entravant ainsi les efforts visant à réduire la propagation et la gravité du COVID-19. Cependant, les fondements moléculaires des événements indésirables consécutifs à la vaccination restent flous.
Pour améliorer la compréhension, Syenina et ses collègues ont analysé des échantillons de sang provenant de 175 agents de santé ayant reçu le BNT162b2, le vaccin Pfizer-BioNTech COVID-19. Plus précisément, ils ont utilisé les échantillons de sang pour analyser un instantané de l’expression génétique de chaque participant, ou quels gènes sont activés ou désactivés.
Cette analyse a révélé que les personnes qui ont ressenti une fatigue modérément sévère après la vaccination étaient plus susceptibles d’avoir une expression de base plus élevée des gènes liés à l’activité des cellules T et des cellules tueuses naturelles, deux types de cellules clés du système immunitaire humain. .
Les chercheurs ont également testé deux stratégies différentes d’injection de vaccins chez la souris. Certaines souris ont reçu le BNT162b2 par injection intramusculaire, la méthode actuellement utilisée pour les patients humains, dans laquelle le vaccin est injecté dans les muscles. D’autres souris ont reçu une injection sous-cutanée , dans laquelle le vaccin est injecté dans le tissu juste sous la peau.
Après la vaccination, par rapport aux souris ayant reçu une vaccination intramusculaire, les souris ayant reçu une vaccination sous-cutanée ont montré des réponses du système immunitaire qui correspondent à une probabilité plus faible d’effets indésirables tels que la fatigue. Toutefois, l’injection sous-cutanée ne semble pas compromettre les effets protecteurs de la vaccination.
Des recherches supplémentaires seront nécessaires pour s’appuyer sur ces résultats et explorer leur signification clinique. Néanmoins, ils améliorent la compréhension de la fatigue post-vaccination et offrent une stratégie potentielle pour réduire sa probabilité.
Le co-auteur Eng Eong Ooi ajoute : « Cette étude fournit le premier aperçu de la base moléculaire d’un effet secondaire que beaucoup ont ressenti après la vaccination par ARNm. « Nous espérons que cette découverte incitera à d’autres études pour comprendre pleinement les mécanismes sous-jacents à l’origine des effets secondaires associés aux vaccins et contribuera collectivement au développement de vaccins encore plus tolérables. »