Riepilogo Garantire un’elevata copertura vaccinale e persino una copertura vaccinale di richiamo è fondamentale per prevenire la grave malattia da coronavirus 2019 (COVID-19). Tra i vari vaccini COVID-19 attualmente in uso, i vaccini mRNA hanno dimostrato una notevole efficacia. Tuttavia, gli eventi avversi sistemici (EA), come l’affaticamento post-vaccinazione, sono comuni dopo la vaccinazione con mRNA e la loro causa non è nota. Qui, abbiamo scoperto che una maggiore espressione basale di geni correlati all’esaurimento e alla soppressione delle cellule T e NK era correlata positivamente con lo sviluppo di affaticamento moderatamente grave dopo la vaccinazione con Pfizer-BioNTech BNT162b2; L’aumento dell’espressione dei geni associati all’esaurimento e alla soppressione delle cellule T e NK che hanno risposto alla vaccinazione è stato associato a livelli più elevati di attivazione immunitaria innata un giorno dopo la vaccinazione. Inoltre, abbiamo scoperto, in un modello murino, che alterare la via di vaccinazione da intramuscolare (im) a sottocutanea (sc) potrebbe diminuire la risposta proinfiammatoria e, di conseguenza, l’entità degli eventi avversi sistemici; la risposta immunitaria umorale alla vaccinazione BNT162b2 non è stata compromessa. Invece, è possibile che la via sc possa migliorare le risposte delle cellule T CD8 citotossiche alla vaccinazione BNT162b2. Pertanto, i nostri risultati forniscono informazioni sulle basi molecolari dell’affaticamento post-vaccinazione derivante dalla vaccinazione con mRNA e suggeriscono una soluzione facilmente traducibile per ridurre al minimo gli eventi avversi sistemici. |
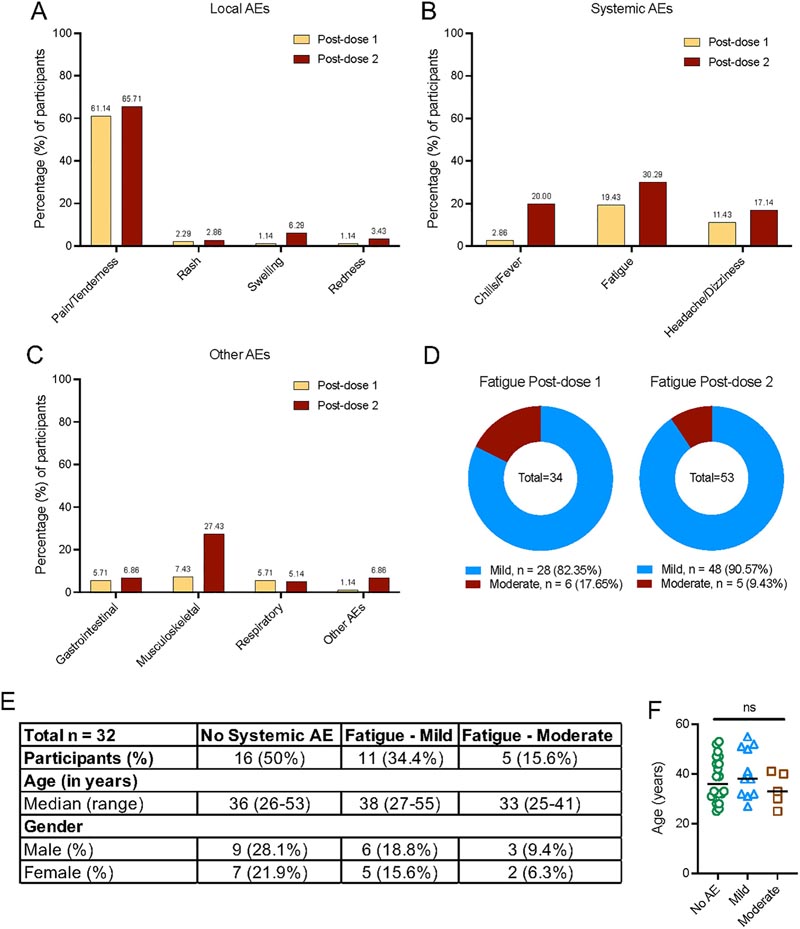
EA locali e sistemici segnalati dopo la vaccinazione con il vaccino Pfizer-BioNTech (BNT162b2) (n = 175). (A) Percentuale di partecipanti che hanno segnalato eventi avversi locali nel sito di iniezione dopo le dosi 1 e 2 di vaccinazione. (B) Percentuale di partecipanti che hanno segnalato eventi avversi sistemici dopo le dosi 1 e 2 di vaccinazione. (C) Percentuale di partecipanti che hanno segnalato eventi avversi associati a eventi avversi respiratori, gastrointestinali, muscoloscheletrici e altri che hanno riferito di non appartenere ad alcuna categoria. (D) Percentuale di partecipanti che riferiscono affaticamento classificato in base alla gravità (lieve e moderatamente grave) dopo le dosi 1 e 2 di vaccinazione. (E) Dati demografici dei partecipanti selezionati nello studio caso-controllo annidato. (F) Età dei partecipanti classificati in base alla gravità della fatica. I dati alla base di questa figura possono essere trovati in S1 Data. AE, evento avverso.
Commenti
Nonostante la loro forte efficacia contro la SARS-CoV-2, i vaccini COVID-19 basati su mRNA sono associati ad effetti avversi post-vaccinazione come l’affaticamento; Come si può evitare questo?
In un nuovo studio pubblicato sulla rivista ad accesso aperto PLOS Biology , Ayesa Syenina della Duke-NUS Medical School di Singapore e colleghi riferiscono che una nuova analisi di campioni di sangue di persone vaccinate contro COVID-19 ha identificato caratteristiche molecolari distinte legate a una maggiore probabilità di stanchezza post-vaccinazione. Inoltre, gli esperimenti sui topi suggeriscono che il cambiamento della strategia di iniezione del vaccino potrebbe alleviare questi effetti avversi.
Gli eventi avversi post-vaccinazione possono influenzare la disponibilità delle persone a vaccinarsi o a ricevere una dose di richiamo, ostacolando gli sforzi volti a ridurre la diffusione e la gravità del COVID-19. Tuttavia, le basi molecolari degli eventi avversi successivi alla vaccinazione non sono chiare.
Per migliorare la comprensione, Syenina e colleghi hanno analizzato campioni di sangue di 175 operatori sanitari che hanno ricevuto BNT162b2, il vaccino Pfizer-BioNTech COVID-19. Nello specifico, hanno utilizzato i campioni di sangue per analizzare un’istantanea dell’espressione genetica di ciascun partecipante o quali geni sono attivati o disattivati.
Questa analisi ha rivelato che le persone che hanno sperimentato un affaticamento moderatamente grave dopo la vaccinazione avevano maggiori probabilità di avere un’espressione di base più elevata di geni legati all’attività delle cellule T e delle cellule natural killer, due tipi di cellule chiave nel sistema immunitario umano. .
I ricercatori hanno anche testato due diverse strategie di iniezione di vaccinazione nei topi. Alcuni topi hanno ricevuto BNT162b2 mediante iniezione intramuscolare, il metodo attualmente utilizzato per i pazienti umani, in cui il vaccino viene iniettato nei muscoli. Altri topi hanno ricevuto un’iniezione sottocutanea , in cui il vaccino viene iniettato nel tessuto appena sotto la pelle.
Dopo la vaccinazione, rispetto ai topi che hanno ricevuto la vaccinazione intramuscolare, i topi che hanno ricevuto la vaccinazione sottocutanea hanno mostrato risposte del sistema immunitario in linea con una minore probabilità di effetti avversi come l’affaticamento. Tuttavia, l’iniezione sottocutanea non sembra compromettere gli effetti protettivi della vaccinazione.
Saranno necessarie ulteriori ricerche per basarsi su questi risultati ed esplorarne il significato clinico. Tuttavia, migliorano la comprensione dell’affaticamento post-vaccinazione e offrono una potenziale strategia per ridurne la probabilità.
Il coautore Eng Eong Ooi aggiunge: “Questo studio fornisce la prima visione delle basi molecolari di un effetto collaterale che molti hanno sperimentato dopo la vaccinazione con mRNA. “Ci auguriamo che questa scoperta possa stimolare ulteriori studi per comprendere appieno i meccanismi alla base degli effetti collaterali associati ai vaccini e contribuire collettivamente allo sviluppo di vaccini ancora più tollerabili”.