Riepilogo Vi sono prove crescenti che la dopamina (DA) funzioni come un regolatore negativo della secrezione di insulina stimolata dal glucosio (GSIS); tuttavia, il meccanismo molecolare sottostante rimane sconosciuto. Utilizzando la microscopia a fluorescenza a riflessione interna totale, abbiamo monitorato l’esocitosi dei granuli di insulina nelle cellule delle isole primarie per analizzare l’effetto della DA. Abbiamo scoperto che gli antagonisti del recettore D1 hanno salvato l’inibizione mediata da DA del flusso di calcio (Ca2+) stimolato dal glucosio, suggerendo un ruolo per D1 nell’inibizione della secrezione di insulina mediata da DA. La sovraespressione di D2, ma non solo di D1, ha esercitato un effetto inibitorio e tossico che ha soppresso l’afflusso di Ca2+ stimolato dal glucosio e la secrezione di insulina nelle cellule beta. La legatura di prossimità e i test Western blot hanno rivelato che D1 e D2 formano eteromeri nelle cellule beta. Il trattamento con un agonista eteromerico D1-D2, SKF83959, ha inibito transitoriamente l’afflusso di Ca2+ indotto dal glucosio e l’esocitosi dei granuli di insulina. La coespressione di D1 e D2 ha consentito alle cellule beta di sfuggire all’effetto tossico della sovraespressione di D2. DA ha inibito transitoriamente il flusso di Ca2+ stimolato dal glucosio e l’esocitosi di insulina attivando l’eteromero D1-D2. Concludiamo che D1 protegge le cellule beta dagli effetti deleteri del DA modulando la segnalazione D2. La scoperta contribuirà alla nostra comprensione della segnalazione del DA nella regolazione della secrezione di insulina e migliorerà i metodi per prevenire e curare il diabete. |
Commenti
Il diabete è una condizione di salute cronica, che dura tutta la vita, causata da anomalie nella produzione e nell’utilizzo dell’ormone insulina nel corpo . La ricerca ha dimostrato che la dopamina (DA), l’ ormone del benessere , svolge un ruolo chiave nel modo in cui il corpo regola la produzione di insulina .
L’insulina viene tipicamente secreta dalle cellule del pancreas chiamate “cellule beta ”, in risposta al glucosio, un processo giustamente chiamato “ secrezione di insulina stimolata dal glucosio ” (GSIS). La dopamina (DA) sottoregola il GSIS, portando a cambiamenti transitori nei livelli di insulina del corpo. Ma il meccanismo alla base di questa regolazione era sconosciuto fino ad ora.
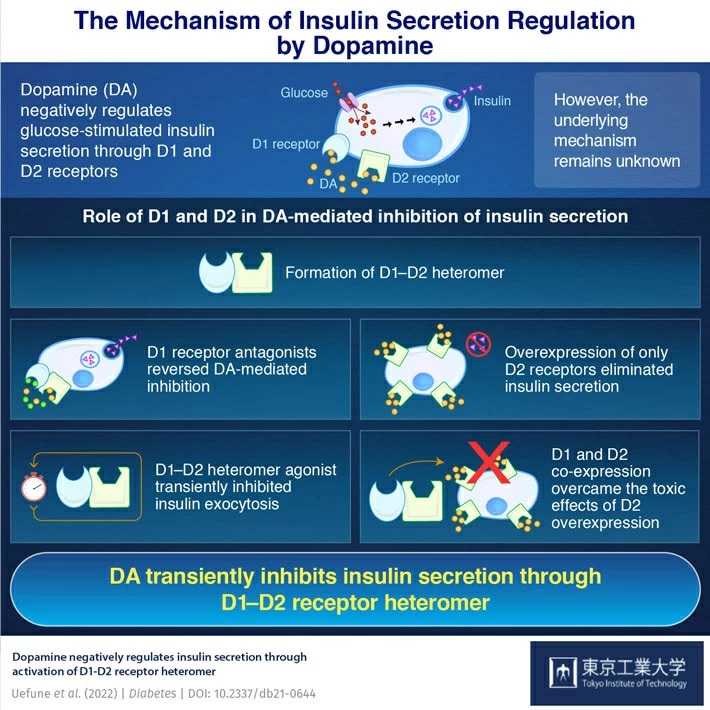
Recentemente, un team guidato da ricercatori del Tokyo Institute of Technology (Tokyo Tech) ha scoperto il meccanismo preciso con cui il DA regola la secrezione di insulina. Usando una tecnica chiamata "microscopia a fluorescenza a riflessione interna totale ", sono stati in grado di rivelare che i "recettori" del DA - proteine nelle cellule a cui il DA può legarsi, chiamate D1 e D2 - agiscono insieme per ottenere una regolazione transitoria dell’insulina.
“Abbiamo scoperto che gli antagonisti dei recettori D1 , i farmaci che bloccano l’attivazione dei recettori D1, diminuiscono l’inibizione della secrezione di insulina mediata dalla dopamina. Abbiamo anche visto che la sovraespressione dei soli recettori D2 nelle cellule beta esercitava un effetto inibitorio e tossico e aboliva la secrezione di insulina nelle cellule beta. Questo ci ha dato un indizio sul meccanismo di downregulation”, spiega il professor Shoen Kume della Tokyo Tech, che ha condotto lo studio.
Il gruppo di ricerca ha quindi eseguito ulteriori esperimenti chiamati “legatura di prossimità” e “saggi Western blot” per studiare ulteriormente i recettori. Hanno scoperto che D1 e D2 si univano per formare un complesso chiamato "eteromero" . Quando attivato dalla DA, questo eteromero inibisce temporaneamente la secrezione di insulina . Hanno anche visto che quando D1 e D2 venivano espressi simultaneamente nelle cellule beta, le cellule riuscivano a sfuggire agli effetti tossici della sovraespressione di D2.
Il dottor Kume afferma: “Da questi risultati, si può concludere che D1 modula la segnalazione D2 per proteggere le cellule beta dagli effetti dannosi del DA. "Questo studio migliora notevolmente la nostra comprensione della segnalazione DA nel diabete."
Comprendere il meccanismo di segnalazione del DA nella regolazione della secrezione di insulina fornirà sicuramente nuovi bersagli terapeutici per la prevenzione, il trattamento e il controllo del diabete.