La sepsi è definita come una disfunzione d’organo pericolosa per la vita causata da una risposta disregolata dell’ospite all’infezione.
In questo contesto, i biomarcatori potrebbero essere considerati indicatori di infezione, risposta disregolata dell’ospite, risposta al trattamento e/o aiutare i medici a prevedere il rischio del paziente.
Nella pratica quotidiana, per la diagnosi e la gestione della sepsi, nonché per la somministrazione di antibiotici, i medici combinano dati provenienti da fonti diverse che risultano dall’intersezione di tre vettori ( Fig. 1 ): manifestazioni sistemiche , disfunzione d’organo e documentazione microbiologica . I biomarcatori potrebbero fornire informazioni aggiuntive sul vettore delle manifestazioni sistemiche (biomarcatori della risposta dell’ospite, ad esempio, proteina C-reattiva-CRP e procalcitonina-PCT), disfunzione d’organo (ad esempio, biomarcatori di danno renale) e documentazione microbiologica ( biomarcatori specifici del patogeno).
Circa il 40-50% dei casi di sepsi sono considerati colturali negativi. I biomarcatori sono stati studiati nel contesto della previsione della sepsi, della diagnosi della sepsi, della valutazione della risposta della sepsi alla terapia e della terapia antibiotica guidata dai biomarcatori. Inoltre, i biomarcatori della sepsi possono essere suddivisi in prognostici, predittivi e teranostici, cioè per guidare la scelta, la dose e la durata della terapia ( Fig. 1 ).
Lo scopo di questa revisione è quello di informare i medici sui biomarcatori di infezione o sepsi e fornire indicazioni sul loro utilizzo, vale a dire biomarcatori patogeno-specifici e due biomarcatori di risposta dell’ospite, PCT e CRP.
Come utilizzare i biomarcatori?
Quando si sospetta la sepsi, il medico ha diverse domande a cui rispondere:
1) Qual è la probabilità di infezione?
2) Qual è la gravità della malattia e il rischio di sviluppare shock settico?
3) Quali sono gli agenti patogeni più probabili?
4) Qual è il trattamento antimicrobico più appropriato?
5) Il paziente sta migliorando o no e, in caso contrario, perché?
6) Quando si può fermare l’uso degli antimicrobici?
I medici spesso cercano di rispondere a queste domande con l’aiuto di biomarcatori, ma è importante riconoscere che la loro performance nella gestione della sepsi non è ottimale.
Biomarcatori patogeno-specifici e di risposta dell’ospite
I biomarcatori sono descritti come una caratteristica biologica, misurata oggettivamente e utilizzata come registrazione surrogata di un processo fisiologico o patologico, o come indicatore dell’attività di un farmaco. Nel presente contesto, i biomarcatori di infezione e sepsi potrebbero essere considerati indicatori di infezione o di risposta disregolata dell’ospite o di risposta al trattamento.
Biomarcatori patogeno-specifici
Sebbene il rilevamento degli acidi nucleici microbici stia diventando sempre più comune, il suo posto nella gestione delle infezioni in generale, e in quelle batteriche in particolare, rimane incerto e non ancora ben standardizzato. I biomarcatori patogeno-specifici, come il test antigenico diretto, sono già ampiamente utilizzati nei pazienti critici.
La maggior parte dei test rapidi basati sull’antigene si basano su test immunocromatografici e possono essere utilizzati al capezzale. Test antigenici respiratori per influenza e SARS-CoV-2 e test antigenici urinari per Streptococcus pneumoniae e Legionella spp. Sono utilizzati nella polmonite acquisita in comunità (CAP). Hanno un’elevata specificità ma una sensibilità da bassa a moderata.
I test dell’antigene della Legionella rilevano il sierogruppo 1 della Legionella pneumophila . Sebbene questa sia la causa predominante della legionellosi, si verificano falsi negativi con altri sierogruppi o specie.
L’infezione da Clostridioides difficile (CDI) può essere diagnosticata in pazienti sintomatici, utilizzando un algoritmo in due fasi con test immunoenzimatici rapidi per analizzare i campioni di feci sia per la glutammato deidrogenasi (GDH) che per le tossine libere A e B. Bassi valori predittivi positivi con una bassa prevalenza di CDI dovrebbe impedire che il test venga utilizzato da solo. Il test GDH è molto sensibile e, se positivo, viene abbinato al test più specifico delle tossine A/B.
I test sugli antigeni fungini prendono di mira i polisaccaridi strutturali derivati dalle pareti cellulari dei funghi. (1,3)-β-D-glucano (BDG) è un biomarcatore sierico panfungineo comunemente utilizzato per rilevare la candidosi invasiva. Con un’elevata sensibilità, ma una bassa specificità, il BDG è uno strumento prezioso per escludere la candidosi invasiva nelle unità di terapia intensiva (ICU) a bassa prevalenza.
Tuttavia, un recente studio clinico randomizzato (RCT) non è riuscito a dimostrare i benefici in termini di sopravvivenza derivanti dall’inizio precoce della terapia antifungina guidata da BDG in pazienti settici critici con rischio da basso a intermedio di candidosi invasiva e al prezzo di un sostanziale uso eccessivo. degli antifungini.
Il galattomannano (GM) può essere misurato in campioni di siero e di lavaggio broncoalveolare (BAL) e mostra un’elevata specificità per la diagnosi di aspergillosi polmonare invasiva (IPA). Da notare che il test BAL fluido GM è più sensibile del test sul siero per diagnosticare l’IPA in pazienti non neutropenici e questo test svolge un ruolo centrale nei criteri diagnostici per l’IPA tra i malati critici.
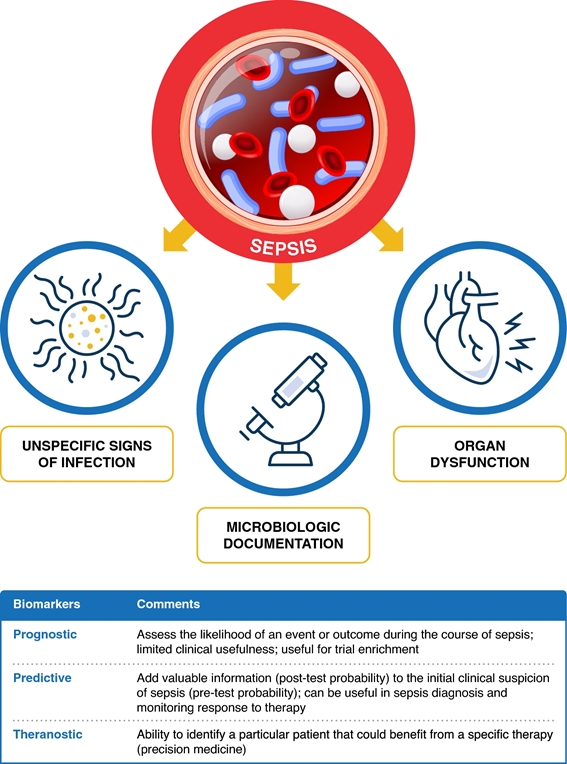
Figura 1. I tre vettori dell’approccio alla sepsi: manifestazioni sistemiche, disfunzione organica e documentazione microbiologica (vedi testo). I biomarcatori potrebbero fornire informazioni aggiuntive sulle manifestazioni sistemiche del vettore (biomarcatori della risposta dell’ospite, ad esempio, proteina C-reattiva-CRP e procalcitonina-PCT), disfunzione d’organo (ad esempio, biomarcatori di danno renale) e documentazione microbiologica (biomarcatori patogeno-specifici). I biomarcatori possono essere classificati come prognostici, predittivi e teranostici.
Biomarcatori della risposta dell’ospite
Nella sezione successiva analizzeremo due biomarcatori della risposta dell’ospite, PCT e CRP.
PROCALCITONINA
La procalcitonina è un proormone precursore della calcitonina. La PCT è prodotta da quasi tutti gli organi e dai macrofagi e i suoi livelli iniziano ad aumentare 3-4 ore dopo uno stimolo infiammatorio, raggiungendo il picco intorno alle 24 ore.
Predizione della sepsi : la PCT è il biomarcatore più studiato nel contesto della polmonite associata al ventilatore (VAP). Gli studi sulla cinetica della PCT in pazienti critici hanno mostrato una scarsa accuratezza diagnostica e un basso impatto per quanto riguarda le indicazioni per l’inizio della terapia. Pertanto, sebbene associata a una diminuzione dell’uso di antibiotici in contesti selezionati, l’utilità della PCT nel predire la sepsi in terapia intensiva è limitata.
Diagnosi di sepsi : gli studi pubblicati non riportavano il valore soglia né utilizzavano valori compresi tra 0,5 e 2 μg/L. Sebbene la PCT possa essere superiore alla CRP nei pazienti con sospetta sepsi, la PCT non dovrebbe essere utilizzata per guidare la prescrizione di antimicrobici. Allo stesso modo, non raccomandano l’uso della PCT per la diagnosi di VAP.
Valutazione della risposta della sepsi alla terapia: nei pazienti con VAP, la PCT misurata al basale e al giorno 4 del trattamento potrebbe predire la sopravvivenza, differenziando i pazienti con esiti buoni e scarsi. Nella pratica clinica, i pazienti che presentano livelli persistentemente elevati di biomarcatori D3/D4 della terapia antibiotica dovrebbero sollevare il sospetto di fallimento del trattamento e dovrebbero indurre una diagnosi e un trattamento aggressivi. Tuttavia, è necessario prestare cautela quando si utilizzano i biomarcatori come criterio indipendente per decidere quando intensificare la diagnosi.
Terapia antibiotica guidata dalla PCT: un approccio sempre più popolare consiste nell’utilizzare biomarcatori per personalizzare la durata del trattamento antibiotico. Questo approccio include la risposta del singolo paziente alla terapia, abbinando la sospensione dell’antibiotico al decorso clinico effettivo del paziente.
Ad oggi, esistono prove evidenti che valutano la terapia antibiotica guidata dalla PCT in pazienti critici, confermando che questa strategia è sicura, è associata a una durata di terapia più breve e, in alcuni studi randomizzati, riduce la mortalità. Tuttavia, le critiche principali riguardavano il fatto che nei controlli dei primi studi la durata della terapia antibiotica era più lunga di quella raccomandata.
PROTEINA C-REATTIVA
La CRP sierica è una proteina della fase acuta sintetizzata esclusivamente nel fegato in risposta alle citochine. I suoi livelli cominciano ad aumentare 4-6 ore dopo uno stimolo infiammatorio e non sono influenzati dall’immunosoppressione (steroidi o neutropenia) o dall’insufficienza renale. o terapia sostitutiva renale e non differisce significativamente tra individui con o senza cirrosi.
Previsione della sepsi : un risultato simile è stato osservato in un ampio studio sulle infezioni del flusso sanguigno acquisite in comunità (BSI) in cui la concentrazione di CRP ha iniziato ad aumentare durante i tre giorni precedenti una diagnosi definitiva.
Diagnosi di sepsi: il valore di una singola determinazione della PCR nei pazienti con sospetta sepsi non è stato dimostrato in modo coerente. Tuttavia, in un recente studio prospettico osservazionale, lo studio CAPTAIN, che ha valutato la prestazione di 53 biomarcatori nel discriminare tra sepsi e sindrome da risposta infiammatoria sistemica non settica (SIRS), è stato riscontrato che nessun biomarcatore o combinazione ha funzionato meglio della CRP. da solo e migliore del PCT.
Valutazione della risposta della sepsi alla terapia: l’ uso delle variazioni relative della CRP (rapporto CRP), il rapporto tra la concentrazione di CRP di ciascun giorno rispetto al livello del giorno 0 (D0), è stato più informativo rispetto alle variazioni assolute del CRP. Una forte diminuzione dell’indice CRP è un indicatore surrogato della risoluzione della sepsi, mentre un indice persistentemente elevato o in aumento suggerisce che la sepsi è refrattaria alla terapia.
Terapia antibiotica guidata dalla PCR: il numero di studi randomizzati che valutano la strategia guidata dalla PCR è limitato, in particolare nei pazienti in terapia intensiva. Studi osservazionali e randomizzati hanno rilevato che la strategia guidata dalla CRP rispetto a quella guidata dalla PCT o dalla durata fissa (breve corso) non presentava differenze sostanziali nella capacità di riflettere il miglioramento (o il peggioramento) nel decorso clinico della sepsi e dello shock. settico e nel ridurre l’esposizione agli antibiotici
La terapia individualizzata consisterebbe nel combinare la durata fissa con la guida dei biomarcatori, utilizzando una strategia del “doppio trigger”. Dopo alcuni giorni di terapia, gli antibiotici potrebbero essere interrotti in base al decorso clinico e alla diminuzione dei livelli di biomarcatori (CRP o PCT), secondo un algoritmo predefinito, o al completamento di 5-7 giorni interi di terapia con antibiotici, a seconda di quale evento si verifichi per primo ( Fig.2 ). Questa strategia individualizzata è stata valutata in diversi studi randomizzati dimostrando che la guida dei biomarcatori può ridurre in modo sicuro la durata della terapia rispetto alla durata fissa.
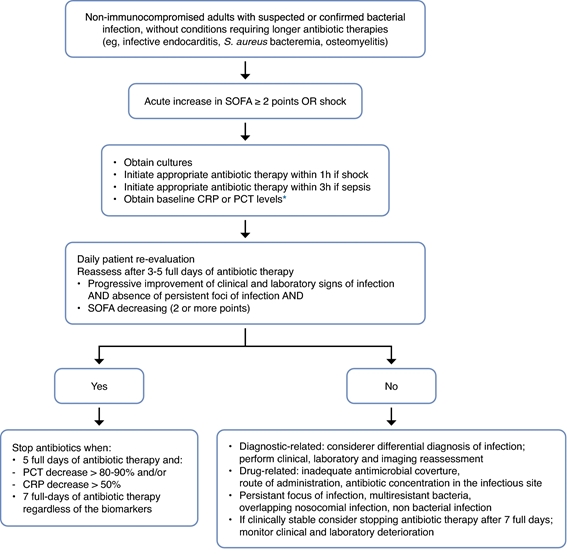
Figura 2. Guida per l’utente per la terapia antibiotica guidata dai biomarcatori. L’inizio della terapia antibiotica nei pazienti critici con sospetta sepsi dovrebbe essere effettuato indipendentemente dal livello di qualsiasi biomarcatore. Ma questo va rivalutato quotidianamente. Utilizzare il decorso clinico, il decorso della disfunzione d’organo (con punteggio SOFA), la cinetica dei biomarcatori e la durata della terapia antibiotica per determinare la durata ottimale della terapia. Queste raccomandazioni non si applicano ai pazienti immunocompromessi o ai pazienti con infezioni che richiedono una terapia antibiotica a lungo termine, come l’endocardite o l’osteomielite.
Prospettive future
La combinazione di più biomarcatori per costruire un pannello diagnostico non ha dimostrato di essere costantemente superiore a qualsiasi singolo biomarcatore nella diagnosi di sepsi. Ciò deriva dal fatto che i biomarcatori della sepsi sono spesso altamente correlati e pertanto l’accuratezza diagnostica non è migliorata quando questi test sono stati combinati.
L’accuratezza diagnostica di un pannello di biomarcatori dipende inoltre da come vengono ponderati i risultati dei singoli test e da quanti devono essere positivi affinché il pannello complessivo indichi la presenza di sepsi. Ad esempio, un pannello di biomarcatori può essere relativamente sensibile (richiedendo che un solo test individuale sia “positivo”) o relativamente specifico (richiedendo che tutti i test individuali siano positivi) a seconda di come viene interpretato il pannello.
Tuttavia, gli algoritmi che combinano biomarcatori con dati clinici si sono mostrati promettenti nell’identificazione dei pazienti con sepsi in pronto soccorso. Uno di questi algoritmi che combina variabili cliniche e un pannello di biomarcatori ha affermato un valore predittivo negativo del 100% e un valore predittivo positivo del 93% in una coorte di 158 pazienti.
Conclusioni Passare da dove siamo attualmente con i biomarcatori della sepsi a un punto in cui disponiamo di marcatori clinicamente utili che guidano i percorsi di trattamento dei pazienti per migliorare i risultati richiederà un cambiamento significativo nell’approccio. È improbabile che gli studi unidimensionali condotti da un singolo centro portino grandi progressi. Ciò che serve sono ampi studi di coorte multicentrici che utilizzino algoritmi all’avanguardia per identificare biomarcatori che predicono risposte differenziali agli interventi in endotipi clinici specifici. La combinazione degli strumenti esistenti in collaborazioni multicentriche e multidisciplinari sarà il modo più efficace per scoprire nuovi biomarcatori che possono essere implementati nella pratica clinica per ottimizzare la cura del paziente. Fino ad allora, i biomarcatori della sepsi potrebbero essere utili strumenti complementari quando i medici necessitano di ulteriori informazioni per ottimizzare la cura del paziente al letto del paziente. Le determinazioni seriali sono più informative di un singolo valore e i biomarcatori non dovrebbero mai essere utilizzati come test autonomo, ma sempre insieme a una valutazione clinica approfondita. |
















