Höhepunkte
|
Zusammenfassung
Psychosozialer Stress hat tiefgreifende Auswirkungen auf das Wohlbefinden und die Gesundheit. Die Stressreaktion wird in erster Linie mit der Amygdala in Verbindung gebracht, einer entscheidenden Struktur des Angstabwehrsystems, die für die soziale Wahrnehmung und Emotionsregulation unerlässlich ist. Aktuelle Neuroimaging-Studien haben gezeigt, wie eine erhöhte Stoffwechselaktivität der Amygdala Entzündungen verstärkt und zu kardiometabolischen Erkrankungen führt.
Die Entwicklung therapeutischer Strategien hängt von unserem Verständnis der Faktoren ab, die das Angstabwehrsystem aktivieren, und der nachgeschalteten molekularen Mechanismen, die emotionalen Stress in Zellschäden umwandeln. Angst vor Emotionen als Folge eines Bindungstraumas ist der wichtigste Auslöser der maladaptiven Aktivierung des Angstabwehrsystems. Die zentralen molekularen Wege sind eine verstärkte Myelopoese und eine hochregulierte proinflammatorische Genexpression, Glukokortikoid- und Insulinresistenz sowie oxidativer Stress.
Therapeutische Strategien können von ganzheitlichen Ansätzen profitieren. Eine Psychotherapie kann die maladaptiv erhöhte Aktivierung des Angstabwehrsystems reduzieren. Biologische Eingriffe können die schädlichen Auswirkungen von oxidativem Stress auf den Körper abfedern.
Einführung
Es ist allgemein bekannt, dass psychischer Stress gesundheitsschädlich ist und es ist bekannt, dass Menschen mit psychischen Störungen ein erhöhtes Risiko für die Entwicklung von Herz-Kreislauf-Erkrankungen und eine deutlich verkürzte Lebenserwartung haben. Diese Übersicht wird zeigen, dass psychischer Stress durch die maladaptive Aktivierung des Angstabwehrsystems verursacht wird und die Rolle von Emotionen, die das wichtigste angeborene Motivations- und Regulierungssystem des Menschen sind, in diesem Prozess hervorheben.
- Zunächst geben wir einen Überblick über das Angstabwehrsystem und die zentrale Rolle der Amygdala .
- Zweitens beschreiben wir, wie die Aktivierung des Angstabwehrsystems zu Entzündungen führt .
- Drittens zeigen wir die wichtigsten Auslöser des Angstabwehrsystems auf.
- Viertens beschreiben wir die Wege von der Amygdala-Aktivierung bis hin zu oxidativem Stress .
- Fünftens kartieren wir die klinischen und sozialen Implikationen.
Die Amygdala und das Angstabwehrsystem
Das Angstabwehrsystem ist ein angeborenes System, das arttypische Abwehrreaktionen organisiert, die fest verdrahtet sind, um auf Bedrohungen zu reagieren, die das Überleben fördern. Die Aktivierung des Abwehrverhaltens beginnt mit einer Erregungsreaktion, die von der Amygdala verarbeitet wird und ohne bewusste Wahrnehmung abläuft. Die bewusste Wahrnehmung dieser Reaktion ist das Angstgefühl (zum Beispiel Muskelverspannungen im Nacken, Schwitzen, erhöhter Herzschlag, Hyperventilation, Gefäßkrämpfe bei kalten Händen).
Die Muster der Abwehrreaktionen können wie folgt klassifiziert werden:
Kampf oder Flucht stellen aktive Reaktionen dar (beim Menschen zum Beispiel wütend werden und reden oder sich unterwerfen).
Einfrieren ist ein Zustand aufmerksamer Unbeweglichkeit, der es dem Säugetier ermöglicht, die Umgebung zu scannen und Kampf- oder Fluchtreaktionen vorzubereiten (z. B. ein Zustand erhöhter Wachsamkeit mit aktiviertem, angespanntem Körper). In Situationen unausweichlicher Bedrohung reagieren Säugetiere mit tonischer Unbeweglichkeit . Diese Endabwehr hat die Funktion, den Killerreflex des Raubtiers zu deaktivieren, wenn das Säugetier gefangen wurde.
Beim Menschen ist diese Abwehr durch Erfahrungen von Taubheit, Angst, Wahrnehmungsverzerrungen wie Derealisation und Depersonalisierung sowie Hoffnungslosigkeit gekennzeichnet. Eine ähnliche Abwehrreaktion ist die kollabierte Immobilität (beim Menschen beispielsweise angstbedingte Ohnmacht aufgrund einer zerebralen Hypoxie).
Die letzte Reaktion ist inaktive Immobilität , die nach Phasen akuten Stresses auftritt, wenn das Säugetier in eine sichere Umgebung zurückgekehrt ist und der Erholung dient. Diese Abwehrreaktion ist der zugrunde liegende Gehirnmechanismus klinischer Zustände wie chronischen Schmerzsyndromen oder anhaltender Erschöpfung .
Diese Abwehrreaktionen erfolgen über spezifische neurohumorale Bahnen, zu denen die Amygdala, der Hypothalamus, das periaquäduktale Grau sowie die sympathischen und vagalen Kerne gehören.
Fehlanpassungen des Angstabwehrsystems und dysregulierte Angst bilden die psychophysiologischen Grundlagen häufiger psychischer Störungen.
Auslöser des Angstabwehrsystems und die Rolle von Emotionen
Angeborene Reize oder äußere Bedrohungen können das Angstabwehrsystem auslösen. Beim Menschen stellt beispielsweise die Einwirkung von Lärm oder aversiven Hörreizen einen natürlichen Reiz dar, der die Amygdala aktiviert.
Die Belastung durch psychosoziale Stressfaktoren, etwa in armen und einkommensschwachen Wohngebieten, ist eine allgegenwärtige äußere Bedrohung, die das Angstabwehrsystem aktiviert und schädliche Auswirkungen auf die Gesundheit und das Überleben hat.
Beim Menschen sind jedoch erfahrungsabhängige Auslöser für die Aktivierung des Angstabwehrsystems von besonderer Bedeutung. Der zugrunde liegende Mechanismus wird Pawlowsche Abwehr oder Angstkonditionierung genannt : Unbedeutende Reize werden zu Bedrohungssignalen, wenn sie neben biologisch bedeutsamen Bedrohungen auftreten.
Beim Menschen ist die Gehirnentwicklung stärker als bei anderen Spezies verlängert, um eine optimale Anpassung durch den Erwerb komplexer Verhaltensweisen zu ermöglichen. Bindungserfahrungen mit den Eltern spielen eine entscheidende Rolle beim Erwerb komplexer kognitiver und affektiver Verhaltensweisen und spielen eine einzigartige Rolle bei der Angstkonditionierung.
Daher sind frühe Widrigkeiten der Bezugsperson wie Missbrauch (körperlich, emotional, sexuell) oder Vernachlässigung der emotionalen Bedürfnisse des Babys (z. B. aufgrund psychischer Störungen der Eltern oder früher Verluste der Bezugsperson oder sozialer Widrigkeiten) sehr starke Stressfaktoren für die neurologische Entwicklung.
Diese Effekte werden insbesondere von der Amygdala und dem medialen präfrontalen Kortex (mPFC) verarbeitet. Der mPFC ist eine Gehirnstruktur, die für die soziale Wahrnehmung und die Regulierung von Emotionen und Verhalten wichtig ist.
Während der menschlichen Entwicklung bilden Amygdala und mPFC vielfältige Verbindungen. Tatsächlich sind sichere Bindungserfahrungen im Säuglingsalter im Vergleich zu unsicheren Bindungserfahrungen mit einer adaptiveren Reifung der Amygdala-mPFC-Konnektivität und kleineren Amygdala-Volumina verbunden.
Ein Bindungstrauma sagt ein größeres Amygdala-Volumen im Erwachsenenalter voraus und führt zu einer stärkeren Reaktion der Amygdala auf hervorstechende Reize. In diesem Zusammenhang ist es wichtig zu erkennen, dass die Bindungsbeziehung zwischen Babys und Eltern durch Grundemotionen wie Glück, Traurigkeit, Wut, Ekel, Überraschung und Angst reguliert wird.
Emotionen sind das wichtigste Motivationssystem des Menschen.
Babys, die nicht sprechen können, kommunizieren mit ihren Eltern durch den Ausdruck ihrer Gefühle. Emotionen sind intra- und zwischenmenschliche Regulatoren. Wut löst beispielsweise ein selbstbejahendes Verhalten des Babys gegenüber den Eltern aus . Die adaptiven Reaktionen der Eltern gegenüber dem wütenden Säugling erhöhen die Selbstwirksamkeit und das Vertrauen des Säuglings in die Bezugsperson.
Allerdings kann die Reaktion der Eltern auch zu einer Angstkonditionierung der Emotion „Wut“ führen . Stellen Sie sich vor, dass die Eltern mit Angst reagieren oder dem Säugling Angst machen, indem sie aggressiv werden oder sich zurückziehen. Dann wird das Gefühl der Wut zu einem Bedrohungssignal für den Säugling.
Aufgrund der immensen Abhängigkeit von der Bezugsperson besteht das wichtigste Motiv des Babys darin, die Bindung zum Vater aufrechtzuerhalten und jedes Verhalten zu vermeiden, das die Bindung zum Vater gefährden könnte. Psychische Störungen sind die Folge solcher erlernter affektiver Phobien und der Vermeidung oder Abwehr solcher Emotionen im Erwachsenenalter.
Da Emotionen das grundlegende Motivationssystem des Menschen sind, haben konditionierte Angst vor Emotionen und die Abwehr von Gefühlen einen tiefgreifenden Einfluss auf die Identitätsentwicklung, Selbstregulierung und zwischenmenschliche Fähigkeiten.
Ein entscheidender Indikator für die psychische Gesundheit ist daher die Fähigkeit, die gesamte Bandbreite an Emotionen adaptiv zu erleben und auszudrücken.
Es ist wichtig zu beachten, dass viele ungesunde Verhaltensweisen, beispielsweise Rauchen, eine Möglichkeit zur Bewältigung von Fehlanpassungen darstellen, indem das Angstabwehrsystem aktiviert wird.
Aktivierung und Entzündung der Mandel
Aktuelle bildgebende Untersuchungen zeigten erstmals, wie die Aktivierung des auf der Amygdala basierenden Angstabwehrsystems zu somatischen Erkrankungen führt.
In der ersten Studie haben Tawakol et al. (2017) zeigten mithilfe der 18F-Fluordesoxyglucose-Positronenemissionstomographie, dass eine erhöhte Stoffwechselaktivität der Amygdala die unabhängige und robuste Entwicklung von Arteriosklerose und Herz-Kreislauf-Erkrankungen vorhersagte .
Die Stoffwechselaktivität der Amygdala korrelierte außerdem mit dem selbstberichteten Stressniveau, und wahrgenommener Stress war mit Entzündungsmaßen verbunden. Erhöhte Stoffwechselaktivität der Tonsillen, hervorgerufen durch die Bahnen des sympathischen Nervensystems, Aktivierung des Knochenmarks und damit erhöhte Freisetzung von Entzündungszellen als Folge einer erhöhten Gefäßentzündung.
Die gleichen Wege wurden in einer Stichprobe von Patienten mit Psoriasis , einer chronisch entzündlichen Hauterkrankung , aufgeklärt : Eine erhöhte Stoffwechselaktivität der Amygdala führte zu einer Aktivierung des hämatopoetischen Systems mit einer erhöhten Freisetzung aktivierter Monozyten, die Entzündungen und Arteriosklerose stimulieren.
Andere Neuroimaging-Studien zeigten, dass die Amygdala-Aktivität mit basaler viszeraler Adipositas sowie mit einer Zunahme der viszeralen Adipositas und der Entwicklung eines adipositasunabhängigen Diabetes mellitus verbunden war. Auch hier wurden diese gesundheitsschädlichen Auswirkungen hauptsächlich durch einen Anstieg der proinflammatorischen Leukopoese verursacht , der durch die Aktivierung des Angstabwehrsystems hervorgerufen wurde.
Amygdala-Aktivierung und oxidativer Stress
Die neurochemische Kaskade, die durch maladaptive Aktivierung des Amygdala-bezogenen Angstabwehrsystems induziert wird, kann langfristige Folgen wie Entzündungen, Arteriosklerose, Veränderungen der Insulinsensitivität und Herz-Kreislauf-Erkrankungen haben. Eine chronische Aktivierung der Amygdala führt zur Aktivierung des sympathischen Nervensystems (SNS) und der Hypothalamus-Hypophysen-Nebennieren-Achse (HPA) (Abb. 1).
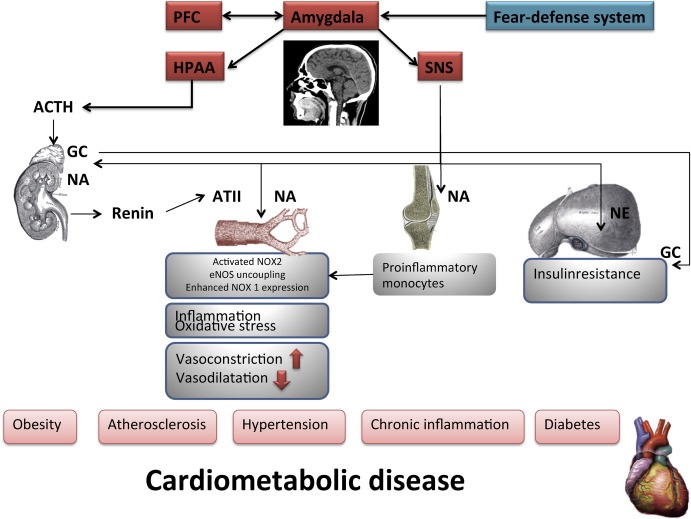 Abbildung 1. Die chronische Aktivierung der Amygdala führt zur Aktivierung der Hypothalamus-Hypophysen-Nebennieren-Achse (HPA) sowie zur Aktivierung des sympathischen Nervensystems (SNS). Die Aktivierung von SNS führt zur Reninsekretion und Freisetzung von Angiotensin II (ATII). ATII aktiviert NOX2 (NADPH-Oxidase 2) in Endothelzellen, was zu oxidativem Stress führt. Dies kann zur Entkopplung der endothelialen Stickstoffmonoxid-Synthetase (eNOS) führen. Oxidativer Stress in Endothelzellen aktiviert NF-kB (Kernfaktor-K-Leichtketten-Verstärker aktivierter B-Zellen), was zur Induktion von Adhäsionsmolekülen führt, die zu Gefäßentzündungen führen. Die HPA-Achse wird durch CRF (Corticotropin-Releasing-Faktor), ACTH (adrenocorticotropes Hormon) und Kortikosteroide vermittelt. Bei Stimulation setzt die HPA-Achse schnell Glukokortikoide (GCs) frei. GC steigert die NOX1-Expression (NADPH-Oxidase 1) in Gefäßmuskelzellen. GC und NA (Noradrenalin) können zu einer verminderten Insulinsensitivität führen. Das Schema wurde teilweise von Li et al. übernommen. Br J Pharmacol. 2019 (Li, Kigallen und Münzel, 2019).
Abbildung 1. Die chronische Aktivierung der Amygdala führt zur Aktivierung der Hypothalamus-Hypophysen-Nebennieren-Achse (HPA) sowie zur Aktivierung des sympathischen Nervensystems (SNS). Die Aktivierung von SNS führt zur Reninsekretion und Freisetzung von Angiotensin II (ATII). ATII aktiviert NOX2 (NADPH-Oxidase 2) in Endothelzellen, was zu oxidativem Stress führt. Dies kann zur Entkopplung der endothelialen Stickstoffmonoxid-Synthetase (eNOS) führen. Oxidativer Stress in Endothelzellen aktiviert NF-kB (Kernfaktor-K-Leichtketten-Verstärker aktivierter B-Zellen), was zur Induktion von Adhäsionsmolekülen führt, die zu Gefäßentzündungen führen. Die HPA-Achse wird durch CRF (Corticotropin-Releasing-Faktor), ACTH (adrenocorticotropes Hormon) und Kortikosteroide vermittelt. Bei Stimulation setzt die HPA-Achse schnell Glukokortikoide (GCs) frei. GC steigert die NOX1-Expression (NADPH-Oxidase 1) in Gefäßmuskelzellen. GC und NA (Noradrenalin) können zu einer verminderten Insulinsensitivität führen. Das Schema wurde teilweise von Li et al. übernommen. Br J Pharmacol. 2019 (Li, Kigallen und Münzel, 2019).
Das sympathische Nervensystem, oxidativer Stress und proinflammatorische Monozyten
Aktivierung des SNS bei der schnellen Freisetzung von Adrenalin und Noradrenalin, hauptsächlich durch das Nebennierenmark. Das SNS stimuliert die Reninsekretion und die Produktion von Angiotensin II (ATII). NADPH-Oxidase (NOX2) in Endothelzellen wird durch ATII aktiviert, was zu oxidativem Stress führt.
Der Begriff oxidativer Stress wird allgemein als ein Überschuss an prooxidativen Faktoren, reaktiven Sauerstoffspezies (ROS) und reaktiven Stickstoffspezies (RNS) gegenüber Antioxidantien definiert. Hohe Konzentrationen an ROS und RNS sowie eine geringe antioxidative Kapazität können verschiedene Zellkomponenten schädigen. Die Folge ist eine schwere zelluläre Belastung mit beeinträchtigter Zellfunktion und Zelltod.
Aktiviertes NOX2 kann die Entkopplung der endothelialen Stickstoffoxidase (eNOS) induzieren. Die Entkopplung von eNOS führt zu einer verringerten NO-Produktion. Darüber hinaus steigert Noradrenalin die NOX-Expression und fördert die Adhäsion von Immunzellen an der Gefäßwand. Die Infiltration von Immunzellen verursacht vaskulären oxidativen Stress durch NOX2-Aktivität.
Darüber hinaus aktiviert die ROS-Signalübertragung Transkriptionsfaktoren, was zur Expression mehrerer Gene führt, die an der tumorsuppressiven und antioxidativen Wirkung beteiligt sind. Beispielsweise kann die ROS-Signalübertragung die Expression des Kernfaktors Kappa B (NF-κB) verstärken [33]. NF-κB reguliert die Expression von fast 500 verschiedenen Genen, darunter Enzyme, zum Beispiel induzierbare NO-Synthase (iNOS), Zytokine und Tumornekrosefaktor (TNF) [59].
NF-κB kann vorübergehend durch verschiedene Reize aktiviert werden, wie z. B. akute Exposition gegenüber Alkohol, Zigarettenrauch, physiologischer Stress, aber auch durch mentalen Stress, der bei Mäusen neuroinflammatorische Reaktionen hervorruft [1,69], was einen „ Stresssensor“ darstellt .
Die SNS-Aktivierung steigert die Monozytopoese im Knochenmark, was zur Expansion entzündungsfördernder Monozyten führt . Darüber hinaus führt eine chronische Entzündung zu einer Veränderung der hämatopoetischen Topographie vom Knochenmark bis zur Milz. Die Migration hämatopoetischer Vorläuferzellen vom Knochenmark in die Peripherie trägt zu einer erhöhten Leukozytenproduktion bei.
Immer mehr Daten deuten darauf hin, dass psychosozialer Stress und ein ungesunder Lebensstil die Verdrängung hämatopoetischer Stammzellen und die Freisetzung von Vorläuferzellen aus dem Knochenmark in die Peripherie auslösen.
Darüber hinaus verringerte eine erhöhte Aktivität des sympathischen Nervensystems die Expression des CXC-Chemokins 12 (CXCL12) in der Nische der hämatopoetischen Stammzellen und steigerte die Neutrophilen- und Monozytenproduktion bei stressexponierten Mäusen. Dies führte zu einer umfassenden Freisetzung entzündlicher Leukozyten in den Kreislauf und förderte die Entzündung atherosklerotischer Plaques.
Die HPA-Achse und Glukokortikoide
Die HPA-Achsen-Kaskade ist äußerst wirksam bei der Aufrechterhaltung der Allostase und der Anpassung an Stressreize.
Bei Depressionen ist die Aktivität der HPA-Achse mit Hyperkortisolämie und verminderter inhibitorischer Rückkopplung verbunden. Bei Einzelgängern ist die Aktivierung der HPA-Achse ein ständiger Befund. Die HPA-Achse wird durch den Corticotropin-Releasing-Faktor (CRF) und das adrenocorticotrope Hormon (ACTH) vermittelt. Bei Stimulation setzt die HPA-Achse schnell hohe Konzentrationen an Glukokortikoid-Stresshormonen frei, was zu einem erhöhten Zellstoffwechsel und der spontanen Bildung von Sauerstoff- und Stickstoffradikalen führt.
Die Glukokortikoidfreisetzung folgt dem zirkadianen Rhythmus , mit den höchsten Werten morgens und den niedrigsten Werten abends. Glukokortikoide steuern die physiologische Funktion, einschließlich Immunität, Insulinsensitivität , Herz-Kreislauf-Aktivität, Fortpflanzungsprozesse, Neurodegeneration und Apoptose.
Die langfristige Aufrechterhaltung eines maladaptiven Abwehrzustands kann zu einer Hypersekretion von Glukokortikoiden und einer Fehlregulation der Funktion des Glukokortikoidrezeptors (GR) führen, einschließlich Abbau von GR, Unterbrechung der GR-Translokation, Bindung von GR-DNA und Veränderungen im Phosphorylierungszustand von GR. Frühere Erkenntnisse legen nahe, dass Glukokortikoidrezeptoren in Mitochondrien translozieren und die mitochondriale Genexpression modulieren können.
Eine Resistenz gegen Glukokortikoide kann durch entzündliche Zytokine verstärkt werden. Die Regulierung der Mitochondrienfunktion durch Corticosteron ist mit der Neuroprotektion verbunden . Die Behandlung mit niedrigen Corticosteron-Dosen hatte eine neuroprotektive Wirkung. Die Behandlung mit hohen Corticosteron-Dosen war toxisch für kortikale Neuronen. Die Regulierung der neuronalen Mitochondrienfunktion durch Steroide steht auch im Zusammenhang mit Neuroprotektion und synaptischer Plastizität.
Die Freisetzung von endogenem CNI kann bei Stress in der Amygdala gemessen werden. Starke anxiolytische Wirkungen werden beobachtet, wenn CRF-Rezeptorantagonisten an die Amygdala verabreicht werden. CRF-haltige Amygdala-Neuronen können direkt durch Veränderungen der zirkulierenden Glukokortikoide über Glukokortikoidrezeptoren moduliert werden, die in Amygdaloid-CRF-haltigen Neuronen exprimiert werden.
Psychische Störungen gehen mit oxidativem Stress einher
Psychische Störungen gehen mit einer verstärkten Entzündung einher.
Dieser Zusammenhang wurde für Angststörungen (posttraumatische Belastungsstörung, generalisierte Angststörung, Panikstörung und phobische Störungen), somatische Symptomstörungen und insbesondere für schwere Depressionen nachgewiesen . Bei depressiven Patienten geht die Entzündung mit neurochemischen, neuroendokrinen und Verhaltensänderungen einher.
Entzündungsprozesse erhöhen die Produktion von ROS und RNS sowie oxidativen Stress sowohl in der Peripherie als auch im zentralen Nervensystem. Depressive Störungen werden mit Biomarkern für erhöhten oxidativen Stress in Verbindung gebracht. Oxidativer Stress führt zu vorzeitigem Altern, was sich in der Verkürzung der Telomere bei Patienten mit schwerer Depression widerspiegelt, und spielt eine Rolle bei der Entstehung und dem Verlauf einer Depression.
Es wurde beobachtet, dass NOX2 als wesentliche Quelle von oxidativem Stress mit schwerem Lebensstress verbunden ist. Darüber hinaus besteht ein negativer Zusammenhang zwischen Depression und Antioxidantienstatus. Antidepressivum-ähnliche Wirkungen können durch die Senkung des NO-Spiegels oder die Blockierung der NO-Synthese im Gehirn hervorgerufen werden.
Bei Patienten mit schwerer depressiver Störung hatte eine Langzeitbehandlung mit Antidepressiva positive Auswirkungen auf oxidative Schäden und das Entzündungsprofil sowie auf die Aktivitäten antioxidativer Enzyme.
Psychotherapie kann auch oxidativen Stress bei Patienten mit schwerer Depression modulieren . Die Behandlung reduzierte die Grundwerte von erhöhtem NO im Serum auf Werte nahe der gesunden Kontrollgruppe. Darüber hinaus kann Psychotherapie durch affektive Etikettierung (Ausdrücken von Gefühlen in Worten) Angstzustände reduzieren.
Zusammengenommen führt die chronische Aktivierung des Angstabwehrsystems zur Aktivierung der SNS- und HPA-Achse. Dies führt zu einer Entkopplung von eNOS, Veränderungen der GC-Sensitivität und einer erhöhten Monozytopoese im Knochenmark, chronischen Entzündungen und damit verbundenen Krankheiten (Arteriosklerose, Fettleibigkeit, Diabetes).
Klinische und soziale Implikationen
Auf Bevölkerungsebene würden Maßnahmen zur Überwindung sozialer Ungleichheiten und zur Verbesserung eines gesunden und sicheren Umfelds Maßnahmen zur Verringerung von Angstzuständen, Entzündungen und oxidativem Stress darstellen. Andere bevölkerungsbezogene Ansätze umfassen gesetzliche Maßnahmen zur Förderung einer antioxidativen Ernährung und eines körperlich aktiven Lebensstils, wie in aktuellen Leitlinien empfohlen.
Auf individueller Ebene können pharmakologische Interventionen möglicherweise hilfreich sein.
|
Es gibt viele evidenzbasierte Interventionen zur Verbesserung der Anpassungsfähigkeit des Angstabwehrsystems, zur Verbesserung der emotionalen Gesundheit und zur Verbesserung des Lebensstils, die von intensiver psychischer Gesundheitsfürsorge über Psychotherapie bis hin zu Achtsamkeitsmeditation zur Verbesserung der Selbstfürsorge und Entspannung reichen. .
















