| Punti salienti |
|
| 1. Introduzione |
Le malattie cardiovascolari (CVD) rappresentano la principale causa di morbilità e mortalità a livello mondiale. Le tendenze globali della disabilità corrette per anni di vita e anni di vita persi sono quasi raddoppiate. L’alta pressione sanguigna (HTN) è il principale fattore di rischio modificabile, responsabile di cambiamenti strutturali e/o funzionali nei principali organi.
La presenza di danno d’organo mediato dall’ipertensione riflette la gravità e l’onere pratico dell’HTN in tali pazienti, nei quali il loro rischio CV totale aumenta significativamente. Esiste una forte relazione epidemiologica tra HTN cronica, CAD e malattia cerebrovascolare.
Esiste una correlazione lineare tra i livelli di pressione arteriosa (PA) e il rischio di CAD, mentre quasi il 25% del rischio di infarto miocardico attribuibile alla popolazione può essere rappresentato da HTN. Allo stesso modo, l’HTN è il fattore di rischio prevalente per l’incidente cerebrovascolare (CVA) presentato in quasi due terzi di questi pazienti. Pertanto, molto spesso i medici dovranno valutare e trattare pazienti affetti da HTN e CAD o malattie cerebrovascolari.
Il trattamento dell’HTN è fondamentale poiché la riduzione della pressione arteriosa si traduce in un miglioramento della morbilità e della mortalità CV. Ogni riduzione della pressione sistolica (SBP) di 10 mmHg diminuisce il rischio di eventi CV di circa il 20%. Tuttavia, quanto bassa dovrebbe essere la pressione arteriosa nei pazienti con malattie coronariche o cerebrovascolari croniche?
Negli ultimi trent’anni, molti ricercatori hanno unito le forze e condotto meta-analisi focalizzate sui pericoli derivanti dalla riduzione della pressione arteriosa al di sotto di una certa soglia, soprattutto nei pazienti con malattie cardiovascolari e ictus. Nonostante ciò, le attuali linee guida ACC/AHA per il trattamento dell’HTN raccomandano una riduzione più aggressiva della pressione arteriosa, una strategia guidata principalmente dai risultati dello studio SPRINT. Al contrario, le linee guida ESC/ESH hanno adottato una strategia più conservativa, soprattutto nei pazienti in cui la riduzione intensiva della pressione arteriosa può essere dannosa.
| 2. Soglie pressorie più basse nei pazienti con malattie coronariche e/o cerebrovascolari croniche |
Secondo le linee guida ACC/AHA per la gestione dei pazienti ipertesi con CAD clinica o ictus), l’obiettivo pressorio raccomandato è <130/80 mmHg, con livelli <120/80 mmHg considerati valori normali. Inoltre, questi pazienti dovrebbero iniziare un trattamento antipertensivo e modifiche dello stile di vita quando i livelli di pressione arteriosa sono ≥ 130/80 mmHg. Al contrario, le linee guida ESC/ESH e International Society of Hypertension (ISH) fissano la pressione arteriosa nei pazienti <65 anni di età, un valore <130/80 mmHg e non un valore <120/70 mmHg. D’altra parte, il trattamento antipertensivo dovrebbe essere iniziato quando i livelli di pressione arteriosa sono ≥ 140/90 mmHg.
La differenza tra queste linee guida rispetto alla soglia inferiore della PA sta nel fatto che le linee guida ESC/ESH e ISH rispettano la possibile esistenza del fenomeno della curva J (le linee guida ACC/AHA non prevedono alcuna soglia inferiore della PA). pressione che deve essere rispettata nei pazienti ipertesi con CAD). Le linee guida ACC/AHA hanno basato le loro raccomandazioni principalmente sui risultati dello studio SPRINT e di due meta-analisi.
Nello studio SPRINT, il trattamento intensivo della pressione arteriosa mirato a una pressione sistolica <120 mmHg, rispetto a <140 mmHg, ha prodotto tassi più bassi di decessi ed eventi CV maggiori non fatali e morte per qualsiasi causa (tuttavia, non è stata notata alcuna diminuzione dell’infarto miocardico mentre la pressione arteriosa la misurazione è stata trascurata). D’altro canto, i risultati delle 2 meta-analisi hanno mostrato che il raggiungimento di livelli di pressione arteriosa <130/80 mmHg era sicuro, con un miglioramento della morbilità e mortalità CV.
| 3. Flusso coronarico e livelli di pressione sanguigna |
Il flusso sanguigno coronarico si verifica principalmente in diastole mentre il flusso subendocardico è esclusivamente un evento diastolico. I fattori che influenzano il flusso coronarico sono principalmente la resistenza al flusso coronarico, la pressione di perfusione coronarica (gradiente di pressione tra le arterie coronarie e l’atrio destro) e la durata della diastole.
Quando le richieste di ossigeno del miocardio aumentano il consumo, la resistenza coronarica diminuisce per aumentare il flusso coronarico. Tuttavia, per avere un’adeguata perfusione miocardica, la pressione di perfusione coronarica deve essere almeno compresa tra 50 e 65 mmHg, presupponendo che la pressione diastolica del ventricolo sinistro sia entro i limiti normali (5-12 mmHg). Va notato che nei pazienti con CAD, la pressione di perfusione coronarica è correlata alla pressione diastolica dell’arteria coronaria, distale rispetto a un’ostruzione coronarica significativa (che è inferiore alla pressione diastolica aortica).
| 4. Obiettivo pressorio nei pazienti con malattia coronarica |
Esistono prove schiaccianti, soprattutto nei pazienti ad alto rischio, che l’abbassamento della pressione arteriosa al di sotto di una certa soglia aumenta il rischio di un successivo evento CV. In diversi studi, come ONTARGET (trattamento con telmisartan, ramipril o entrambi, di pazienti ad alto rischio di eventi vascolari) e VALUE (ipertesi con alto rischio CV trattati con valsartan o amlodipina) in pazienti ad alto rischio, nonché In Negli studi INVEST rivisto (revisione dei risultati dello studio internazionale Verapamil SR-Trandolapril) e TNT (Treating to New Targets) su pazienti ipertesi con CAD, esiste una relazione a forma di J tra i livelli di pressione arteriosa e gli eventi CV.
In questi studi, livelli di pressione arteriosa <120 e/o 70 mmHg aumentavano significativamente il rischio cardiovascolare (anche se nello studio INVEST è probabile che, anziché un aumento del tasso di eventi, si sia verificata una diminuzione dell’entità del beneficio). D’altro canto, i dati del registro Clarify con 22.672 pazienti ipertesi con CAD stabile hanno mostrato che una pressione arteriosa <120 e/o 60 mmHg era associata a esiti CV avversi, inclusa la mortalità. D’altra parte, la pressione di perfusione coronarica deve essere mantenuta per avere un’adeguata perfusione miocardica.
Esistono studi che affermano che nei pazienti con CAD, con o senza rivascolarizzazione, livelli di pressione diastolica <70 mmHg portano ad una marcata riduzione del flusso sanguigno coronarico, fenomeno che era molto più intenso nei pazienti con ipertrofia ventricolare sinistra, una condizione molto grave . comune nei pazienti ipertesi.
Pertanto, non sorprende che nei pazienti ipertesi con CAD, livelli pressori ridotti <70 mmHg fossero anche indipendentemente associati al danno miocardico progressivo, espresso dall’aumento della troponina-T ultrasensibile. D’altra parte, nello studio SPRINT, il trattamento intensivo della pressione arteriosa mirato a una pressione sistolica <120 mmHg, rispetto a <140 mmHg, non ha migliorato la prognosi dei pazienti ipertesi con una storia di CVD. Allo stesso modo, un’analisi di sottogruppi dello studio SPRINT (1.206 partecipanti con CAD e 8.127 partecipanti senza CAD) ha rilevato che il trattamento intensivo della pressione arteriosa ha ridotto il rischio di eventi CV maggiori nei partecipanti senza CAD, ma non in quelli con CAD.
Per i partecipanti con CAD, il trattamento intensivo della pressione arteriosa è stato associato a un ridotto rischio di morte per tutte le cause, ma non ha influenzato altri esiti clinici, rispetto al trattamento standard della pressione arteriosa. Inoltre, nello studio ACCORD, i pazienti con diabete di tipo 2 e una storia di eventi CV, target con pressione sistolica <120 mmHg, rispetto a <140 mmHg, non hanno ridotto il tasso di un esito composito di eventi CV fatali e non fatali. . Secondo gli autori, è deplorevole la mancanza di studi randomizzati e controllati (RCT) progettati per valutare l’esistenza del fenomeno della curva J.
Bassi livelli di pressione arteriosa possono essere correlati a condizioni cliniche sfavorevoli (neoplasia, infezioni, malnutrizione e insufficienza cardiaca) e pertanto presentano un tasso di eventi più elevato. Nello studio INDANA (Individual Antihypertensive Data Analysis), una meta-analisi che ha incluso 40.233 pazienti ipertesi (follow-up medio, 3,9 anni), gli autori hanno concluso che le cattive condizioni di salute erano responsabili dei bassi livelli di pressione arteriosa. , con aumento del rischio di morte.
L’aumento del rischio di eventi non era correlato al trattamento antipertensivo né era specifico agli eventi vascolari correlati alla pressione arteriosa. Inoltre, in una recente meta-analisi, gli autori hanno scoperto che nel prevenire la morte cardiovascolare, un trattamento più intensivo della pressione arteriosa era superiore alla strategia di controllo meno intensivo, sebbene questi risultati siano ancora inconcludenti.
Sebbene esistano risultati contraddittori riguardo all’esistenza del fenomeno della curva a J, nei pazienti con CAD non vi è evidenza che la riduzione dei livelli di pressione arteriosa <120/70 mmHg sia vantaggiosa. Pertanto, la soglia della pressione sistolica <120 mmHg adottata da diversi algoritmi per il trattamento dell’angina stabile. In questo studio sono stati utilizzati farmaci antianginosi, poiché i beta-bloccanti, i calcio-antagonisti o i nitrati hanno anche effetti antipertensivi e, in questi pazienti, giustificano le soglie pressorie <120/70 mmHg delle linee guida ESC/ESH. per la gestione di HTN.
| 5 . Flusso sanguigno cerebrale e livelli di pressione sanguigna |
I vasi cerebrali sono molto vulnerabili agli effetti di una pressione arteriosa più elevata e sia l’ipertensione sistolica che quella diastolica sono fattori di rischio per l’ictus ischemico (CVA) e l’ictus emorragico.
L’autoregolazione della circolazione cerebrale consente di mantenere il flusso sanguigno cerebrale a livelli stabili, nonostante le variazioni della pressione arteriosa comprese tra 60 e 150 mmHg. Tuttavia, l’HTN prolungato provoca marcati cambiamenti adattativi nella circolazione cerebrale, tra cui un aumento della resistenza dei vasi cerebrali e modifiche del meccanismo di autoregolazione fisiologica.
L’HTN modifica l’autoregolazione del flusso sanguigno cerebrale, modificando i limiti inferiore e superiore della capacità di autoregolazione verso valori di pressione arteriosa più elevati. Pertanto, i pazienti ipertesi possono essere particolarmente vulnerabili agli episodi di HBP, che possono svolgere un ruolo nello sviluppo del danno cerebrovascolare silente.
L’effetto della pressione arteriosa elevata sui piccoli vasi è ben noto, con il rimodellamento vascolare che si verifica nei vasi sanguigni cerebrali durante l’HTN cronica. Questa struttura altera l’autoregolazione, giocando un ruolo nello sviluppo della malattia cerebrale silenziosa, che comprende lesioni della sostanza bianca, microsanguinamenti e infarti lacunari, che evolvono verso esiti clinici come ictus e demenza.
| 6. Mirare alla pressione sanguigna per prevenire gli ictus primari |
Studi prospettici hanno dimostrato una relazione positiva continua, forte e indipendente tra i livelli di pressione arteriosa e la CVD. Questo vale sia per la pressione sistolica che per la pressione diastolica. Inoltre, l’evidenza aggregata di studi prospettici di coorte suggerisce che il rischio minimo di pressione arteriosa per CVD potrebbe essere una pressione sistolica compresa tra 110 mmHg e 115 mmHg.
Una meta-analisi di RCT comprendenti centinaia di migliaia di pazienti ha dimostrato che una riduzione di 10 mmHg della pressione sistolica o di 5 mmHg della pressione diastolica è associata a riduzioni significative di quasi il 20% in tutti gli eventi CV maggiori, a una riduzione del 35% dell’ictus e del 10% -15% della mortalità complessiva. Queste riduzioni del rischio relativo sono coerenti indipendentemente dalla pressione arteriosa basale compresa nell’intervallo ipertensivo, dal livello di rischio CV, dalle comorbidità (ad es. diabete, malattia renale cronica), dall’età, dal sesso e dall’etnia.
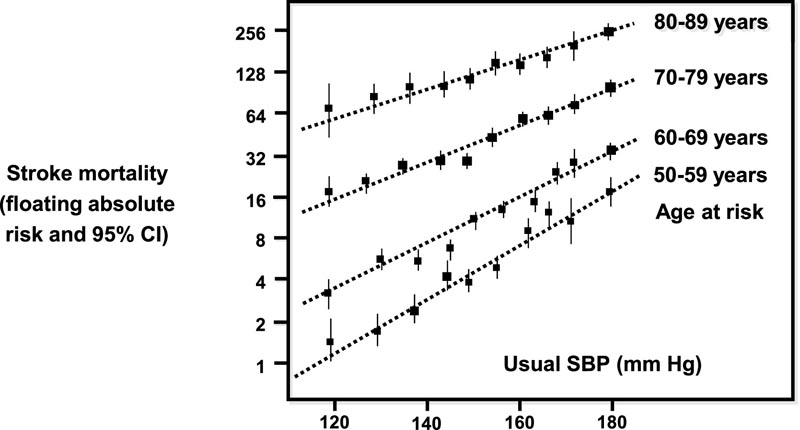
Figura 1 Tasso di mortalità per ictus in ogni decennio rispetto alla normale pressione sistolica all’inizio di quel decennio (rischio assoluto variabile e IC al 95%). Modificato e adattato dal riferimento.
Per raggiungere livelli target <140/90 mmHg in ambulatorio, le linee guida sull’ipertensione ESH/ESC raccomandano un target pressorio <140/90 mmHg, indipendentemente dal numero di comorbilità e dal livello di rischio CV. A quel tempo, le evidenze derivanti dalla meta-analisi e dall’analisi post hoc di studi partecipanti su larga scala non hanno mostrato un aumento significativo dei benefici della pressione arteriosa <130/80 mmHg. Da allora, nuove informazioni sono emerse dall’analisi post hoc dei risultati di ampi studi condotti su pazienti ad alto rischio CV. Nuovi RCT e meta-analisi di tutti gli RCT disponibili.
Nell’analisi post hoc degli RCT e dei dati dei registri, rispetto a un target di pressione sistolica compreso tra 130 mmHg e 139 mmHg, una riduzione della pressione sistolica <130 mmHg è stata associata a una maggiore riduzione del rischio di ictus, in particolare nei pazienti con diabete di tipo 2. 2. Un risultato coerente è stato che la riduzione della pressione sistolica <120 mmHg ha aumentato l’incidenza di eventi CV e morte.
Recentemente sono stati pubblicati due importanti studi randomizzati che affrontano questo problema: lo studio SPRINT e lo studio STEP. Il primo ha confrontato 2 diversi target di pressione sistolica (<140 o <120 mmHg) in più di 9.000 pazienti ipertesi ad alto rischio cardiovascolare, ma sono stati esclusi i pazienti con diabete o precedente ictus. Un trattamento antipertensivo più intensivo con pressione sistolica target <130 mmHg (pressione sistolica media raggiunta 121 contro 136 mmHg nel braccio standard) è stato associato a una riduzione del 25% degli eventi CV maggiori e a una riduzione del 27% della morte per tutte le cause. , sebbene non sia stata osservata alcuna riduzione significativa dell’ictus.
Vale la pena ricordare che, secondo i criteri di inclusione, i pazienti nello studio SPRINT non erano naïve al trattamento antipertensivo ed erano in grado di tollerare 3 farmaci senza ipotensione ortostatica. Non era rappresentativo della media della popolazione non trattata. Lo studio STEP aveva un disegno simile che confrontava 2 diversi target di pressione sistolica (<150 o <130 mmHg) in più di 8.000 pazienti ipertesi cinesi di età compresa tra 60 e 80 anni, esclusi quelli con una storia di ictus o ictus emorragico.
Durante un periodo di follow-up medio di 3,34 anni, il trattamento ipotensivo più intensivo che ha raggiunto una pressione sistolica <130 mmHg (media raggiunta 127,5 contro 135,3 mmHg nel braccio standard) è stato associato ad una riduzione del 26% degli eventi CV maggiori e ad una riduzione del 28% degli eventi CV maggiori. riduzione della mortalità per cause CV. Anche l’ictus da E è stato significativamente ridotto del 33%. Per quanto riguarda la sicurezza e gli esiti renali, non sono state riscontrate differenze significative tra i 2 gruppi, ad eccezione dell’incidenza di ipotensione ortostatica, che è risultata maggiore nel gruppo di trattamento intensivo. Questi ultimi due studi forniscono un supporto indiscutibilmente forte a favore degli effetti benefici di una riduzione più intensa della pressione arteriosa rispetto a strategie terapeutiche intensive nei pazienti ad alto rischio.
Gli autori concludono che, tenendo conto dei risultati di questi 2 RCT e di quelli della meta-analisi, vi è accordo con le nuove raccomandazioni delle linee guida, nel raggiungimento degli obiettivi di PAS <130 mmHg, a condizione che il trattamento sia ben effettuato. tollerato. Nei pazienti in età avanzata, si raccomanda un target di PAS più cauto (<140 mmHg), anche se un target <130 mmHg sarebbe migliore per prevenire l’ictus primario nei soggetti fino a 80 anni di età, se c’è una buona tolleranza al trattamento. e si evita l’ipotensione ortostatica.
| Raccomandazioni per la gestione della pressione arteriosa nei pazienti con ictus emorragico | Classe | Livello |
| Non è raccomandato l’abbassamento immediato della pressione sistolica <220 mmHg | III | A |
| Nei pazienti con pressione sistolica ≥220 mmHg: trattamento acuto della pressione arteriosa, con farmaci per via endovenosa per raggiungere una pressione arteriosa <180 mmHg. | II bis | B |
| NOTA: Raccomandazioni delle linee guida sull’ipertensione ESC/ESH del 2018 sulla gestione della pressione arteriosa nei pazienti in fase acuta di ictus emorragico | ||
| 7. Valori target della pressione arteriosa durante la fase acuta dell’ictus emorragico |
La pressione arteriosa elevata è molto comune nell’ictus emorragico acuto a causa di diversi fattori; Una pressione sistolica elevata è associata a una maggiore espansione dell’ematoma e a deterioramento neurologico, dipendenza e morte. Rispetto all’ictus, in cui sono state trovate associazioni coerenti a forma di J tra pressione sistolica al nadir di 140 e 150 mmHg e scarsi risultati, il problema principale con l’ictus emorragico è l’elevata pressione sistolica superiore a 150 mmHg. Per questi pazienti, la pressione sistolica è compresa tra 150 e 220 mmHg, se non vi sono controindicazioni al trattamento acuto della pressione arteriosa.
Le linee guida AHA/ASA del 2015 raccomandano che la riduzione acuta della pressione sistolica <140 mmHg sia sicura e possa essere efficace nel migliorare gli esiti. Per i pazienti con ictus emorragico con pressione sistolica >220 mmHg, può essere ragionevole considerare una riduzione aggressiva della pressione arteriosa attraverso l’infusione endovenosa continua e un monitoraggio frequente. Queste raccomandazioni si basavano sui risultati di 2 studi, INTERACT-2 e lo studio di Qureshi et al, e su una meta-analisi.
INTERACT-2 è un RCT internazionale di fase 3 in aperto, con esame end-point in cieco (disegno PROBE), con 2.839 pazienti con emorragia intracranica spontanea 6 ore dopo ictus emorragico, con pressione sistolica compresa tra 150 e 220 mmHg. I pazienti sono stati randomizzati per implementare una riduzione intensiva della pressione arteriosa (target <140 mmHg) o il trattamento raccomandato dalle linee guida (pressione arteriosa <180 mmHg) nella prima ora.
Il trattamento intensivo non ha ridotto gli esiti primari di morte o disabilità maggiore a 3 mesi, ma la riduzione dell’espansione dell’ematoma ha migliorato il recupero funzionale ed è stato sicuro, senza alcuna differenza negli effetti collaterali rispetto al controllo contemporaneo della PAS <180. mmHg, raccomandato dalle linee guida. Un’analisi aggiuntiva del set di dati INTERACT-2 ha esplorato se diversi gradi di riduzione della pressione sistolica mediante il trattamento durante i 7 giorni successivi all’ictus emorragico fossero associati al rischio di esiti sfavorevoli a 90 giorni e se il rapporto beneficio/danno variasse in base al livello di pressione arteriosa a 90 giorni. presentazione.
Riduzioni maggiori della pressione sistolica (20 e 30 mmHg durante la prima ora dopo la randomizzazione) erano significativamente associate a rischi inferiori di esiti sfavorevoli rispetto alla riduzione minima <10 mmHg. D’altra parte, un recupero ottimale dall’ictus emorragico è stato osservato nei pazienti ipertesi che hanno ottenuto le maggiori riduzioni della pressione arteriosa (≥20 mmHg) nella prima ora e l’hanno mantenuta per 7 giorni. Tuttavia, in un successivo RCT su 1.000 pazienti con ictus emorragico e PAS <220 mmHg, 500 sono stati assegnati a un target di PAS compreso tra 110 e 139 mmHg (trattamento intensivo) e gli altri 500 a un target compreso tra 140 e 179 mmHg (trattamento standard). . .
Lo scopo dello studio era verificare se la riduzione intensiva della pressione sistolica con nicardipina per via endovenosa fornisce risultati migliori rispetto al trattamento standard. La nicardipina è stata somministrata entro 4,5 ore dall’insorgenza dei sintomi. Similmente allo studio INTERACT-2, l’outcome primario 3 mesi dopo la randomizzazione era la morte o la disabilità maggiore. L’esito primario è stato osservato nel 38,7% dei partecipanti nel gruppo di trattamento intensivo e nel 37,7% nel gruppo di trattamento standard.
Una riduzione più intensa della pressione arteriosa non ha avuto alcun beneficio sull’esito primario simile ed è stata associata a più eventi avversi renali. Per quanto riguarda i pazienti con ictus emorragico e PAX ≥220 mmHg, Tsivgoulis et al. hanno eseguito una revisione sistematica e una meta-analisi di tutti gli studi randomizzati che hanno selezionato casualmente pazienti con ictus emorragico acuto per ricevere un trattamento intensivo o secondo linee guida per la riduzione della pressione arteriosa. Dopo aver identificato 4 studi eleggibili che includevano 3.315 pazienti, la meta-analisi ha mostrato che i tassi di mortalità erano simili in entrambi i gruppi, sebbene il trattamento ipotensivo intensivo mostrasse una tendenza ad essere associato a un tasso inferiore di morte o dipendenza a 3 mesi, rispetto al trattamento ipotensivo. trattamento prescritto.
Un’altra recente meta-analisi dei dati degli studi clinici ha dimostrato che la terapia intensiva ha ridotto in modo sicuro la pressione sistolica, così come l’espansione dell’ematoma, ma questa riduzione non ha portato a un risultato funzionale migliore. A ciò si è aggiunta un’analisi secondaria dello studio ATACH2, in cui è stata eseguita una rapida riduzione intensiva della pressione arteriosa entro 2 ore dall’insorgenza dei sintomi dell’ictus emorragico, una riduzione dell’espansione dell’ematoma e un miglioramento dei risultati funzionali.
In sintesi, gli autori affermano che l’obiettivo di raggiungere una pressione sistolica ottimale nei pazienti con ictus emorragico acuto rimane oggetto di dibattito e, nonostante l’evidenza che l’espansione dell’ematoma sia ridotta nei pazienti trattati in modo intensivo, questo approccio non ha portato costantemente a risultati migliori.
Nei pazienti con ictus emorragico da lieve a moderato e pressione arteriosa sistolica compresa tra 150 e 220 mmHg, la riduzione aggressiva della pressione sistolica fino a un target di 120-139 mmHg è relativamente sicura, sebbene presenti un potenziale rischio di danno renale e potrebbe migliorare l’esito funzionale. limitare l’espansione dell’ematoma. Idealmente, il trattamento dovrebbe iniziare entro 2 h dall’esordio dei sintomi, raggiungendo il target della pressione arteriosa sistolica senza problemi.
Le linee guida ESC/ESH del 2018 sull’ipertensione stabiliscono che l’abbassamento della pressione arteriosa non è raccomandato come approccio di routine per i pazienti con ictus emorragico e pressione sistolica <220 mmHg e per i pazienti con ictus emorragico e pressione sistolica ≥220 mmHg. Un’attenta riduzione acuta della pressione arteriosa a <180 mmHg dovrebbe essere considerata un obiettivo terapeutico. Tuttavia, dati più recenti suggeriscono che una riduzione della pressione sistolica <140 mmHg può essere presa in considerazione nei pazienti con ictus emorragico da lieve a moderato e una pressione sistolica basale compresa tra 150 e 220 mmHg.
| 8 . Valori target della pressione arteriosa durante la fase acuta dell’ictus ischemico |
Come accade nell’ictus emorragico, l’HTN è un problema nelle fasi iniziali dell’ictus acuto, mentre in oltre il 60% dei pazienti si osservano aumenti della pressione sistolica > 160 mmHg, associati a edema cerebrale e scarsi risultati. Teoricamente, le ragioni per abbassare la pressione arteriosa in questa situazione clinica includono la riduzione della formazione di edema cerebrale, la minimizzazione del rischio di trasformazione emorragica dell’infarto, la prevenzione di ulteriori danni vascolari e la diminuzione del rischio di ictus precoce ricorrente. Tuttavia, nella maggior parte dei pazienti senza alcun trattamento medico specifico, si osserva una riduzione spontanea della pressione sistolica di circa 10-15 mmHg durante le prime 24 ore. Pertanto, il trattamento aggressivo di tutti i pazienti con elevata pressione sistolica iniziale può portare a un peggioramento neurologico, derivante dalla ridotta pressione di perfusione nelle aree cerebrali ischemiche, con un peggioramento dell’ipossia neuronale.
La fisiopatologia dell’aumento transitorio della pressione arteriosa nell’ictus acuto è complessa e poco compresa. È stato suggerito l’intervento di diversi fattori, alcuni dei quali non specifici e non correlati al processo ischemico cerebrale, come lo stress psicologico, mentre altri sono specifici dell’ictus, come i sottotipi di ictus.
I risultati degli studi che hanno studiato il collegamento dell’HTN durante le prime ore dopo l’ictus con gli esiti clinici a breve e lungo termine dopo l’ictus sono particolarmente contrastanti. Infatti, l’HTN in fase acuta può essere benefico poiché mantiene il flusso ematico cerebrale nel tessuto ischemico ma, d’altro canto, può essere dannoso poiché facilita l’edema cerebrale e la trasformazione emorragica. Sebbene molti studi abbiano affrontato la questione della gestione della pressione arteriosa nell’ictus acuto, la loro interpretazione è ostacolata da importanti problemi metodologici che portano a risultati diversi tra le popolazioni indagate. Pertanto, la corretta gestione dell’ipertensione nell’ictus acuto rimane poco chiara e le prove disponibili sono insufficienti per dimostrare che la riduzione della pressione arteriosa riduca la mortalità o la disabilità nei pazienti con ictus ischemico acuto. Tuttavia, ci sono alcune indicazioni sulla possibile efficacia di una riduzione molto precoce della pressione arteriosa. Tuttavia, mancano dati affidabili sull’influenza dei valori della PA sugli esiti dell’ictus e pertanto la gestione della PA nella fase acuta dell’ictus rimane piuttosto empirica. Le attuali raccomandazioni di tutte le linee guida riconoscono che si basano su opinioni piuttosto che su prove.
| 9 . Come viene gestita la pressione arteriosa nella fase acuta dell’ictus ischemico? |
L’andamento temporale della pressione arteriosa e l’entità della variazione pressoria nelle prime 24 ore dopo l’ictus sembrano essere molto più prognostici rispetto alla sola pressione basale. La pressione arteriosa al ricovero è spesso fuorviante a causa di fluttuazioni transitorie e non specifiche della pressione arteriosa a seguito di una malattia critica acuta come un ictus acuto. Registrazioni consecutive della pressione arteriosa nella fase acuta dell’ictus (p. es., monitoraggio della pressione arteriosa nelle 24 ore) possono indicare in modo più affidabile i fattori che portano alla risposta ipertensiva acuta.
Il monitoraggio continuo o intermittente della PA nelle 24 ore è correlato più strettamente al danno d’organo bersaglio e agli eventi CV maggiori, compreso l’edema nell’ictus acuto, rispetto ai valori pressori ambulatoriali isolati. Inoltre, rispetto alle registrazioni individuali, il monitoraggio 24 ore su 24 riduce la risposta pressoria al ricovero ospedaliero, il bias dell’osservatore e la variabilità della misurazione.
Il monitoraggio della pressione arteriosa consente di misurare in modo più accurato i rapidi cambiamenti della pressione arteriosa durante un ictus acuto. Pertanto, il monitoraggio continuo o intermittente della PA, con variazioni relative piuttosto che assolute, potrebbe fornire informazioni prognostiche migliori sul decorso e sull’intervallo delle fluttuazioni della PA rispetto alla PA casuale.
Recentemente, valori pressori più elevati derivanti dal monitoraggio delle 24 ore, rispetto alla PA durante il ricovero, sono stati associati all’esito dell’ictus. Tuttavia, non è ancora chiaro se questa associazione sia causale o meno. Tuttavia, l’opzione migliore sembra essere un attento monitoraggio delle registrazioni della PA nelle prime 24 ore, sebbene manchino dati a supporto della modulazione attiva della PA con la terapia antipertensiva durante l’ictus acuto.
Negli ultimi anni, diversi studi clinici randomizzati hanno valutato i benefici e i rischi della riduzione della pressione arteriosa durante l’ictus acuto attraverso il trattamento antipertensivo. Tuttavia, la maggior parte degli studi ha valutato l’effetto degli interventi nella fase subacuta, iniziando entro 24-72 ore dall’insorgenza dell’ictus.
Il tempo mediano per iniziare la riduzione della pressione arteriosa in 13 studi controllati, con 12.703 partecipanti, non era anteriore a 15 ore dopo l’insorgenza dell’ictus. In generale, gli studi che affrontano questo problema non hanno riscontrato effetti benefici della terapia per abbassare la pressione arteriosa. Lo SCAST è un RCT in doppio cieco, controllato con placebo, con 2.029 pazienti con ictus acuto (ischemico o emorragico) e pressione sistolica ≥ 140 mm Hg inclusi entro le prime 30 ore dall’insorgenza dei sintomi. I pazienti sono stati assegnati in modo casuale a candesartan o placebo per 7 giorni, con la dose aumentata da 4 mg il giorno 1 a 16 mg nei giorni dal 3 al 7.
I due endpoint co-primari erano: 1) un endpoint composito di morte vascolare, infarto miocardico o ictus durante i primi 6 mesi e 2) esito funzionale a 6 mesi. Dopo 6 mesi di follow-up, il rischio dell’endpoint vascolare composito non era diverso tra i gruppi di trattamento e l’analisi dei risultati funzionali ha suggerito un rischio più elevato di esito sfavorevole nel gruppo trattato.
Non è stata osservata alcuna differenza tra i 2 gruppi per tutti gli endpoint secondari prespecificati, tra cui morte per qualsiasi causa, morte vascolare, ictus e ictus emorragico, infarto miocardico, progressione dell’ictus, ipotensione sintomatica e insufficienza renale. .
Un’analisi secondaria dello studio SCAST mirava a studiare l’effetto della riduzione della pressione sistolica durante i primi 2 giorni dopo l’ictus sul rischio di eventi avversi e sugli esiti a breve e lungo termine nell’intera popolazione, indipendentemente dal trattamento assegnato. Da notare che i pazienti con una marcata diminuzione o aumento/nessuna variazione della pressione sistolica avevano un rischio significativamente più elevato di eventi avversi precoci rispetto a quello dei pazienti con piccole diminuzioni.
I pazienti con un aumento o nessuna variazione della pressione arteriosa e quelli con una notevole riduzione della pressione sistolica > 28 mmHg avevano un rischio significativamente maggiore di esito neurologico sfavorevole rispetto ai gruppi con una diminuzione piccola (<15 mmHg) o moderata (15-28 mmHg). mmHg) del PAAS, adottando una curva a forma di “U”. Questi risultati supportano le linee guida ESC/ESH 2018 sull’ipertensione, che raccomandano di evitare ampie riduzioni della pressione arteriosa e che la riduzione della pressione arteriosa non dovrebbe essere un’azione di routine nella fase acuta dell’ictus tranne che in 2 situazioni cliniche: 1) nei pazienti idonei alla trombolisi endovenosa, La pressione arteriosa deve essere cautamente ridotta e mantenuta al di sotto di 180/105 mmHg, almeno per 24 ore dopo la trombolisi e, 2) nei pazienti con livelli di pressione sistolica marcatamente elevati e mantenuti durante le prime 24 ore, che non sono candidati alla fibrinolisi. Si può prendere in considerazione una riduzione lieve/moderata della pressione sistolica pari a circa il 15% dei valori basali.
La tempistica dell’intervento dell’Autorità Palestinese potrebbe essere cruciale. Esistono alcune prove della possibile efficacia di una riduzione molto precoce della pressione arteriosa entro 6 ore dall’esordio dell’ictus, sebbene ciò sia basato sull’analisi di sottogruppi di un singolo studio. D’altra parte, i risultati di uno studio osservazionale suggeriscono che, nei pazienti con ictus acuto, la riduzione della pressione arteriosa e l’uso di agenti ipotensivi durante le prime 24 ore potrebbero essere associati a un minor rischio di prognosi sfavorevole, indipendentemente dal fatto che siano stati trattati o meno. . o meno con un attivatore tissutale del plasminogeno ricombinante. Anche una sottoanalisi del China Antihypertensive Trial i nell’ictus acuto suggerisce che la riduzione della pressione arteriosa potrebbe ridurre la morte, la disabilità grave e l’ictus ricorrente nei pazienti cinesi che hanno ricevuto un trattamento antipertensivo tra 24 e 48 ore dopo l’insorgenza dell’ictus.
Nessun effetto benefico è stato riscontrato quando il trattamento è iniziato entro 12 ore. Sono necessarie ulteriori ricerche per stabilire se i tempi di riduzione della pressione arteriosa siano importanti nel trattamento dei pazienti con ictus acuto e se siano associati alla presenza di penombra viva. In sintesi, una recente dichiarazione del Gruppo sull’ipertensione e il cervello della Società europea di ipertensione ha concluso che la pressione arteriosa è altamente dinamica e non un’entità statica nella fase acuta e dovrebbe idealmente essere misurata continuamente durante la fase acuta. di ictus ischemico.
Attualmente non esistono dati convincenti a sostegno della riduzione di routine della pressione arteriosa durante le prime ore o giorni di ictus, sebbene risultati recenti suggeriscano che la riduzione precoce della pressione arteriosa nell’ictus ischemico possa essere utile nel prevenire la morte o la dipendenza. almeno in alcuni sottogruppi. Ciò richiede conferma in ulteriori studi per identificare i pazienti che hanno maggiori probabilità di trarre beneficio dalla riduzione della pressione arteriosa in caso di ictus e per stabilire la finestra temporale in cui il trattamento ha maggiori probabilità di portare a una risposta favorevole.
| Raccomandazioni per la gestione della pressione arteriosa nei pazienti con ictus ischemico acuto | Classe | Livello |
| L’abbassamento di routine della pressione arteriosa non è raccomandato nei pazienti con ictus acuto. | II | A |
| Nei pazienti eleggibili per la trombolisi, la pressione arteriosa EV deve essere cautamente ridotta e mantenuta <180/105 mmHg, almeno 224 ore dopo la trombolisi. | II bis | B |
| Nei pazienti con un marcato aumento della pressione arteriosa che non ricevono fibrinolisi, il trattamento farmacologico può essere somministrato secondo criteri clinici, per ridurre del 15% della pressione arteriosa[A durante le prime 24 ore dopo la comparsa dei sintomi. | IIb | C |
| NOTA: Raccomandazioni delle linee guida sull’ipertensione ESC/ESH del 2018 sulla gestione della P durante la fase acuta dell’ictus ischemico | ||
| 10 . Valori target della pressione arteriosa per la prevenzione dell’ictus secondario |
La riduzione della pressione arteriosa dopo un ictus riduce il rischio di recidiva e di altri eventi vascolari. Tutte le linee guida affermano che i sopravvissuti all’ictus, sia ipertesi che normotesi, esclusi quelli con ipotensione sintomatica, dovrebbero essere trattati con antipertensivi e apportare modifiche allo stile di vita. Tuttavia, vi sono prove che una pressione arteriosa bassa può portare a risultati sfavorevoli.
Lo studio NEMESIS (North East Melbourne Stroke Incidence Study), volto ad indagare la relazione tra pressione arteriosa ed esito nei sopravvissuti a ictus a 5 anni, ha dimostrato che la pressione sistolica ≤120 mmHg era associata ad un aumento del 61% del rischio di recidiva di ictus, infarto miocardico acuto e morte rispetto ai pazienti con una categoria di pressione sistolica di riferimento compresa tra 131 e 141 mmHg rispetto alla categoria di riferimento, non è stata riscontrata alcuna differenza nell’esito dei pazienti con pressione sistolica di riferimento compresa tra 121 e 130 mmHg. Questo studio ha confermato che una pressione sistolica molto bassa <120 mmHg può comportare una prognosi sfavorevole.
Lo studio SPS3 era uno studio clinico multicentrico, randomizzato, che mirava a esplorare il target ottimale di pressione arteriosa da raggiungere dopo un ictus. I partecipanti sono stati randomizzati a 2 diversi obiettivi di pressione sistolica: lo standard 130-149 mmHg e l’intensivo <130 mmHg. Nel corso di un follow-up di circa 3,5 anni, i partecipanti più anziani hanno raggiunto livelli di PAS simili a quelli dei partecipanti più giovani con una media di 127 mmHg nel gruppo intensivo e 138 mmHg nel gruppo standard.
Negli adulti più giovani, l’ictus ricorrente era meno probabile nel gruppo intensivo rispetto al gruppo di trattamento standard, ma non negli anziani. Tuttavia, l’obiettivo SBP intensivo è stato associato a una significativa riduzione della morte vascolare nei partecipanti più anziani.
Lo studio ha dimostrato chiaramente che il trattamento intensivo riduce significativamente il rischio di emorragia cerebrale del 63%, ma non riduce il rischio di recidiva di infarti lacunari. È stata trovata un’associazione a forma di J tra la pressione arteriosa raggiunta e i risultati. I soggetti che presentavano il rischio più basso erano quelli con pressione sistolica compresa tra 128 mmHg/67 mmHg e pressione diastolica compresa tra 65 e 70 mmHg. Al di sotto di questi livelli il rischio di mortalità aumenta.
Una revisione sistematica e un’analisi di meta-regressione dell’associazione tra riduzione della pressione arteriosa, ictus ricorrente ed eventi CV, utilizzando dati provenienti da 42.736 pazienti provenienti da 14 bracci di studi clinici randomizzati sulla prevenzione secondaria dell’ictus, hanno mostrato che la riduzione della pressione sistolica era correlata in modo lineare e significativo a un minor rischio di ictus ricorrente, infarto miocardico, morte per qualsiasi causa, malattie cardiovascolari e morte. Allo stesso modo, la riduzione della pressione diastolica era correlata linearmente al minor rischio di ictus ricorrente e alla mortalità complessiva. Tutti questi risultati mostrano chiaramente che un controllo rigoroso e aggressivo della pressione arteriosa è essenziale per la prevenzione secondaria dell’ictus e che un target di pressione arteriosa <130/80 mmHg dovrebbe essere stabilito per tutti i pazienti di età compresa tra 18 e 80 anni.
Nei pazienti >80 anni, il Berlin Initiative Study, uno studio di coorte prospettico in corso su individui di età ≥70 anni iniziato nel 2009, ha mostrato che su 1.628 pazienti (età media 81 anni) trattati con antipertensivi, 636 presentavano una pressione arteriosa normalizzata (< 140 /90 mmHg) e 992 avevano valori di PA ≥140/90 mmHg. Rispetto alla pressione arteriosa non normalizzata, la pressione normalizzata era associata a un rischio più elevato di mortalità complessiva. I rischi osservati erano aumentati nei pazienti di età >80 anni e in quelli con precedenti eventi CV, ma non nei pazienti di età compresa tra 70 e 79 anni.
Tenendo conto delle evidenze attuali, tutte le linee guida raccomandano un target pressorio <130/80 mmHg per i pazienti di età compresa tra 18 e 79 anni con una storia di ictus o attacco ischemico transitorio e, nei pazienti più anziani, l’utilizzo di target pressori più cauti e regimi più prudenti e farmaci individualizzati.