Il lupus eritematoso sistemico (LES) è una malattia autoimmune, in cui oltre il 90% dei pazienti sono donne. I sintomi variano ampiamente, da lievi manifestazioni cutanee a insufficienza d’organo potenzialmente letale.
Sebbene la prognosi dall’introduzione dei corticosteroidi e di altre modalità di trattamento sia migliorata considerevolmente, vi è ancora un aumento della mortalità nel LES con complicanze, soprattutto nel caso della nefrite da lupus e delle malattie cardiovascolari (CVD).
L’evoluzione dei criteri diagnostici per il LES è di per sé interessante e i più recenti provengono dalla European League Against Rheumatism/American College of Rheumatology nel 2019, dove erano richiesti anticorpi antinucleari positivi (ANA) come criterio di ingresso e quindi una combinazione di criteri clinici manifestazioni e misure sierologiche/immunologiche.
Va notato che le malattie reumatiche in generale si basano su criteri , il che riflette il fatto che la conoscenza delle loro cause è relativamente scarsa, sebbene i meccanismi che le causano direttamente siano molto più definiti. È probabile che questi criteri cambieranno in futuro e anche che i confini tra queste malattie, in particolare le malattie autoimmuni sistemiche (SAD), non saranno così chiari come suggeriscono i criteri.
La presenza di ANA come prerequisito per la diagnosi illustra che il materiale nucleare (con cellule morte come probabile origine) e l’autoimmunità contro di esso è una caratteristica centrale della malattia. La clearance anomala e/o disfunzionale delle cellule morte rappresenta un altro aspetto importante. Uno squilibrio nel sistema immunitario con una percentuale inferiore di cellule T regolatorie (Tregs) è un’altra peculiarità del LES e un esempio di aberrazione immunologica.
Il LES è relativamente raro. La sua incidenza è in aumento in diversi paesi, ma ciò può essere attribuito a una migliore diagnosi. Esistono anche differenze interessanti tra le etnie, dove il LES è più comune nelle popolazioni africane e arabe, più basso tra le popolazioni ispaniche e asiatiche e ancora più basso tra i caucasici.
Il LES aveva una prognosi molto peggiore prima che fosse istituito il trattamento con immunosoppressori, compreso il cortisone. Successivamente, divenne chiaro che la CVD era importante come complicanza successiva e in un importante studio della fine degli anni ’70 fu riportato un modello bimodale di LES, in cui le complicanze più acute nella fase iniziale della malattia erano spesso seguite da CVD a una fase successiva.
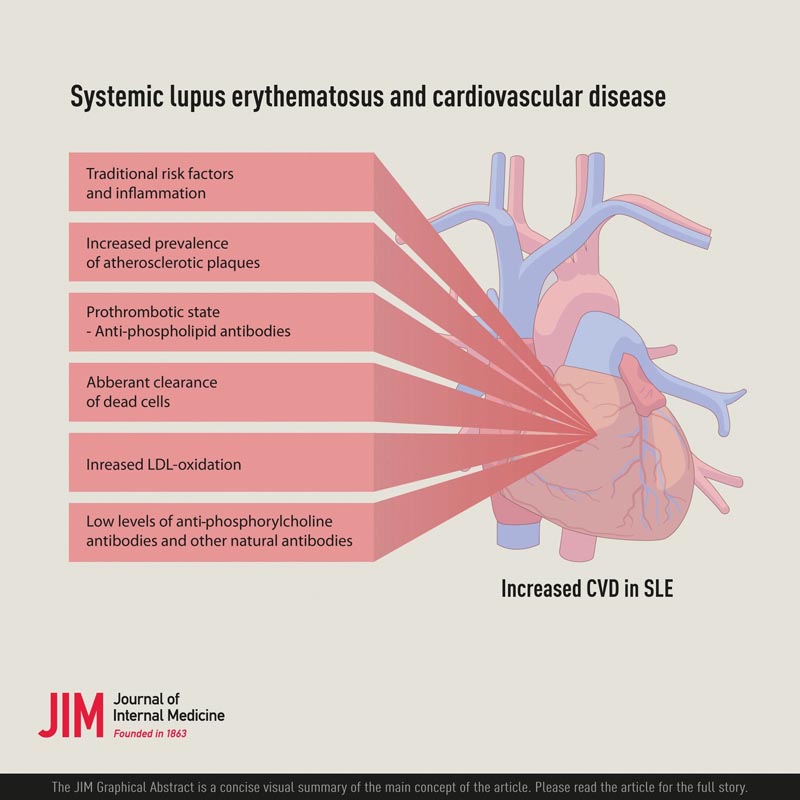
Una questione importante, dato l’aumento del rischio di malattie cardiovascolari nel LES, è quali fattori di rischio siano coinvolti. Uno studio controllato ha riportato che era coinvolta una combinazione di fattori di rischio tradizionali e non tradizionali . Tra quelli non tradizionali, è stato osservato un aumento dei livelli di lipoproteine ossidate a bassa densità (OxLDL) e anche di anticoagulanti lupus, che sono correlati agli anticorpi antifosfolipidi. Tra quelli tradizionali, la dislipidemia era associata a CVD. Tuttavia, la dislipidemia nel LES ha caratteristiche specifiche, con basse lipoproteine ad alta densità (HDL), trigliceridi elevati, ma non LDL elevati.
La causa alla base della CVD nel LES può essere correlata sia alla trombosi, alla sindrome da anticorpi antifosfolipidi (APS) causata da anticorpi antifosfolipidi (aPL), sia alla malattia aterosclerotica , che non si esclude ancora a vicenda.
In generale, l’APS è caratterizzata da trombosi, sia arteriose che venose, e da complicanze della gravidanza, soprattutto aborto spontaneo.
La SAF è divisa in primaria e secondaria , dove la prima è rara, sebbene l’aFL di per sé possa essere determinata nell’1%-5% della popolazione, raramente portando alla SAF. La determinazione dell’aPL è importante anche in altre malattie autoimmuni sistemiche, non solo nel LES, per ridurre il rischio di APS secondaria.
Gli anticorpi antifosfolipidi riconoscono i fosfolipidi, in particolare la cardiolipina (CL), ed è diventato chiaro che le proteine leganti i fosfolipidi svolgono un ruolo importante, con la beta-2-glicoproteina che attualmente considero la più rilevante come cofattore per aPL. Molto probabilmente, gli effetti patogeni possono essere divisi in due, che non si escludono a vicenda: effetti diretti sull’endotelio e su altre cellule e piastrine, e interferenza con il sistema di coagulazione che porta ad uno stato protrombotico.
Gli effetti sul sistema della coagulazione potrebbero svolgere un ruolo importante nelle malattie cardiovascolari correlate al LES attraverso diversi meccanismi. Inoltre ci sono diverse possibilità che non si escludono a vicenda. Un meccanismo specifico su come gli aPL possono causare malattie cardiovascolari come ictus e infarto miocardico nel LES è correlato all’annessina A5 , una proteina nota per legare la fosfatidilserina, che è esposta sulle cellule morte e morenti e che funziona come modello molecolare associato al pericolo (DAMP ).
La natura infiammatoria dell’aterosclerosi è nota da molto tempo. Il LES potrebbe favorire l’aterosclerosi e/o le placche aterosclerotiche.
Allo stesso tempo, l’aterosclerosi è un processo infiammatorio che si sviluppa lentamente nelle arterie. È caratterizzata dall’accumulo di cellule morte, OxLDL e infiltrato attivato di cellule immunocompetenti, comprese le cellule T, monociti/macrofagi e anche cellule muscolari lisce, ma non molti granulociti, che sono tipicamente una componente importante nell’artrite come nell’artrite reumatoide. artrite.
Le cellule T e i monociti/macrofagi mostrano segni di attivazione e producono citochine, principalmente proinfiammatorie come l’interleuchina 1, 6 e il TNF-alfa e si accumulano vicino alle lesioni e alle parti danneggiate delle placche. Anche la calcificazione è una caratteristica importante dell’aterosclerosi ed è molto probabilmente un fenomeno correlato all’infiammazione prolungata. L’esatto tipo di immunomodulazione e l’effetto antinfiammatorio sono quindi essenziali nel trattamento della CVD con l’obiettivo di migliorare l’infiammazione della placca.
È interessante notare che l’accumulo di cellule morte nelle placche aterosclerotiche è un segno distintivo di questa malattia, che potrebbe essere descritta come eliminazione disfunzionale delle cellule morte. Inoltre, l’OxLDL è un fattore rilevante nell’aterosclerosi e, come le cellule morte, si accumula nelle placche e aumenta il LES.
Da quando è stato stabilito che le cellule T sono presenti nelle placche aterosclerotiche e producono attivamente anche citochine proinfiammatorie, il loro ruolo funzionale nello sviluppo della malattia cardiovascolare è stato ampiamente studiato e discusso. Sebbene resti ancora molto da sapere sul ruolo dell’IL-17 e delle corrispondenti cellule Th17 e anche di altri sottogruppi di cellule T proinfiammatorie, sembrano essere principalmente proaterogeniche.
Uno squilibrio nel sistema immunitario con una percentuale inferiore di cellule T regolatorie (Tregs) è un’altra caratteristica del LES e un esempio di calibrazione immunitaria. Le Treg sono importanti per la soppressione delle reazioni autoimmuni contro se stessi .
Le cellule T regolatorie (Treg) possono sopprimere gli effetti proinfiammatori e hanno anche altre proprietà interessanti che potrebbero migliorare l’aterosclerosi, come l’inibizione della formazione di cellule schiumose e l’induzione di macrofagi antinfiammatori.
Un’opzione terapeutica nelle malattie autoimmuni, soprattutto nel LES, potrebbe essere quella di aumentare la proporzione delle cellule T regolatorie (Treg), per ripristinare l’equilibrio con le cellule T effettrici. Le opzioni includono composti che attivano le Treg come l’interleuchina-2 a basso dosaggio.
La causa alla base della bassa percentuale di cellule T regolatorie (Treg) nel LES non è chiara, ma potrebbe essere correlata all’ambiente delle citochine, che promuove il declino cellulare. Esistono anche altre possibilità interessanti in relazione sia all’aterosclerosi che al LES, tra cui OxLDL e i cosiddetti anticorpi naturali, in particolare anti-PC e la proteina plasmatica annessina A5.
Poiché l’ossidazione rimane un denominatore comune, viene comunemente utilizzato il termine OxLDL. L’OxLDL è stato sotto i riflettori come colpevole dell’aterosclerosi almeno dalla fine degli anni ’80. Viene assorbito dai macrofagi , che diventano cellule schiumose inerti nelle lesioni aterosclerotiche, dove alla fine muoiono e diventano parte di un nucleo necrotico. OxLDL promuove la morte cellulare e ha proprietà proinfiammatorie e immunostimolanti.
Un’altra causa non reciprocamente esclusiva degli effetti proinfiammatori e dell’attivazione immunitaria da parte di OxLDL è la fosforilcolina (PC), che in studi precedenti è stata segnalata per svolgere un ruolo nell’attivazione immunitaria indotta da OxLDL e nella produzione della principale citochina proinfiammatoria IFNgamma. .
La CVD è, quindi, una causa considerevole di morbilità e mortalità nel LES ed è causata da una combinazione di fattori con proprietà protrombotiche e/o aterogene. I fattori di rischio tradizionali, come l’ipertensione, l’iperlipidemia e il diabete, dovrebbero essere ridotti mediante terapie consolidate nella prevenzione generale delle malattie cardiovascolari. Recentemente sono stati pubblicati dati positivi sull’uso delle statine, sia nell’iperlipidemia che nell’APS nel LES.
Un’altra questione importante è quale ruolo gioca il trattamento con corticosteroidi nelle malattie cardiovascolari correlate al LES. Esistono associazioni tra alte dosi di corticosteroidi e malattie cardiovascolari nel LES, ma d’altro canto questi pazienti sono quelli che presentano le manifestazioni più gravi e, ancora una volta, è importante ottimizzare la terapia affinché le manifestazioni più acute della malattia siano trattato nel miglior modo possibile.
L’idrossiclorochina è una pietra angolare nel trattamento del LES e, cosa interessante, ha anche un ruolo nella prevenzione delle malattie cardiovascolari . In una recente meta-analisi, l’idrossiclorochina ha dimostrato di ridurre il rischio di eventi tromboembolici del 49%.
Il rischio di malattie cardiovascolari è elevato nel LES ed è causato sia da un aumento del rischio di trombosi che da un aumento dell’aterosclerosi, in particolare delle placche aterosclerotiche.
Ciò rappresenta un importante problema clinico, ma potrebbe anche far luce sulla natura infiammatoria e immunologica dell’aterosclerosi. Una combinazione di fattori di rischio tradizionali e non tradizionali, compresi quelli legati al LES come attività patologica, sembrano spiegare questo aumento del rischio. Per la prevenzione e il trattamento delle malattie cardiovascolari nel LES è necessario affrontare i tradizionali fattori di rischio e ottimizzare le risorse terapeutiche.